荔枝(Litchi chinensis Sonn.)是无患子科热带果树,主要分布在我国两广、海南、福建和台湾等省份,是我国华南地区栽培面积最大的果树之一[1]。妃子笑是中国荔枝产区的主要品种之一,其果肉芳香、细嫩、甘甜多汁,是风味极佳的优良品种。此外,通过基因编辑和转基因技术已获得妃子笑再生植株[2]。但目前已报道的荔枝品种体胚分化数量少且体胚高度不同步,导致其再生效率较低,严重限制了荔枝生物育种进程[3-5]。
研究发现,悬浮培养通过液体振荡优化了营养、激素及不同形态细胞的分布,可显著提升体胚发生效率[6],已在三棱果[7]、云杉[8]等较多木本植物中成功实现再生。俞长河等[9]在荔枝胚性悬浮培养体系构建方面取得了初步进展,建立了包括下番枝、元红及乌叶在内的3个品种的胚性悬浮培养物,但该体系仍存在愈伤组织及体胚发育不同步的问题。为进一步提升培养效率,赖钟雄等[10]在对该体系进行了优化,通过选用淡黄色、颗粒状且状态一致的胚性愈伤组织作为起始悬浮材料,成功构建了下番枝荔枝的胚性悬浮细胞系。该体系获得的愈伤组织可在固体培养基上直接诱导体胚发生,体胚发生数量达10 000个·g-1以上,且其中75%以上的成熟体胚均能够正常萌发并形成完整植株。上述研究为减少荔枝畸形胚比例、提高体胚同步化水平奠定了重要基础。
本研究拟在前期已建立的妃子笑离体再生技术的基础上[11],以其花药愈伤组织为材料,系统探究肌醇、2,4-D、蔗糖、水解乳蛋白、椰汁和起始接种量对悬浮细胞生理状态的影响,旨在建立高效的悬浮培养体系,以提高妃子笑荔枝体胚分化效率,为荔枝离体再生、细胞工程育种和诱变育种提供技术支撑,加速优质新种质的选育进程。
1 材料和方法
1.1 材料
供试材料为妃子笑荔枝花药愈伤组织,在基础继代培养基M3(MS+1.0 mg·L-1 2, 4-D)和M4(MS+1.0 mg·L-1 2, 4-D+0.5 mg·L-1 KT+5.0 mg·L-1 AgNO3)上交替继代培养进行保存[10]。
1.2 方法
1.2.1 胚性细胞悬浮培养 (1)不同肌醇浓度对悬浮细胞生长的影响。选取疏松、干燥、易碎、生长旺盛的颗粒状胚性愈伤组织各1 g,分别接种于50 mL含不同肌醇浓度的5组液体培养基。以MS+2 mg·L-1 2, 4-D+30 g·L-1蔗糖为基本培养基,分别添加不同浓度(ρ,后同)的肌醇(0、0.05、0.10、0.15、0.20 g·L-1),以不含肌醇的处理作为对照。
(2)不同2,4-D浓度对悬浮细胞生长的影响。在上述确定的最适肌醇浓度基础上,以MS+30 g·L-1蔗糖 +0.15 g·L-1肌醇为基本培养基,分别添加不同浓度的2,4-D(0、0.1、0.5、1.0、2.0 mg·L-1),以不含2,4-D的处理作为对照。
(3)不同蔗糖浓度对悬浮细胞生长的影响。在上述确定的最适肌醇和2,4-D浓度基础上,以MS+0.15 g·L-1肌醇+1 mg·L-1 2, 4-D为基本培养基,分别添加不同浓度的蔗糖(0、10、20、30、40 g·L-1),以不含蔗糖的处理作为对照。
(4)不同水解乳蛋白浓度对悬浮细胞生长的影响。在上述确定的最适肌醇、2,4-D和蔗糖浓度基础上,以MS+0.15 g·L-1 肌醇+1 mg·L-1 2, 4-D+20 g·L-1蔗糖为基本培养基,分别添加不同浓度的水解乳蛋白(0、0.2、0.3、0.4 g·L-1),以不含水解乳蛋白的处理作为对照。
(5)不同椰汁浓度对悬浮细胞生长的影响。在上述确定的最适肌醇、2,4-D和蔗糖浓度基础上,以MS+0.15 g·L-1肌醇+1 mg·L-1 2, 4-D+20 g·L-1 蔗糖为基本培养基,分别添加不同浓度的椰汁(0、50、100、150、200 mL·L-1),以不含椰汁的处理作为对照。
(6)不同起始接种量对悬浮细胞生长的影响。在上述确定的最适肌醇、2,4-D、蔗糖和椰汁浓度基础上,将愈伤组织接种于MS+0.15 g·L-1肌醇+1 mg·L-1 2, 4-D+20 g·L-1 蔗糖+50 mL·L-1椰汁培养基上,接种量分别为10、20、30和40 g·L-1。
起始继代培养时,每 4 d继代1次,将装有悬浮培养物的三角瓶静置10 min,轻轻向下倾斜瓶口倒掉约2/3上清液,再加入相同体积的新鲜培养基。经过3次继代培养后,使用0.85 mm孔径的无菌不锈钢筛网过滤悬浮培养物,收集通过孔径筛网的细小、均匀的悬浮细胞颗粒,补充新鲜培养基继续培养7 d,测定悬浮单细胞和细胞团的生成率、单细胞成活率、鲜质量(fresh weight,FW)和干质量(dry weight,DW)。
单细胞及细胞团密度:用血球计数板对样品进行计数。将样品稀释至适宜浓度后,滴加至计数板,在光学显微镜下(20~25倍)统计中央大方格内单细胞及细胞团的数量,重复3次取平均值。
单细胞成活率:取一滴稀释后的细胞悬浮液滴于载玻片上,用0.4% Evans blue进行染色,被染为蓝色的为死细胞,未被染色的为活细胞,随机统计5个视野下未被染色的活细胞数,计算平均值。
细胞鲜质量和干质量:将悬浮培养物置于滤纸上充分吸收其表面及筛网上的水分,称质量记为W1;然后洗去筛网上的培养物,将筛网置于滤纸上充分吸干水分,称质量记为W2,细胞FW记为W,则W=W1-W2。将收集的培养物于60 ℃下烘干约12 h至恒重,称质量即为DW。细胞FW和DW均以每50 mL悬浮培养物的质量表示。
细胞密实体积(Packed cell volume,PCV):每2 d取整瓶悬浮培养物置于离心管中,经1000 r·min-1离心5 min后,测量细胞密实体积。
1.2.2 悬浮培养细胞生长特性的检测 选取与1.2.1状态一致的胚性愈伤组织1.5 g,接种于液体培养基(MS+0.15 g·L-1肌醇+1 mg·L-1 2, 4-D+20 g·L-1蔗糖+50 mL·L-1椰汁,pH=5.8,1.2.1筛选的悬浮细胞体系),经3次继代培养后,使用0.85 mm孔径的无菌不锈钢筛网过滤除去大块悬浮培养物后继续培养。每2 d测定相同时间段培养液的细胞FW、DW、PCV,单细胞密度和成活率,培养液的pH值、电导率,连续测定至第16天。其中pH值和电导率值精确至0.01,测量时仪器温度补偿至25 ℃。上述悬浮培养均在黑暗、120 r·min-1条件下进行,每个处理设置3次重复,每次重复5瓶。
1.2.3 悬浮培养胚性愈伤组织增殖 使用移液枪吸取培养7 d的胚性悬浮细胞转移到无菌滤纸上彻底吸干水分。选取小细胞团接种至愈伤组织增殖培养基(MS+1 mg·L-12, 4-D+30 g·L-1蔗糖+3.5 g·L-1结冷胶)上,暗培养20 d。
1.2.4 体胚分化和成熟 将易碎性胚性愈伤组织接种于体胚诱导培养基(MS+0.1 mg·L-1 NAA+5 mg·L-1 KT+0.1 g·L-1肌醇+0.4 g·L-1水解乳蛋白+60 g·L-1蔗糖+100 mL·L-1椰汁+10 g·L-1琼脂),暗培养45 d;将分化的体胚接种于成熟培养基(MS+0.5 mg·L-1 吲哚乙酸+1.0 mg·L-1脱落酸+60 g·L-1蔗糖+100 mL·L-1椰汁+10 g·L-1琼脂),暗培养60 d。
1.2.5 体胚植株再生 将成熟体胚转接至萌发培养基(培养基中均含1 mg·L-1 GA3),每天12 h光照培养,约50 d后统计体胚萌发率(具有茎及根的体胚)与生根率。本研究所用培养基的pH为5.8~6.2,均在(25±2)℃下进行培养。
2 结果与分析
2.1 不同培养条件对悬浮细胞生长的影响
2.1.1 不同肌醇浓度对悬浮细胞生长的影响 胚性愈伤组织接种至液体培养基后会立即小幅度自动散开,刚开始培养时颗粒较大,无浑浊现象,此时多为大块细胞团(图1-A),个别单细胞游离(图1-B,红箭头)。随着培养时间延长(约第3天开始),培养液逐渐浑浊,颜色鲜黄并逐渐褐化(图1-C),细胞质皱缩成团(图1-B,黄箭头),长条形或者不规则形(图1-D,绿箭头),内含物较少。若继续培养,该培养物难以成活,需要每隔3~4 d更换培养液以去除褐化、死亡培养物。经过3~4次继代培养后,使用0.85 mm孔径的筛网过滤块状愈伤组织,收集颜色鲜黄、颗粒细小的悬浮培养物(图1-E);继续培养后,悬浮细胞趋向近圆形,内含物逐渐丰富,小细胞团渐多(图1-D)。

图1 荔枝悬浮细胞的培养过程
Fig. 1 Culture process of litchi suspension cells
接种初期,各处理组细胞形态差异不明显,不含肌醇的培养液中细胞呈块状,仅少数单细胞游离。培养7 d后发现,随着肌醇浓度升高(0~0.10 g·L-1),小细胞团比例逐渐增大,游离的单细胞比例逐渐降低;部分细胞逐渐转变为椭圆形,颗粒状内含物也逐渐丰富。当肌醇浓度为0.15 g·L-1时,单细胞成活率、细胞团分散度及培养物FW、DW等指标均较高(图2)。此后继续提高肌醇浓度,上述生长指标随之下降。
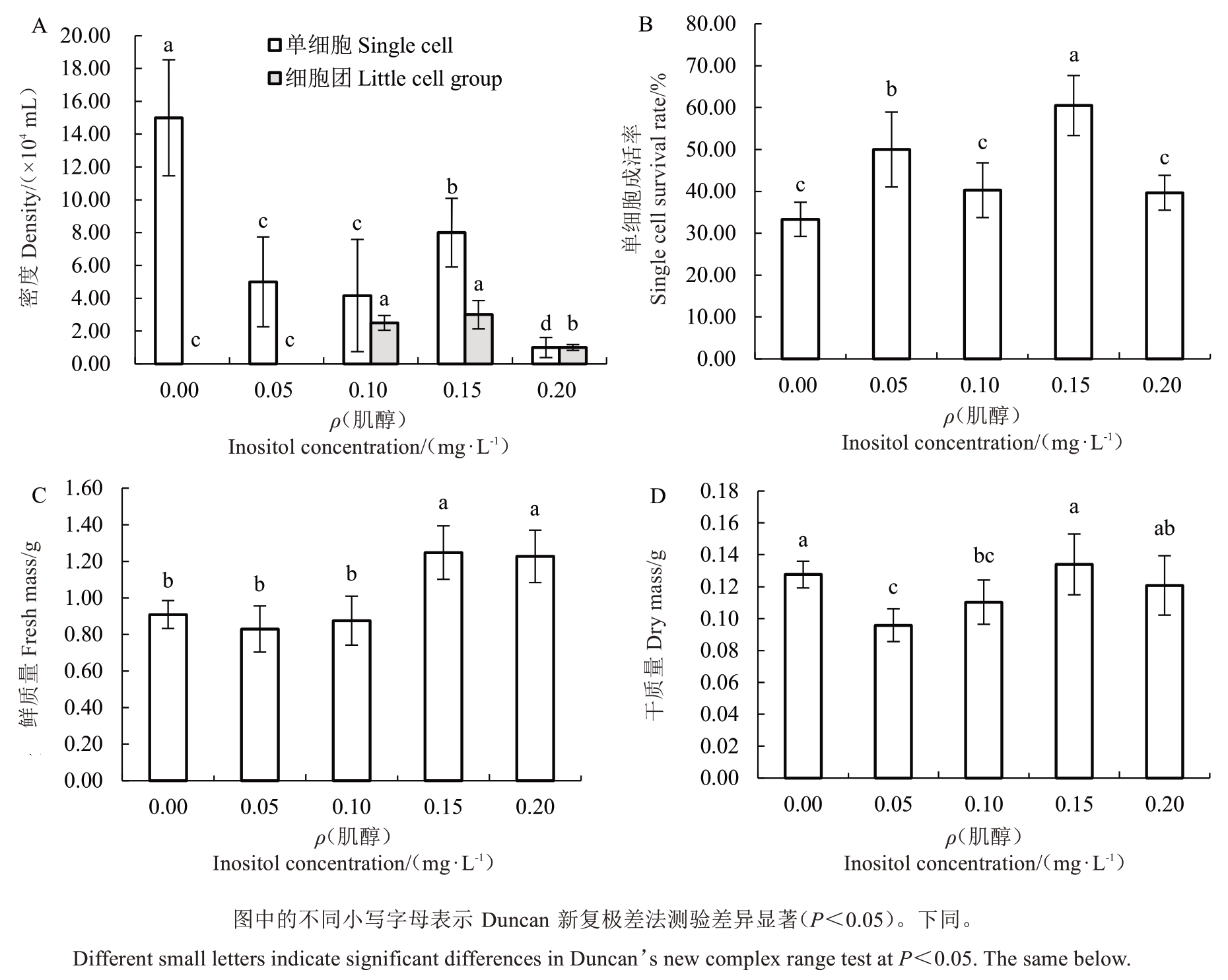
图2 肌醇对荔枝悬浮细胞生长的影响
Fig. 2 Effect of inositol on the growth of litchi suspension cells
2.1.2 不同2,4-D浓度对悬浮细胞生长的影响 2,4-D浓度对悬浮细胞生长具有显著调控作用。当2,4-D浓度在0~0.10 g·L-1之间时,细胞质量与单细胞成活率随其浓度增加而升高。单细胞密度和鲜质量在 1.0 mg·L-1 2,4-D处理下最高,而单细胞成活率则在 0.5 mg·L-1时达到峰值(图3)。此时,细胞趋向圆滚饱满,内含物较明显,可见细胞中透明质体活动。之后随着2,4-D浓度升高,悬浮细胞逐渐呈管状,细胞质皱缩至一端,细胞碎片增多。
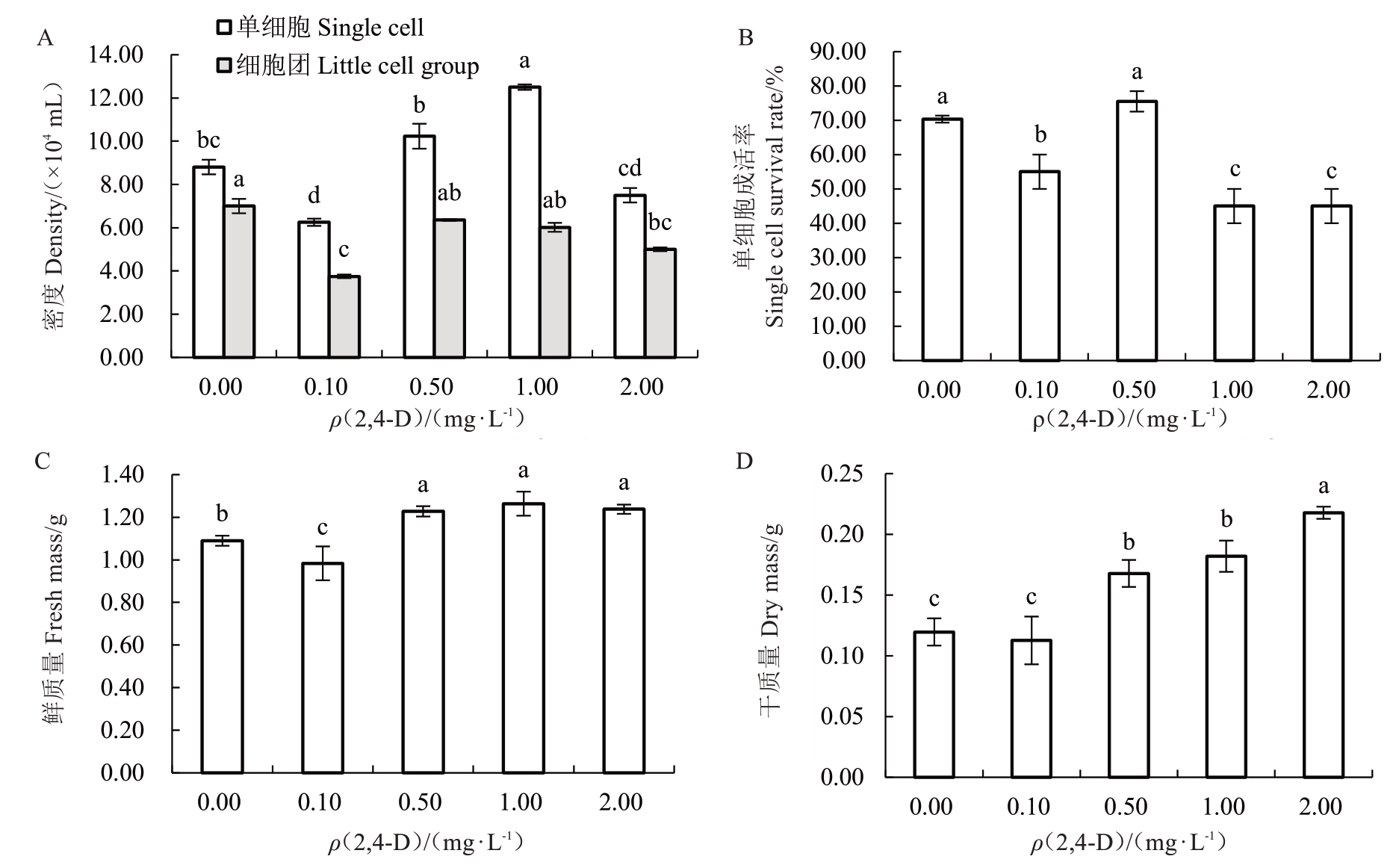
图3 2,4-D对荔枝悬浮细胞生长的影响
Fig. 3 Effect of 2,4-D on the growth of litchi suspension cells
2.1.3 不同蔗糖浓度对悬浮细胞生长的影响 悬浮细胞质量随蔗糖浓度升高而增大(图4),当蔗糖浓度为20 g·L-1时,单细胞及小细胞团数量较多,单细胞成活率最高,大部分细胞呈圆形,细胞生长旺盛。但随着蔗糖浓度升高,悬浮分散的单细胞占比逐渐减小,单细胞成活率骤降。
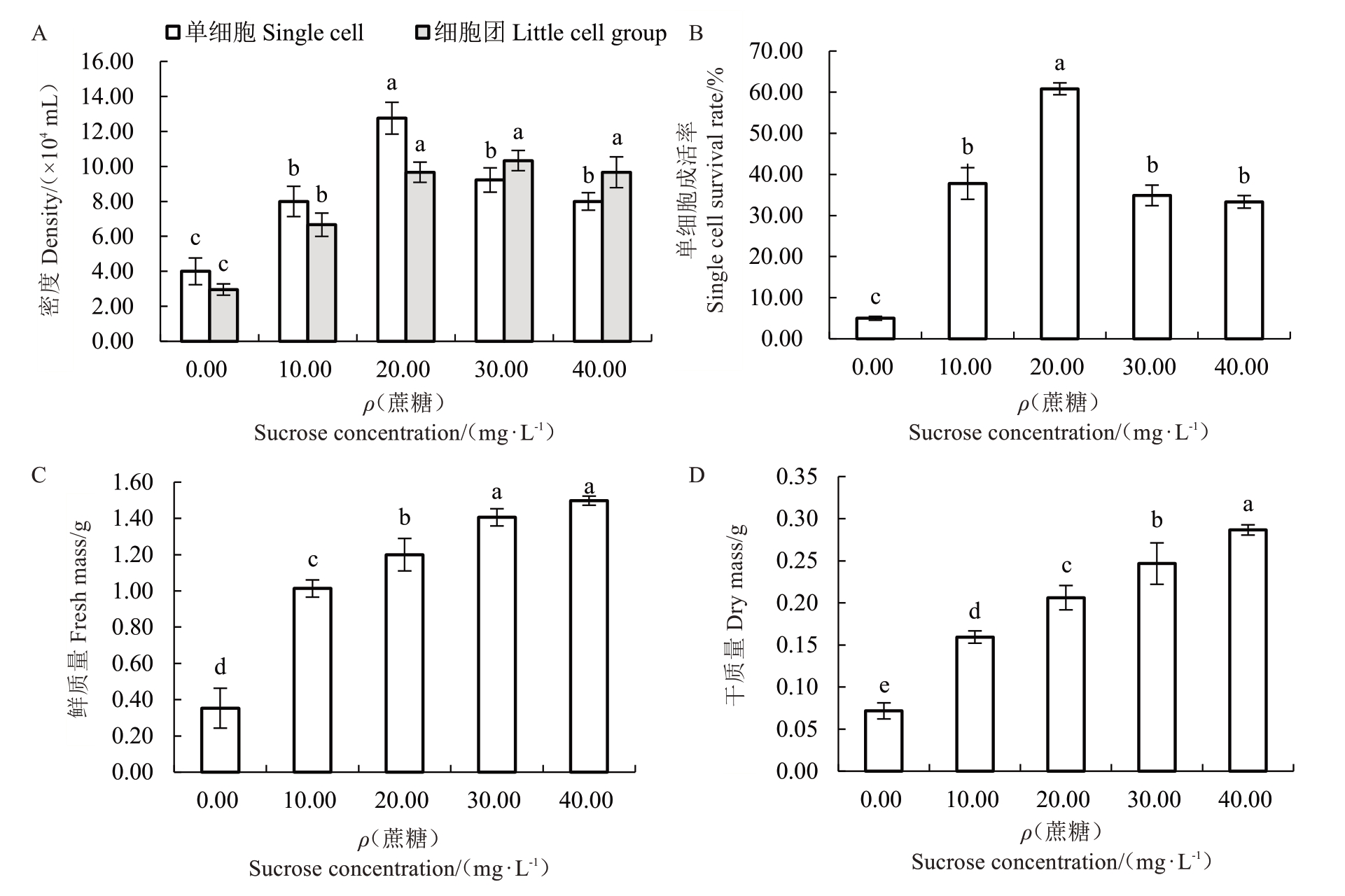
图4 蔗糖对荔枝悬浮细胞生长的影响
Fig. 4 Effect of sugar on the growth of litchi suspension cells
2.1.4 不同水解乳蛋白浓度对悬浮细胞生长的影响 悬浮细胞的生长状态与水解乳蛋白浓度呈负相关(图5)。在含水解乳蛋白的培养液中,分散的单细胞与细胞团数量、单细胞成活率及悬浮细胞FW、DW均降低;且随着水解乳蛋白浓度升高,细胞多为小细胞团,细胞由圆形逐渐变成长条形,细胞质皱缩成团,死亡细胞碎片逐渐增多。
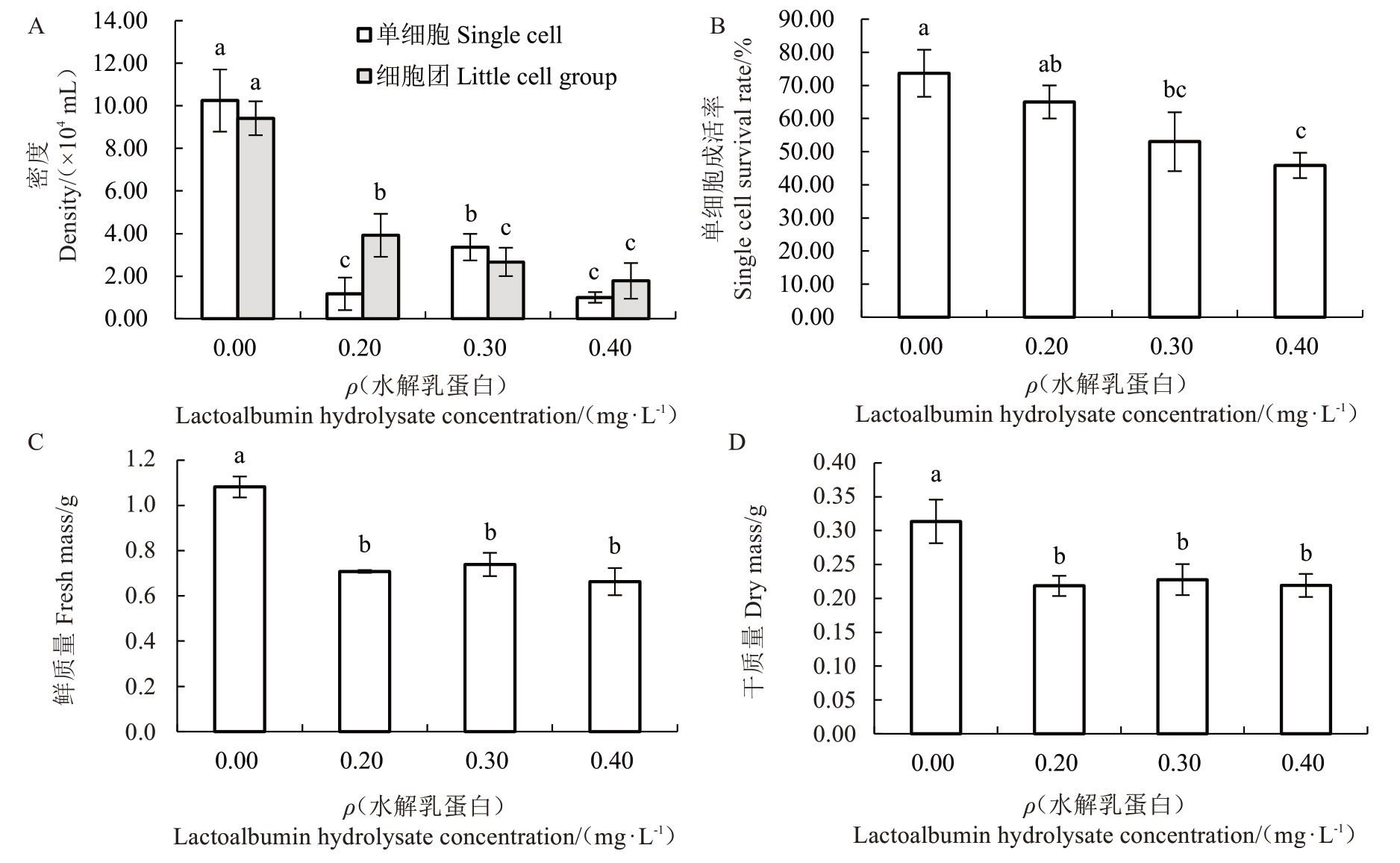
图5 水解乳蛋白对荔枝悬浮细胞生长的影响
Fig. 5 Effect of lactalbumin hydrolysate on the growth of litchi suspension cells
2.1.5 不同椰汁浓度对悬浮细胞生长的影响 不同椰汁浓度下,悬浮细胞生长状态存在差异(图6)。当椰汁浓度为50 mL·L-1时,单细胞数量、单细胞成活率、FW及DW均较高,但细胞团数量降低;当椰汁浓度为100 mL·L-1时,单细胞数量、单细胞成活率及培养物质量骤降,但细胞团数量显著增加。当椰汁浓度持续增大时,单细胞数量和培养物质量持续上升,单细胞成活率和细胞团数量则表现为先降低后上升。
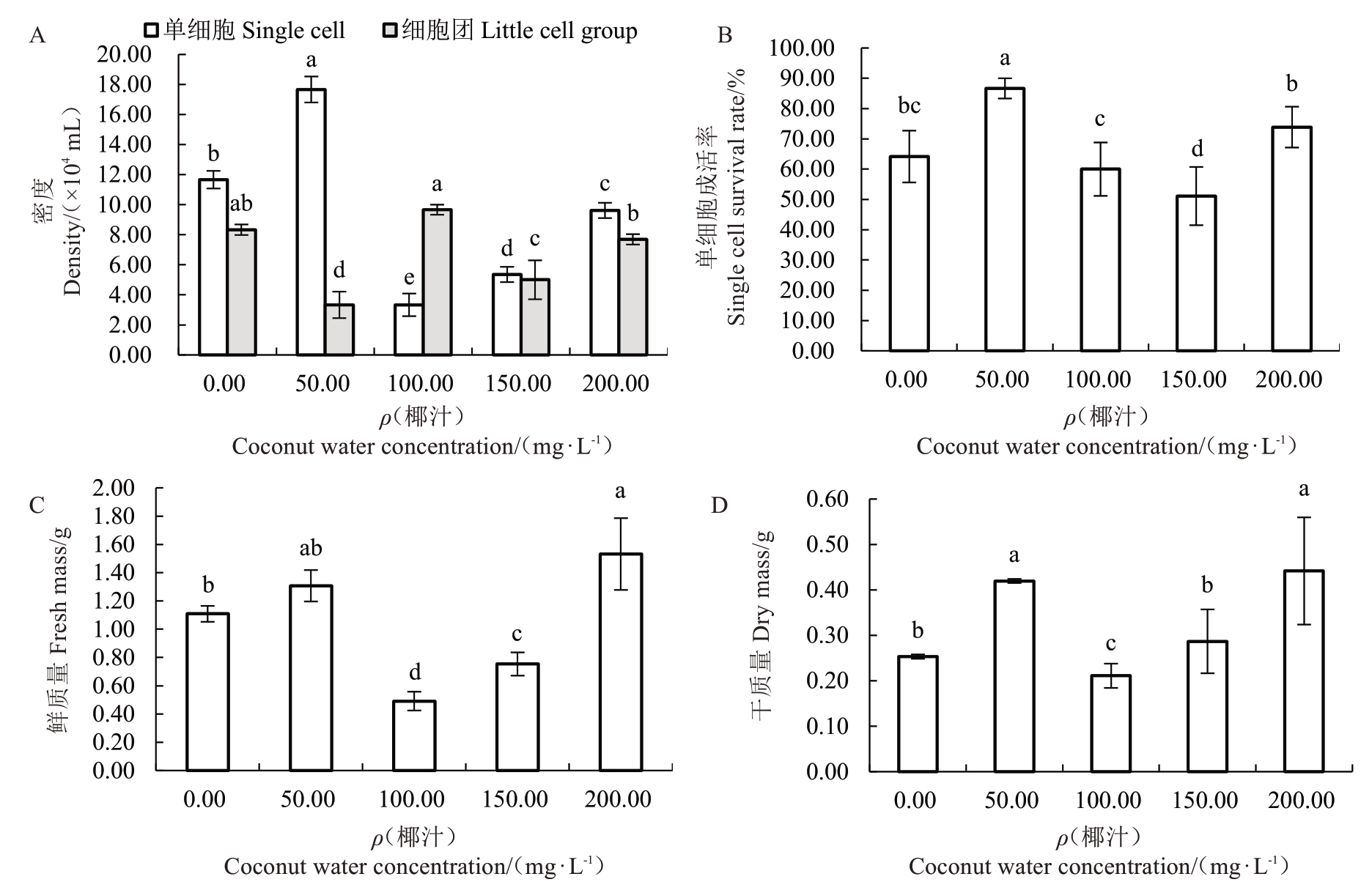
图6 椰汁对荔枝悬浮细胞生长的影响
Fig. 6 Effect of coconut juice on the growth of litchi suspension cells
2.1.6 不同起始接种量对悬浮细胞生长的影响 起始接种量不仅决定了悬浮细胞的形成与维持时间,也显著影响细胞数量、成活率及质量(图7)。本研究发现,最适起始接种量为30 g·L-1。在此条件下,悬浮培养物呈淡黄色、易分散、细胞大小均一、形态一致;细胞团主要由6~15个细胞聚合而成,培养液清澈透亮。上述生长特性指标均随起始接种量的增加而呈现先升后降的趋势。当起始接种量较低时,悬浮细胞颜色虽鲜黄,但单细胞和小细胞团分散较少,表明群体效应不显著;而当起始接种量提高至40 g·L-1时,培养液开始浑浊,部分细胞粘连于瓶壁,并出现褐化趋势;镜检可见细胞内含物减少、液泡增大,单细胞成活率下降。
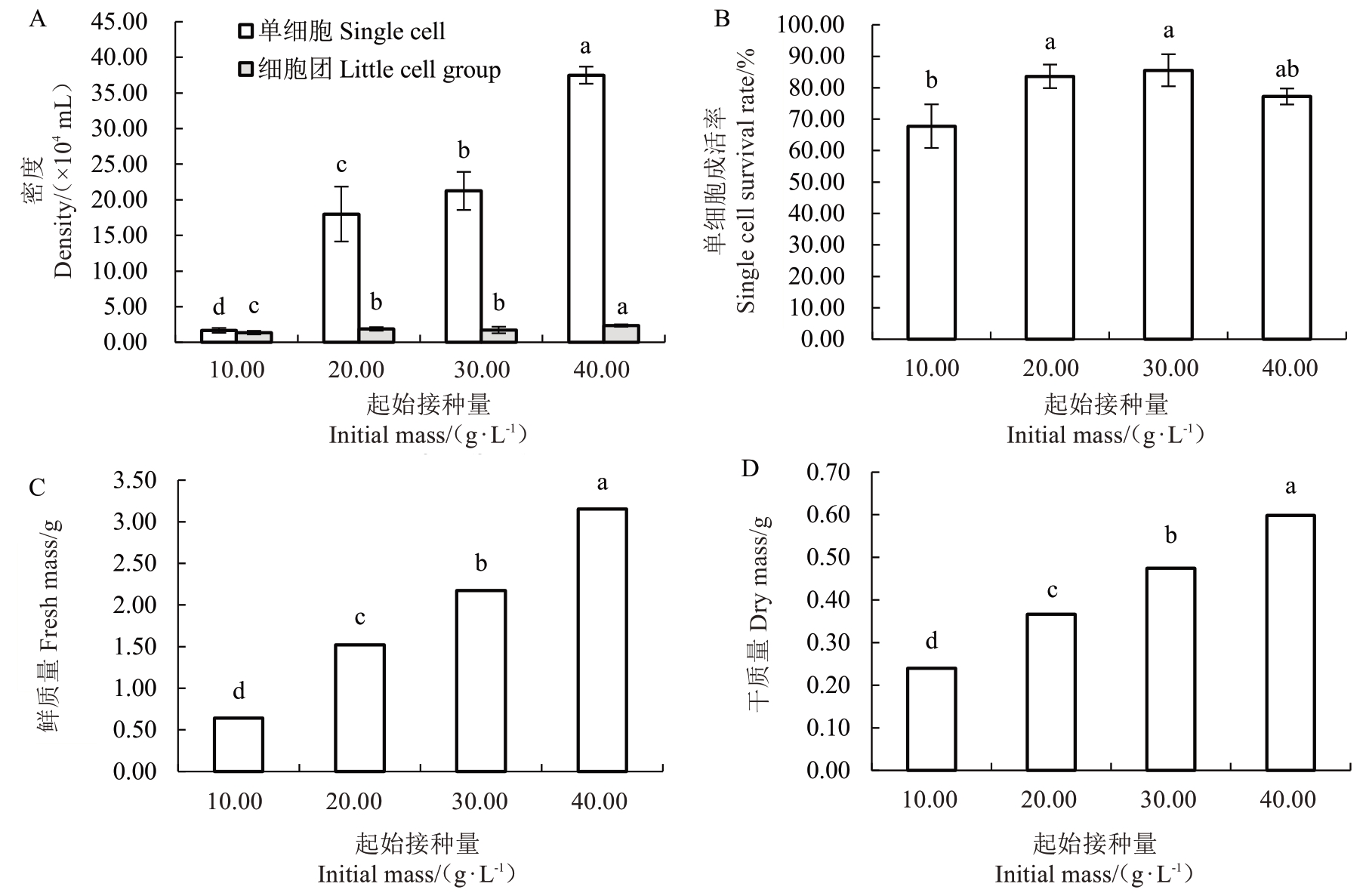
图7 起始接种量对荔枝悬浮细胞生长的影响
Fig. 7 Effect of initial weight on the growth of litchi suspension cells
2.2 悬浮细胞培养参数测定
在30 g·L-1最适起始接种量下,悬浮单细胞数量、培养物FW及PCV的生长曲线均呈典型的“S”型(图8)。悬浮细胞的培养过程大致可划分为延迟期(1~2 d),对数生长期(3~6 d)和稳定期(7~16 d)三个阶段。延迟期内,单细胞分散较少,FW、DW和PCV增长缓慢;进入对数生长期后,细胞快速分裂,各项生长指标均迅速上升;培养至7~10 d后,生长趋于平缓,进入稳定期。根据该生长动态,确定最适宜继代周期为6~8 d。此后若继续培养,细胞逐渐衰老、死亡并形成碎片,导致单细胞数量及成活率急剧下降,FW、DW和PCV仅略有增加或维持不变。
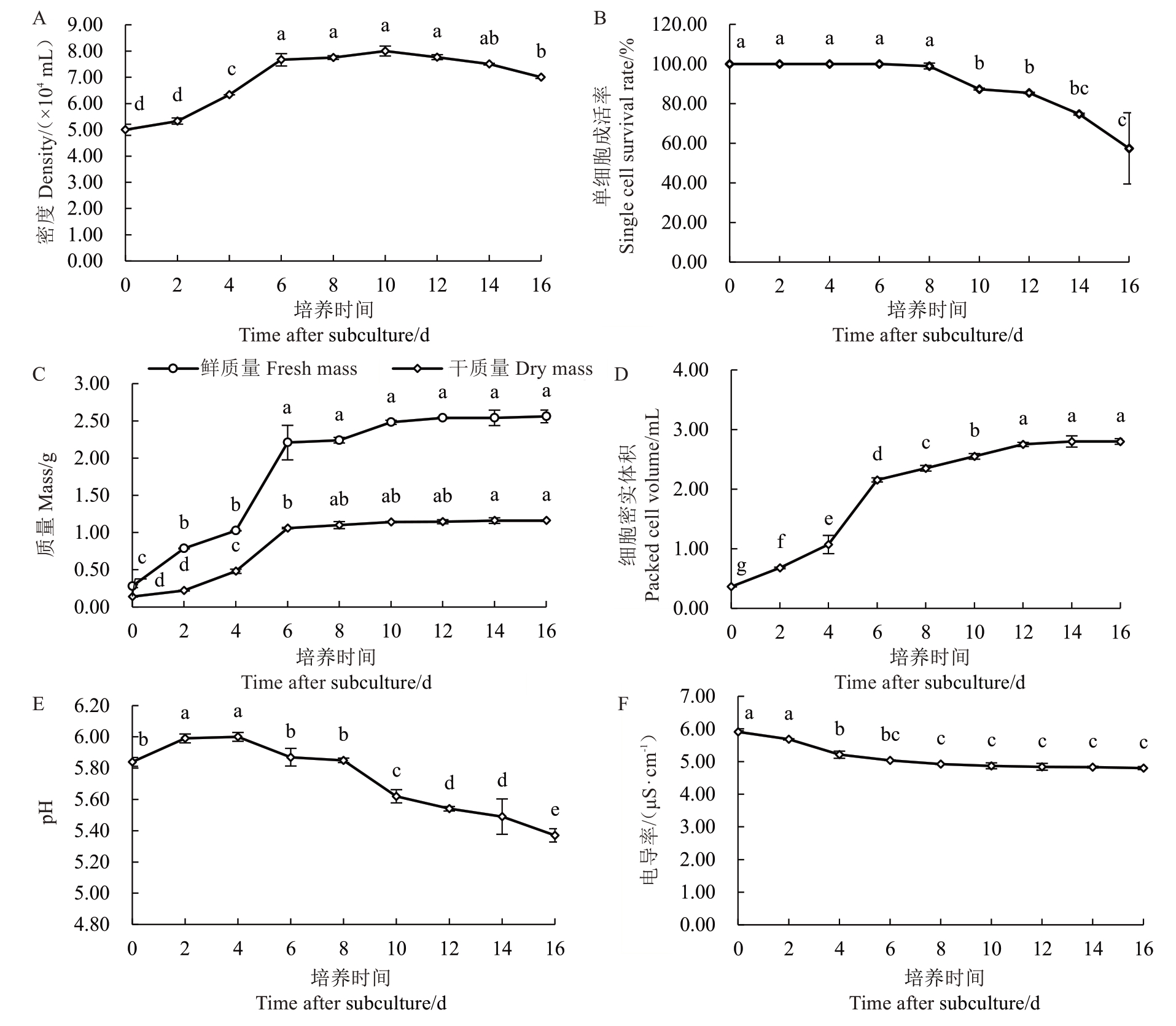
图8 荔枝悬浮细胞生长参数测定
Fig. 8 Determination of growth parameters in litchi suspension culture
伴随上述生长过程,培养液环境也发生规律性变化。接种前培养液pH值为5.84,继代培养第2~4天略升至约6.00,第4~8天回落至约5.85,之后持续缓慢下降至5.37。电导率则在培养0~8 d时持续下降,其中第2~4天降幅最大;第4~8天下降趋缓;第8天后平缓下降,至第16天降至约4.83 μS·cm-1并趋于稳定。
2.3 悬浮细胞植株再生
将悬浮培养物接种至固体培养基上进行增殖(图9-A)。培养约20 d后,将其转移至体胚分化培养基诱导分化(图9-B)。待体胚发育成熟后,再接种至萌发培养基上,继续培养约50 d即可获得完整再生植株(图9-C~D)。

图9 荔枝悬浮细胞再生植株
Fig. 9 Plant regeneration from suspension cell in litchi
不同基本培养基对体胚萌发与生根的影响不同(表1)。MS培养基的体胚萌发率显著高于B5培养基,而B5培养基上的体胚生根率则更高。不同稀释浓度MS培养基的影响也存在差异,其中1/3 MS培养基的体胚萌发率最高,其生根率也保持在较高水平。固体培养基上的体胚萌发率和生根率远高于半固体和液体培养基。半固体、液体培养基对体胚萌发率无较大影响,但对生根率影响较大,半固体培养基的体胚生根率较高。
表1 不同基本培养基对妃子笑体胚萌发的影响
Table 1 Effects of different base media on somatic embryos regeneration
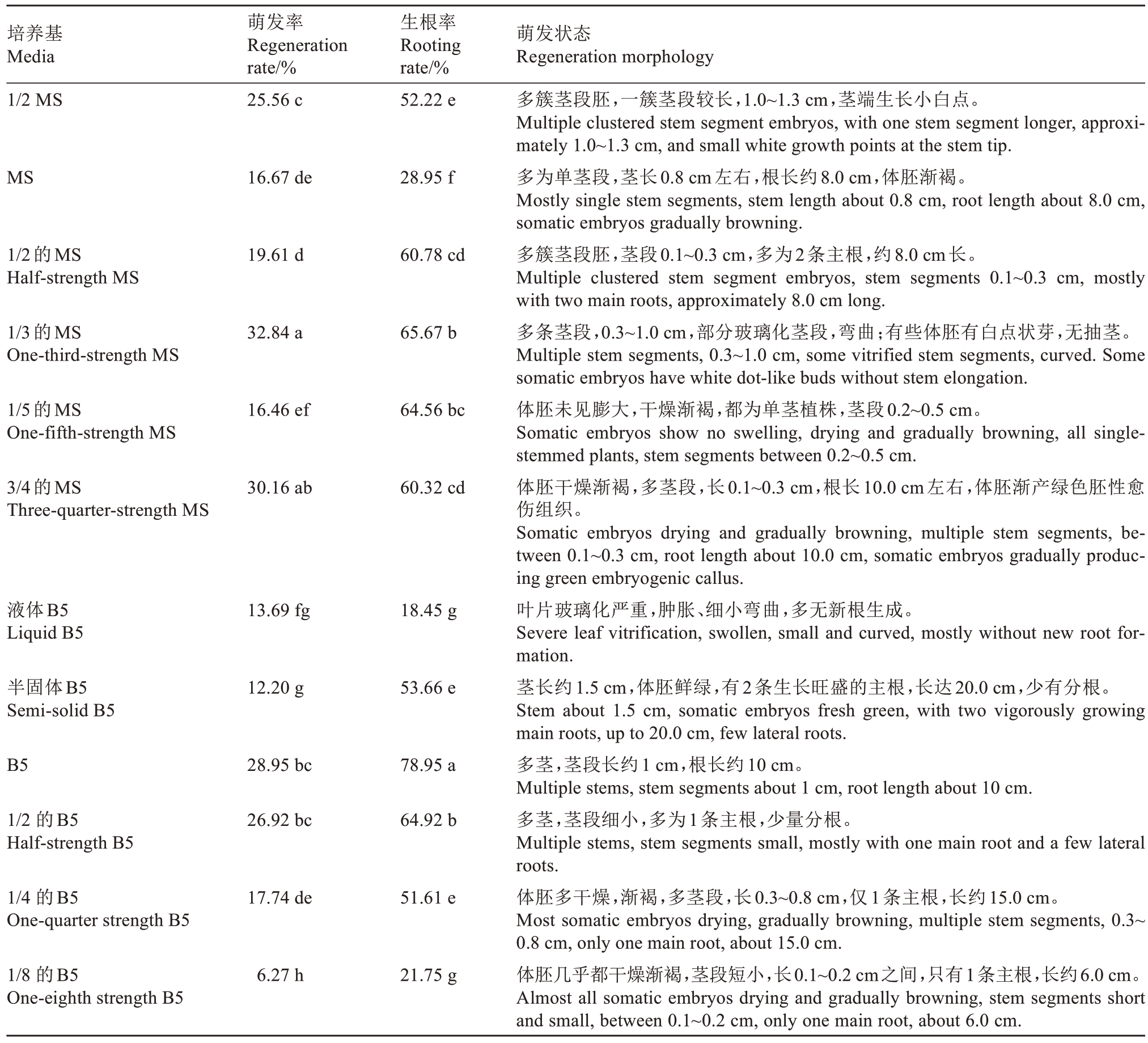
注:1/2 MS购自Phytotechnology Laboratories的商用预混粉末制剂(产品代码:M153)。1/2的MS:将MS培养基所有成分稀释一半。表中同一列数据后的不同小写字母表示Duncan新复极差法测验差异显著(P<0.05)。下同。
Note:1/2 MS, a commercial, pre-mixed powder formulation purchased from Phytotechnology Laboratories (Product Code:M519). Half-strength MS medium was prepared by diluting the full-strength MS macro- and micronutrient stock solutions to 50% of the standard concentration. Different small letters in the same column indicate significant differences in Duncan's new complex range test at P<0.05. The same below.
萌发率Regeneration rate/%25.56 c生根率Rooting rate/%52.22 e萌发状态Regeneration morphology多簇茎段胚,一簇茎段较长,1.0~1.3 cm,茎端生长小白点。Multiple clustered stem segment embryos, with one stem segment longer, approximately 1.0~1.3 cm, and small white growth points at the stem tip.多为单茎段,茎长0.8 cm左右,根长约8.0 cm,体胚渐褐。Mostly single stem segments, stem length about 0.8 cm, root length about 8.0 cm,somatic embryos gradually browning.多簇茎段胚,茎段0.1~0.3 cm,多为2条主根,约8.0 cm长。Multiple clustered stem segment embryos, stem segments 0.1~0.3 cm, mostly with two main roots, approximately 8.0 cm long.多条茎段,0.3~1.0 cm,部分玻璃化茎段,弯曲;有些体胚有白点状芽,无抽茎。Multiple stem segments, 0.3~1.0 cm, some vitrified stem segments, curved. Some somatic embryos have white dot-like buds without stem elongation.体胚未见膨大,干燥渐褐,都为单茎植株,茎段0.2~0.5 cm。Somatic embryos show no swelling, drying and gradually browning, all singlestemmed plants, stem segments between 0.2~0.5 cm.体胚干燥渐褐,多茎段,长0.1~0.3 cm,根长10.0 cm左右,体胚渐产绿色胚性愈伤组织。Somatic embryos drying and gradually browning, multiple stem segments, between 0.1~0.3 cm, root length about 10.0 cm, somatic embryos gradually producing green embryogenic callus.叶片玻璃化严重,肿胀、细小弯曲,多无新根生成。Severe leaf vitrification, swollen, small and curved, mostly without new root formation.茎长约1.5 cm,体胚鲜绿,有2条生长旺盛的主根,长达20.0 cm,少有分根。Stem about 1.5 cm, somatic embryos fresh green, with two vigorously growing main roots, up to 20.0 cm, few lateral roots.多茎,茎段长约1 cm,根长约10 cm。Multiple stems, stem segments about 1 cm, root length about 10 cm.多茎,茎段细小,多为1条主根,少量分根。Multiple stems, stem segments small, mostly with one main root and a few lateral roots.体胚多干燥,渐褐,多茎段,长0.3~0.8 cm,仅1条主根,长约15.0 cm。Most somatic embryos drying, gradually browning, multiple stem segments, 0.3~0.8 cm, only one main root, about 15.0 cm.体胚几乎都干燥渐褐,茎段短小,长0.1~0.2 cm之间,只有1条主根,长约6.0 cm。Almost all somatic embryos drying and gradually browning, stem segments short and small, between 0.1~0.2 cm, only one main root, about 6.0 cm.培养基Media 1/2 MS MS 16.67 de 28.95 f 1/2的MS Half-strength MS 19.61 d 60.78 cd 1/3的MS One-third-strength MS 32.84 a 65.67 b 1/5的MS One-fifth-strength MS 16.46 ef 64.56 bc 3/4的MS Three-quarter-strength MS 30.16 ab 60.32 cd液体B5 Liquid B5 13.69 fg 18.45 g半固体B5 Semi-solid B5 12.20 g 53.66 e B5 28.95 bc 78.95 a 1/2 的B5 Half-strength B5 26.92 bc 64.92 b 1/4 的B5 One-quarter strength B5 17.74 de 51.61 e 1/8 的B5 One-eighth strength B5 6.27 h 21.75 g
3 讨 论
悬浮细胞密度、单细胞成活率及生长状态是衡量悬浮培养体系的重要指标[12],本研究在荔枝[10]、龙眼[12]、梨[13]等果树悬浮培养体系的基础上发现肌醇、激素、碳源和椰汁等附加物,以及起始接种量均影响妃子笑胚性细胞的悬浮培养效率。其中,肌醇和激素是建立及维持胚性细胞悬浮培养较为关键的因素[14],其浓度因作物种类及品种而异,肌醇常用浓度为0.05~0.1g·L-1,2,4-D常用浓度为0.5~1.0 mg·L-1。在本研究中,0.15 g·L-1 肌醇对妃子笑荔枝愈伤组织细胞分裂、单细胞成活率作用显著,这与肌醇在金茶花悬浮细胞生长中的促进作用一致[15]。
前人研究表明,2,4-D浓度需维持在一定范围方能有效保持悬浮细胞的胚性。过低或过高的浓度均不利于胚性维持,前者易导致细胞分裂过快、单细胞成活率降低[16-17];后者则会抑制细胞生长,导致空细胞增多、细胞褐化[17]。魏岳荣等[16]在贡蕉悬浮细胞培养中发现,使用0.5 mg·L-1 2,4-D建立的细胞系,继代培养8个月后胚性逐渐丧失。同一研究指出,在1 mg·L-1 2,4-D下建立的贡焦悬浮细胞,在继代培养20个月后仍保持较强的体胚发生能力。林秀莲等[17]报道,当2,4-D浓度高于0.5 mg·L-1 时,相思悬浮细胞生长受抑,表现为空细胞增多,颜色黯淡并最终褐化。然而在本研究的妃子笑荔枝胚性悬浮细胞培养体系中,在1 mg·L-1 2,4-D条件下,悬浮单细胞及细胞团的数量与FW均维持在较高水平,且细胞形态近圆形、饱满。
蔗糖是大多数作物细胞生长的主要碳源[18],椰汁因营养成分均衡,常用于作物离体再生[19],二者主要通过调节渗透势影响悬浮细胞成长。本研究发现,妃子笑荔枝胚性愈伤组织悬浮培养所需的蔗糖浓度与下番枝相同[10],且所需蔗糖与椰汁浓度均略低于其在固体培养基中的浓度[11]。推测这可能是由于振荡培养使悬浮细胞更均匀地接触养分与氧气,提高了营养利用效率,从而在相对较低的蔗糖与椰汁浓度下,仍可支持细胞的快速增殖。水解乳蛋白是多种氨基酸的混合物,可作为植物组织培养的有机氮源[20]。但本研究发现,水解乳蛋白抑制妃子笑荔枝悬浮细胞的生长,这一现象与黄芩悬浮细胞中代谢物生产受抑制的结果一致[21],推测其原因可能是:一方面,其中某类氨基酸浓度过高产生了抑制作用;另一方面,小分子肽与糖类(如蔗糖)的协同作用可能改变了体系的碳氮比,进而抑制了荔枝悬浮细胞的分裂与生长。
起始接种量是决定悬浮培养体系建成时间与细胞生长周期的关键因素[22-23],本研究结果显示,起始接种量过低或过高均不利于悬浮细胞的正常生长。具体而言,起始接种量过低时,细胞难以形成有效的群体效应,导致其生长速率显著降低甚至停滞;而起始接种量过高时,则会因细胞间对养分的激烈竞争而缩短对数生长期,进而引起细胞成活率下降、死细胞碎片增多,并加速细胞群体的衰亡进程。在本研究条件下,胚性愈伤组织以30 g·L-1作为起始接种量时,悬浮细胞成活率最高,最有利于保持细胞良好的生长状态。
本研究测定了荔枝胚性悬浮细胞在一个生长周期(16 d)内培养液pH、电导率和细胞生物量的变化。在接种初期,培养液pH先微升后大幅度下降,由适宜生长的5.99迅速下降至5.37;电导率则随着培养时间延长持续下降,这些变化可能是接种后悬浮细胞为应对逆境作出的适应性调节。随着悬浮细胞的生长发育,大量细胞代谢产物释放至培养液中,同时伴随着细胞衰老死亡,共同导致培养液pH及电导率迅速下降,这种变化与橡胶[24]等悬浮细胞的生长特性相似。因此,根据测定的悬浮细胞生长曲线可为确定细胞继代周期提供重要的参考依据。
与下番枝愈伤组织经悬浮培养后直接用于体胚诱导的方法不同[10],本研究中妃子笑愈伤组织经悬浮培养后,先在固体培养基上进行增殖,再用于体胚诱导,这可有效减轻玻璃化及体胚发生不同步现象,从而使体胚萌发率和生根率均高于固体培养基上的再生效率[11]。但是,由于妃子笑荔枝悬浮培养体系采用固-液交替培养方式,其愈伤组织细胞处于多细胞团状态。因此,为获得悬浮系或者单细胞培养系,需进行多次连续的过筛培养,而长期液体培养是否会影响愈伤组织细胞胚性及如何改进仍需进一步研究。
本研究结果可初步应用于荔枝的诱变育种、遗传转化、原生质体制备、细胞杂交等领域,从而改良荔枝种质资源,也对其他多年生木本植物的胚性细胞悬浮培养及植株再生体系建立具有重要参考价值。
4 结 论
本研究建立的妃子笑荔枝悬浮细胞培养体系如下:以30 g·L-1的接种量将妃子笑荔枝花药胚性愈伤组织接入MS+0.15 g·L-1肌醇+1.0 mg·L-1 2,4-D+20 g·L-1蔗糖+50 mL·L-1 椰汁的液体培养基中,在(25±2)℃、120 r·min-1的黑暗条件下振荡培养。每4 d继代1次,继代3~4次后经0.85 mm孔径的不锈钢筛网过滤,随后转至每7 d 继代1次,培养约20 d可获得状态良好的悬浮细胞,细胞悬浮液澄清透明,细胞分散性及均一性好,生长分裂速度快。本研究结果可为荔枝细胞生物学研究及生物技术育种等提供技术基础。
[1] 陈厚彬,庄丽娟,黄旭明,苏钻贤. 荔枝龙眼产业发展现状与前景[J] . 中国热带农业,2013(2):12-18.CHEN Houbin,ZHUANG Lijuan,HUANG Xuming,SU Zuanxian. Development status and prospect of litchi longan industry[J] . China Tropical Agriculture,2013(2):12-18.
[2] WANG S J,WANG G,LI H L,LI F,WANG J B. Agrobɑcterium tumefɑciens-mediated transformation of embryogenic callus and CRISPR/Cas9-mediated genome editing in ‘Feizixiao’ litchi[J] . Horticultural Plant Journal,2023,9(5):947-957.
[3] DAS D K,RAHMAN A,KUMARI D,KUMARI N. Synthetic seed preparation,germination and plantlet regeneration of litchi(Litchi chinensis Sonn.)[J] . American Journal of Plant Sciences,2016,7(10):1395-1406.
[4] QIN Y Q,ZHANG B,WANG S Q,GUO W Y,ZHANG Z K,QIN Y H,ZHAO J T,HU G B. Establishment of somatic embryogenesis regeneration system and transcriptome analysis of early somatic embryogenesis in litchi[J] . Horticultural Plant Journal,2025,11(2):535-547.
[5] HUANG M Q,GUO W Y,WU X Y,QIN Y Q,SABIR I A,ZHANG Z K,QIN Y H,HU G B,ZHAO J T. Somatic embryogenesis and plant regeneration of Litchi chinensis Sonn. cv. ‘Zili’ from immature zygotic embryos[J] . Plant Cell,Tissue and Organ Culture (PCTOC),2024,156(2):39.
[6] GOYAL S,CHATTERJEE V,KULKARNI V M,BHAT V.Plant regeneration through somatic embryogenesis in cell suspensions of Cenchrus ciliɑris L.[J] . Plant Methods,2023,19(1):110.
[7] SINGH M,ASTHANA P,RAI M K,JAISWAL U. Somatic embryogenesis and plant regeneration from suspension cultures of Sɑpindus trifoliɑtus[J] . Plant Cell,Tissue and Organ Culture(PCTOC),2024,157(2):36.
[8] VÄLIMÄKI S,HAZUBSKA-PRZYBYŁ T,RATAJCZAK E,TIKKINEN M,VARIS S,ARONEN T. Somatic embryo yield and quality from Norway spruce embryogenic tissue proliferated in suspension culture[J] . Frontiers in Plant Science,2021,12:791549.
[9] 俞长河,陈振光. 荔枝胚性悬浮培养物的建立、保持和优化原生质体分离的研究[J] . 热带作物学报,1998,19(3):16-20.YU Changhe,CHEN Zhenguang. Embryogenic suspension culture and protoplast isolation in litchee[J] . Chinese Journal of Tropical Crops,1998,19(3):16-20.
[10] 赖钟雄,黄浅,林秀莲,林玉玲,陈义挺,赖呈纯,蔡英卿. 荔枝胚性悬浮细胞系的快速建立及其体胚植株的再生[J] . 中国农学通报,2007,23(1):28-32.LAI Zhongxiong,HUANG Qian,LIN Xiulian,LIN Yuling,CHEN Yiting,LAI Chengchun,CAI Yingqing. Rapid establishment of embryogenic cell suspensions and plant regeneration via somatic embryogenesis in litchi[J] . Chinese Agricultural Science Bulletin,2007,23(1):28-32.
[11] WANG G,LI H L,WANG S J,SUN J H,ZHANG X C,WANG J B. In vitro regeneration of ‘Feizixiao’ litchi (Litchi chinensis Sonn.)[J] . African Journal of Biotechnology,2016,15(22):1026-1034.
[12] 赖钟雄,陈振光. 龙眼胚性细胞悬浮培养再生植株[J] . 应用与环境生物学报,2002,8(5):485-491.LAI Zhongxiong,CHEN Zhenguang. Plant regeneration from embryogenic cell suspensions viɑ somatic embryogenesis of Longan (Dimocɑrpus longɑn Lour.)[J] . Chinese Journal of Applied and Environmental Biology,2002,8(5):485-491.
[13] 庄梦弟,李涛,辛骞祎,周梦瑶,张海霞,马辉,钱稷,张玉星,亓宝秀,许建锋. 梨花药愈伤组织诱导和悬浮培养体系的建立及应用[J] . 果树学报,2023,40(3):577-587.ZHUANG Mengdi,LI Tao,XIN Qianyi,ZHOU Mengyao,ZHANG Haixia,MA Hui,QIAN Ji,ZHANG Yuxing,QI Baoxiu,XU Jianfeng. Establishment and application of callus induction and suspension culture system of pear anther[J] . Journal of Fruit Science,2023,40(3):577-587.
[14] 戴雪梅,华玉伟,李哲,黄天带,孙爱花,周权男,黄华孙. 植物悬浮细胞培养的关键技术及存在问题[J] . 热带生物学报,2013,4(4):381-385.DAI Xuemei,HUA Yuwei,LI Zhe,HUANG Tiandai,SUN Aihua,ZHOU Quannan,HUANG Huasun. Key technologies and their problems in plant cell suspension culture[J] . Journal of Tropical Biology,2013,4(4):381-385.
[15] 钟春水,赖钟雄,赖瑞联,陈裕坤,张梓浩,林玉玲,刘生财. 金花茶松散型愈伤组织诱导与悬浮细胞系建立[J] . 热带作物学报,2016,37(3):476-481.ZHONG Chunshui,LAI Zhongxiong,LAI Ruilian,CHEN Yukun,ZHANG Zihao,LIN Yuling,LIU Shengcai. Induction of friable callus and the establishment of suspension cell lines of Cɑmelliɑ nitidissimɑ Chi[J] . Chinese Journal of Tropical Crops,2016,37(3):476-481.
[16] 魏岳荣,黄学林,李佳,黄霞,李哲,李筱菊. 贡蕉胚性细胞悬浮系的建立和植株再生[J] . 生物工程学报,2005,21(1):58-65.WEI Yuerong,HUANG Xuelin,LI Jia,HUANG Xia,LI Zhe,LI Xiaoju. Establishment of embryogenic cell suspension culture and plant regeneration of edible banana Musɑ ɑcuminɑtɑ cv.Mas (AA)[J] . Chinese Journal of Biotechnology,2005,21(1):58-65.
[17] 林秀莲,叶玲娟,林玉玲,徐小萍,张梓浩,赖钟雄. 相思树悬浮细胞培养及其细胞形态学观察[J] . 热带作物学报,2018,39(9):1786-1793.LIN Xiulian,YE Lingjuan,LIN Yuling,XU Xiaoping,ZHANG Zihao,LAI Zhongxiong. Cell suspension culture and histological observation on some Species of Acɑciɑ spp.[J] . Chinese Journal of Tropical Crops,2018,39(9):1786-1793.
[18] 高晗,陈发菊,王毅敏,梁宏伟. 楸树胚性细胞悬浮系的建立和植株再生[J] . 基因组学与应用生物学,2018,37(2):895-899.GAO Han,CHEN Faju,WANG Yimin,LIANG Hongwei. Establishment of embryogenic cell suspension culture and plant regeneration of Cɑtɑlpɑ bungei[J] . Genomics and Applied Biology,2018,37(2):895-899.
[19] CHAKRABORTY T,CHAITANYA K V,AKHTAR N. Effects of growth regulators,organic nitrogen sources,various nutrient,and non-nutrient adjuvants on somatic embryogenesis in Red Sandalwood (Pterocɑrpus sɑntɑlinus)[J] . Journal of Plant Growth Regulation,2024,43(4):1026-1041.
[20] 耿双贵,赵星星,谭娅,吴高殷,陶光林,彭仲诚,袁杜,李秋英,王爽,刘映良. 基本培养基及碳氮源对异形玉叶金花组织培养的影响[J] . 种子,2025,44(2):236-245.GENG Shuanggui,ZHAO Xingxing,TAN Ya,WU Gaoyin,TAO Guanglin,PENG Zhongcheng,YUAN Du,LI Qiuying,WANG Shuang,LIU Yingliang. Effects of basic medium and carbon and nitrogen source on tissue culture of Mussɑendɑ ɑnomɑlɑ[J] . Seed,2025,44(2):236-245.
[21] 张东向,李康,张磊,王秀秀,张桂枝. 不同理化因子对黄芩悬浮细胞系的影响[J] . 安徽农业科学,2007,35(5):1266-1268.ZHANG Dongxiang,LI Kang,ZHANG Lei,WANG Xiuxiu,ZHANG Guizhi. Effects of different factors on suspension Scutellɑriɑ bɑicɑlensis Georgi cell[J] . Journal of Anhui Agricultural Sciences,2007,35(5):1266-1268.
[22] 潘登浪,邹积鑫,曾宪海,林位夫,CHEAN K. 油棕细胞悬浮培养及植株再生技术[J] . 广东农业科学,2019,46(2):59-65.PAN Denglang,ZOU Jixin,ZENG Xianhai,LIN Weifu,CHEAN K. Suspension culture and plant regeneration of oil palm (Elɑeis guineensis Jacq.)[J] . Guangdong Agricultural Sciences,2019,46(2):59-65.
[23] 郝艳芳,王良群,刘勇,张微,杨伟,白鸿雁,武擘. 高粱幼叶细胞悬浮系的建立[J] . 作物杂志,2018(1):35-40.HAO Yanfang,WANG Liangqun,LIU Yong,ZHANG Wei,YANG Wei,BAI Hongyan,WU Bo. Establishment of sorghum cell suspensions with young leaves[J] . Crops,2018(1):35-40.
[24] 栾林莉,宋玉凤,侯辛辛,陈健妙. 巴西橡胶树体胚胚性愈伤组织悬浮系的建立和植株再生[J] . 分子植物育种,2019,17(8):2614-2621.LUAN Linli,SONG Yufeng,HOU Xinxin,CHEN Jianmiao. Establishment of somatic embryogenic callus suspension lines in Heveɑ brɑsiliensis and plant regeneration[J] . Molecular Plant Breeding,2019,17(8):2614-2621.