阳光玫瑰葡萄(Vitis lɑbruscɑ×Vitis viniferɑ‘Shine Muscat’)作为全球鲜食葡萄产业主导品种之一,凭借其独特的玫瑰香气、脆嫩多汁的口感、优良的商品外观及耐贮运特性,在推动葡萄品种结构优化升级中占据关键地位[1]。在葡萄生殖生物学研究中,花粉生活力作为衡量花粉质量的核心指标,其高低直接决定了授粉受精效率与坐果率,并通过影响受精过程参与调控果实品质的形成[2]。尤其在杂交育种实践中,父本花粉量的精准测定、生活力的科学评估以及贮藏后活性的有效监测是保障杂交授粉成功率、缩短育种周期、提升育种效率的前提与基础[3-5]。因此,系统解析阳光玫瑰葡萄花粉生活力的动态变化规律及其调控机制,对完善杂交育种技术体系、提升果园生产效益、实现种质资源高效利用具有重要的理论价值与实践指导意义。
尽管阳光玫瑰葡萄产业发展态势迅猛,栽培面积与市场需求持续扩大,但关于其花粉生活力的系统性研究仍存在明显不足,已成为该品种种质创新、资源高效利用及育种突破的关键瓶颈[6-7]。从研究方法来看,花粉生活力测定技术虽已从传统染色法(如TTC法、I2-KI法)逐步发展为离体萌发法、荧光染色法等现代技术,但这些方法均存在局限性。离体萌发法虽能直观反映花粉的体外萌发能力,但其结果易受培养基成分(如蔗糖浓度、硼酸含量)、培养环境(温度、湿度)等多因素干扰;传统染色法则因主观性强、准确性不足,难以满足精准评估需求[8-10]。从影响因素来看,现有研究多聚焦于单一环境因子或栽培措施的简单效应分析,缺乏对多因素交互作用的系统性探究,导致难以全面揭示花粉生活力的动态变化规律,无法为生产实践提供完善的理论指导[11]。
基于上述研究背景,笔者以阳光玫瑰葡萄花粉为对象,通过系统测定花粉量、不同贮藏条件下的花粉生活力及相关生理指标(酶活性、细胞膜完整性、碳水化合物代谢),利用正交试验探究多因素互作对花粉生活力的调控机制,解析花粉生活力与生理指标的内在关联,重点优化杂交育种中的花粉采集时期、处理方法及贮藏技术体系。本研究将为优化葡萄杂交育种技术流程、提升育种效率提供关键技术支撑;同时通过阐明阳光玫瑰葡萄花粉生活力调控的生理生化机制,进一步丰富和完善葡萄生殖发育的理论体系,为推动葡萄产业种质创新突破、实现高质量可持续发展提供一定的科学依据。
1 材料和方法
1.1 材料
1.1.1 材料来源 试验材料与花粉采集均在河南科技学院葡萄种质资源圃开展,选取生长健壮、无病虫害、生长势一致的4年生阳光玫瑰葡萄植株作为试验材料。于信使花初现期,采集树冠外围光照充足部位的饱满花序,确保花粉发育进程统一。采摘后迅速将花序装入洁净自封袋,详细标注品种、采集时间、植株编号等信息,随即放入含冰袋的保温箱中低温保湿保存,快速带回实验室备用。将带回的花序平铺于无菌洁净的A4纸上,用灭菌解剖针小心剥离花药,置于25 ℃光照培养箱中自然散粉。待花药完全开裂释放花粉后,使用灭菌药匙收集纯净花粉,分装至无菌离心管中,密封管口并再次标记相关信息,置于低温环境中暂存,以备后续试验使用。整个操作过程须严格避免花粉遭受机械损伤与污染。
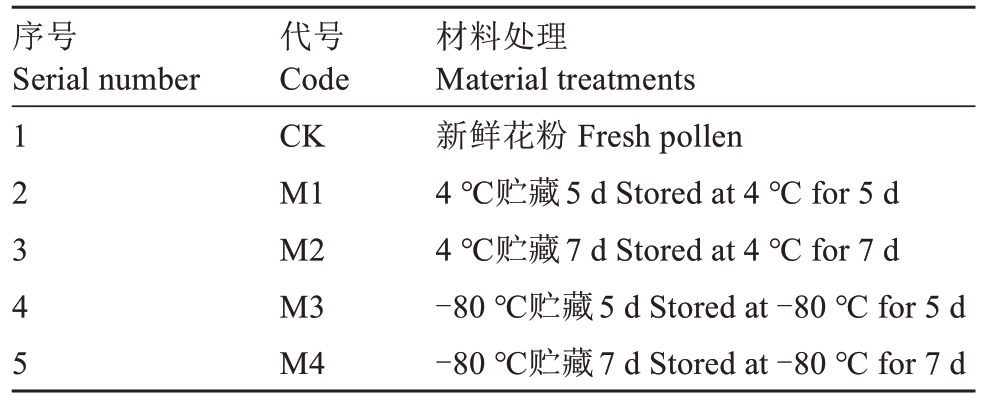
1.1.2 材料处理 基于前期研究[12-13]与相关文献[11,14],试验设置了4 ℃和-80 ℃两个贮藏温度,每个温度下设置了5 d和7 d两个贮藏时长,共4个处理。每个处理设置3次生物学重复,并在贮藏期间严格监控以确保温度稳定(表1)。
表1 材料处理
Table 1 Material treatments
序号Serial number 1 2 3 4 5代号Code CK M1 M2 M3 M4材料处理Material treatments新鲜花粉 Fresh pollen 4 ℃贮藏5 d Stored at 4 ℃ for 5 d 4 ℃贮藏7 d Stored at 4 ℃ for 7 d-80 ℃贮藏5 d Stored at -80 ℃ for 5 d-80 ℃贮藏7 d Stored at -80 ℃ for 7 d
1.2 方法
1.2.1 花粉量测定 采用血球计数板法测定花粉量。取盛花期前1 d的花序,随机选取30枚花药,经50 ℃烘干至开裂散粉;随后加入20%六偏磷酸钠溶液定容至6 mL,并振荡制成悬浮液;吸取2 μL悬浮液滴加至血球计数板,在光学显微镜(10×40倍,重庆澳浦光电UB103i型)下观察。每个样品设置3次重复,参考公式计算花粉量并取其平均值[15],花粉量=(80小格内的花粉数/80)×400×10000×600。
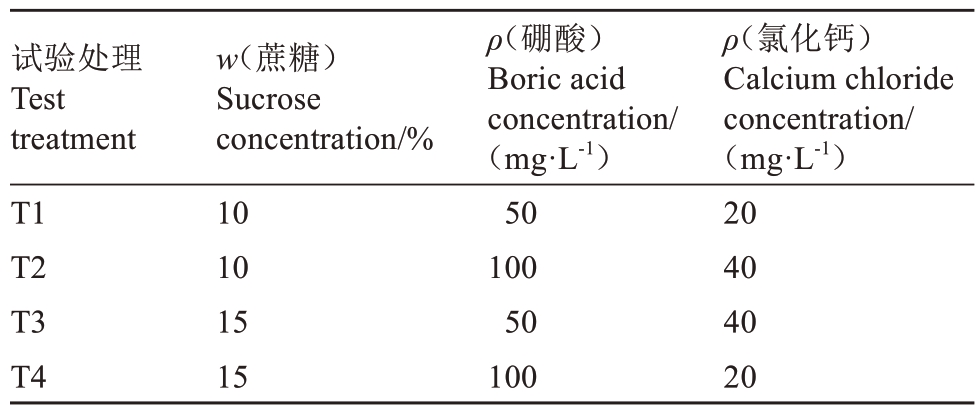
1.2.2 正交试验设计优化葡萄花粉离体萌发培养基及花粉生活力测定 基于前期研究[12-13,16]与相关文献[17-18],选取蔗糖浓度、硼酸浓度和氯化钙浓度这3个对葡萄花粉生活力影响较大的因素,每个因素设置2个浓度(ρ,后同):蔗糖浓度[10%(100 g·L-1),15%(150 g·L-1)] 、硼酸浓度(50 mg·L-1,100 mg·L-1)、氯化钙浓度(20 mg·L-1,40 mg·L-1)。采用L4(23)正交表设计试验,共包含4种培养基,依据正交设计表(表2)配制培养基。以T1培养基为例:将7 g·L-1琼脂粉加热溶解,依次加入10%蔗糖、50 mg·L-1硼酸、20 mg·L-1氯化钙,定容后调节pH至6.0,经灭菌后分装至培养皿,制成花粉离体发芽床。贮藏至5 d和7 d时,取出花粉于室温下平衡30~60 min,随后过筛并均匀接种于培养基,于25 ℃、相对湿度60%~70%条件下培养。每隔1 h在光学显微镜(10×40倍)下观察,以花粉管长度超过花粉直径为萌发标准。每个培养皿随机选取3个视野,按“计上不计下,计左不计右”的原则计数,花粉萌发率/%=(萌发花粉数/花粉总数)×100。
表2 发芽床正交设计表
Table 2 Orthogonal design table for germination test
试验处理Test treatment T1 T2 T3 T4 w(蔗糖)Sucrose concentration/%10 10 15 15 ρ(硼酸)Boric acid concentration/(mg·L-1)50 100 50 100 ρ(氯化钙)Calcium chloride concentration/(mg·L-1)20 40 40 20
1.2.3 荧光染色法评估花粉生活力 将荧光素二乙酸酯(fluorescein diacetate,FDA)粉末溶解于丙酮溶剂中,配制浓度为2 mg·mL-1的母液。将母液转移至棕色离心管,-20 ℃避光保存,避免光照及温度影响导致试剂降解。使用前,吸取10 μL FDA母液,加入1 mL 10%蔗糖溶液,轻轻混匀,配制成终浓度为0.02 mg·mL-1的工作液。工作液需现配现用(建议30 min内使用完毕),全程严格避光保存,以防荧光淬灭。称取约1 mg花粉转移至洁净离心管,加入1000 μL工作液,轻微晃动离心管使花粉与染色液充分接触,于避光环境中染色10 min。染色结束后,吸取20 μL染色花粉悬液滴加至洁净载玻片,缓慢加盖盖玻片(避免产生气泡影响观察),立即将载玻片置于20×荧光显微镜(Olympus BX53)下观察,采集并记录荧光图像。FDA通过活细胞酯酶分解产生荧光,其中显示荧光的花粉为有活力花粉,使用ImageJ软件统计有活力花粉及花粉总数,参考公式计算活力花粉百分比,活力花粉百分比/%=(显示荧光花粉数/花粉总数)×100[19-20]。
1.2.4 不同贮藏条件下花粉生理指标测定 可溶性糖(SS)含量采用蒽酮比色法[21]测定;可溶性蛋白(SP)含量采用马斯亮蓝G-250法[22]测定。游离脯氨酸(Pro)含量采用茚三酮比色法[21]测定;超氧化物歧化酶(SOD)活性采用SOD抑制氮蓝四唑(NBT)光化还原法[23]测定;过氧化物酶(POD)活性采用愈创木酚法[24]测定;过氧化氢酶(CAT)活性采用高锰酸钾滴定法[25]测定。
1.3 数据处理与分析
采用Excel 2010软件处理数据,结果以平均值±标准差表示;采用SPSS 22.0、GraphPad Prism 10.1.2和ImageJ软件进行统计分析与作图,通过单因素方差分析(One-way ANOVA)结合Duncan多重比较法进行显著性分析(P<0.05);采用Pearson相关系数法分析各指标间的相关性。
2 结果与分析
2.1 阳光玫瑰葡萄单植株内及植株间花粉量的稳定性与差异性分析
由图1可知,阳光玫瑰葡萄单株内花粉量稳定性较高。植株1的3次重复测定值均为24.00×104粒·花药-1,标准差为0,表明同一植株不同花序间花粉量受内部因素影响小、重复性良好;但不同植株间花粉量存在显著差异,植株1平均花粉量(24.00×104 粒·花药-1)显著高于植株2(18.67×104 粒·花药-1)和植株3(17.33×104 粒·花药-1),增幅分别为28.55%和38.49%,推测该差异可能与植株间养分积累、光照条件或遗传特性有关。该结果对杂交育种具有指导意义,应优先选择花粉量高的植株作为父本,通过优化栽培管理措施进一步提升花粉量。
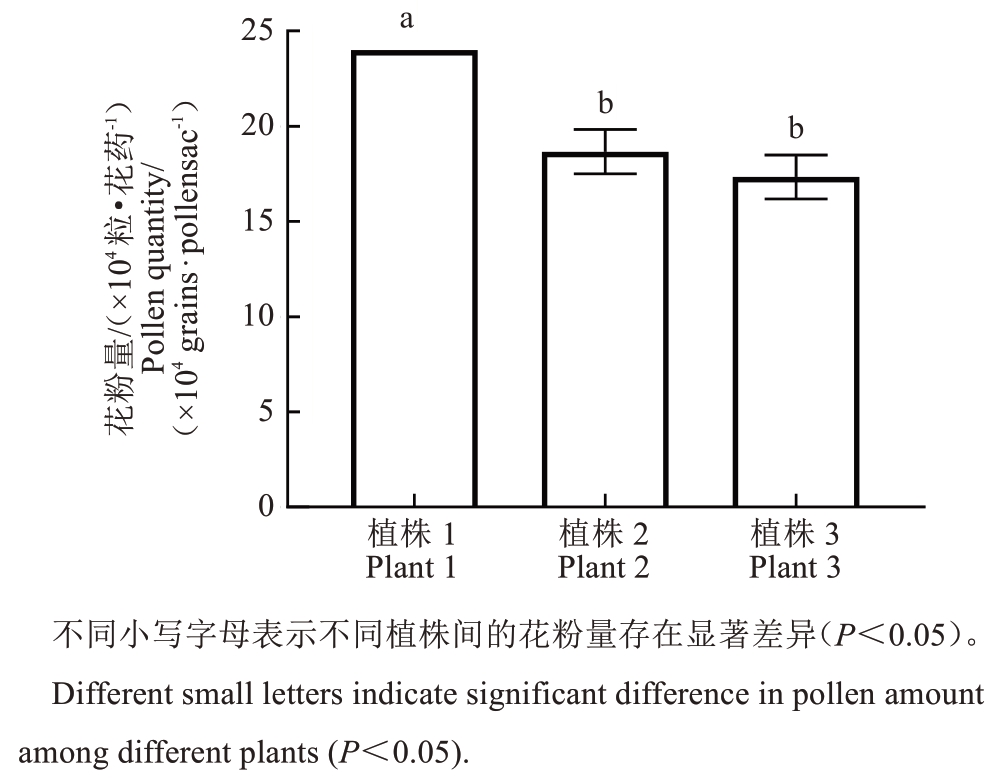
图1 阳光玫瑰葡萄单株内及株间花粉量比较
Fig. 1 Comparison of pollen quantity within and among individual Shine Muscat grape plants
2.2 不同贮藏条件和培养基处理对阳光玫瑰葡萄花粉萌发率的影响及荧光染色验证
由图2可以看出,经4 ℃(M1、M2)与-80 ℃(M3、M4)贮藏后,相同贮藏条件下不同培养基间的花粉萌发率差异显著(P<0.05),且培养基配方效应随贮藏胁迫强度的增加而愈发明显。其中,T4培养基(15%蔗糖+100 mg·L-1硼酸+20 mg·L-1氯化钙)在各贮藏处理组中均维持最高萌发率,其与T1培养基(10%蔗糖+50 mg·L-1硼酸+20 mg·L-1氯化钙)的萌发率差值由M1组的约2个百分点扩大至M4组的约6个百分点。这表明,高浓度蔗糖与硼酸的协同作用是维持贮藏花粉萌发活力的关键,而20 mg·L-1氯化钙可为花粉萌发提供适宜的萌发环境。综上所述,培养基对花粉萌发的调控效应具有贮藏条件依赖性;T4培养基通过优化碳源供给与硼素调控,可在低温胁迫下更有效地补偿内源物质损耗、维持花粉萌发相关代谢过程,有助于优化阳光玫瑰葡萄贮藏花粉的离体萌发体系。
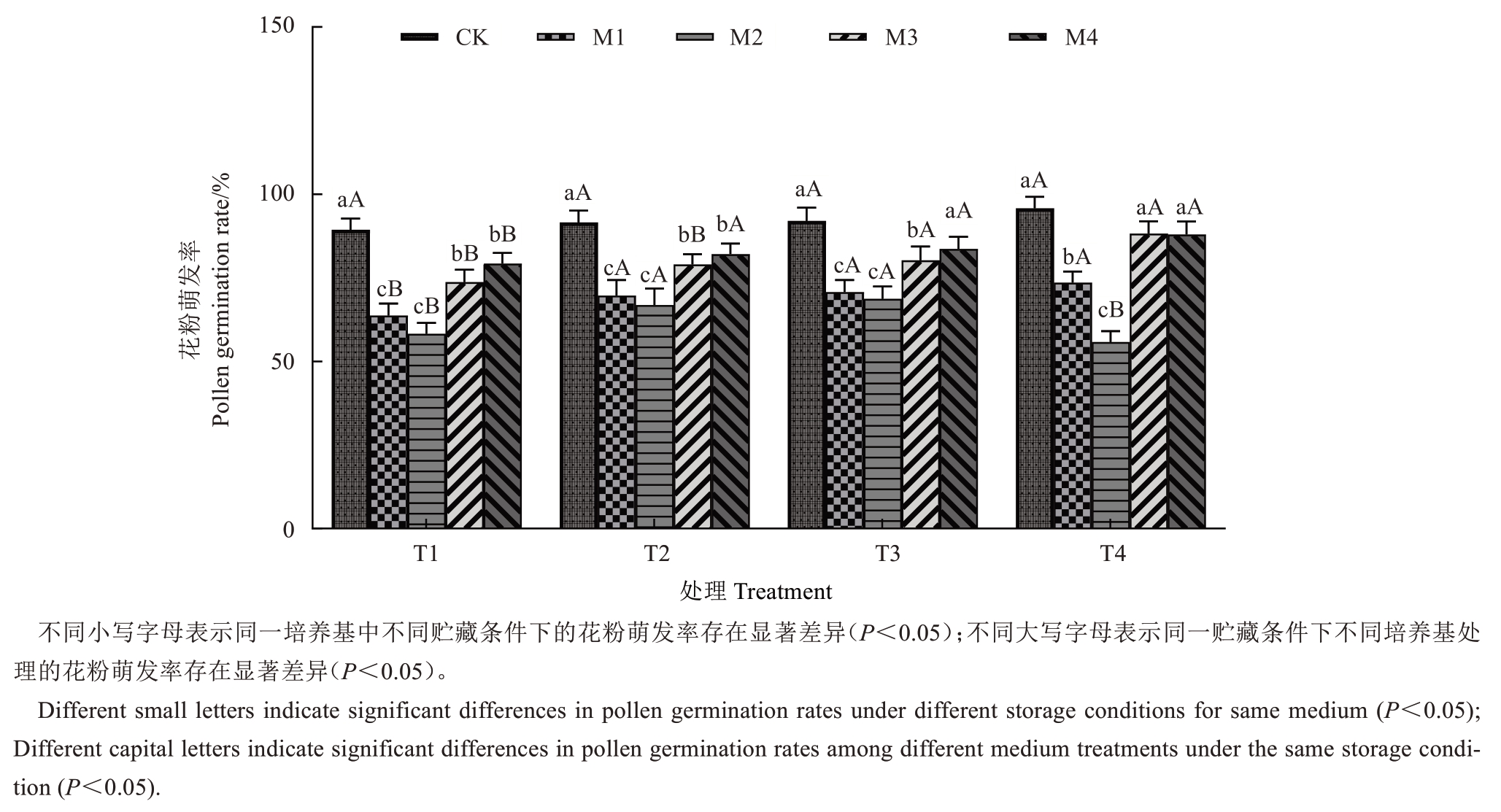
图2 不同贮藏条件和培养基处理对阳光玫瑰葡萄花粉萌发率的影响
Fig. 2 Effects of different storage conditions and medium treatments on pollen germination rate in Shine Muscat grape
贮藏条件对花粉萌发率影响显著。相同贮藏时间下,-80 ℃超低温贮藏的花粉萌发率显著高于4 ℃:贮藏5 d时,4 ℃处理的花粉萌发率为63.67%(T1)~73.54%(T4),-80 ℃处理为73.73%(T1)~88.26%(T4),后者较前者平均提高15%~20%,其中T4培养基上增幅最显著,-80 ℃处理较4 ℃处理显著提高14.72百分点;贮藏7 d时,4 ℃处理的萌发率降至55.75%(T4)~68.75%(T3),而-80 ℃处理仍保持79.23%(T1)~87.98%(T4)的高萌发率,T4培养基上-80 ℃贮藏7 d的萌发率较4 ℃处理显著提高32.23百分点,差异最为显著;此外,随贮藏时间延长,4 ℃下T1~T4培养基的花粉萌发率分别下降5.44、2.81、1.98、17.79个百分点,而-80 ℃下T1~T3培养基萌发率分别上升5.50、3.09、3.43个百分点,可见两种温度下花粉萌发率整体呈下降趋势,但4 ℃下降幅度更大,表明超低温贮藏可有效延缓花粉活力的衰退,且贮藏时间越长,活力保持效果越好。
FDA荧光染色结果进一步验证了不同贮藏条件和培养基处理下的花粉萌发率差异(图3)。新鲜花粉(CK)中,呈现强绿色荧光的有活力花粉占比最高,且荧光强度最为明显;-80 ℃超低温贮藏(M3、M4)的花粉中,有活力花粉数量显著多于4 ℃贮藏(M1、M2)处理;而4 ℃贮藏7 d(M2)的花粉中,弱荧光或无荧光的无活力花粉占比最高。定量统计结果显示(图3-F),不同贮藏条件下的花粉生活力百分比存在显著差异,具体顺序为CK>M3(-80 ℃贮藏5 d)>M4(-80 ℃贮藏7 d)>M1(4 ℃贮藏5 d)>M2(4 ℃贮藏7 d),与花粉萌发率的测定结果高度一致,证实了FDA荧光染色法用于评估阳光玫瑰葡萄花粉生活力的可靠性,更进一步明确了-80 ℃超低温贮藏能更有效地维持花粉生活力,同时结合正交试验数据可知,T4培养基是促进花粉萌发的最优选择。

图3 不同贮藏条件下阳光玫瑰葡萄花粉的FDA荧光染色及活力测定
Fig. 3 FDA fluorescent staining and viability determinations of Shine Muscat grape pollen under different storage conditions
2.3 不同贮藏条件下阳光玫瑰葡萄花粉生理指标的动态变化及其与活力的关联性分析
2.3.1 不同贮藏条件下花粉中可溶性糖、可溶性蛋白及脯氨酸含量的动态变化 由图4-A可知,新鲜花粉(CK)的可溶性糖含量最高。在贮藏过程中,不同条件下可溶性糖含量变化显著。M1时可溶性糖含量降至新鲜花粉的9.32%;M2时进一步降至8.81%;而M3时含量占比为13.35%,M4时降至12.98%,这表明作为花粉萌发的关键能量底物,可溶性糖含量随贮藏时间的延长而降解,且降解速率与贮藏温度紧密相关。超低温环境能有效抑制花粉代谢,显著延缓可溶性糖含量减少。由图4-B可知,可溶性蛋白含量的变化趋势与可溶性糖一致。在贮藏过程中,M1时可溶性蛋白含量为新鲜花粉的82.66%,M2时降至66.63%;而M3时含量占比83.45%,M4时降至71.50%,这表明超低温环境能稳定地抑制蛋白质降解。蛋白质在花粉中作为酶功能载体与细胞结构物质的关键角色,其在-80 ℃贮藏下具有较高的保留量,是该贮藏条件下花粉生活力更优的重要物质基础。由图4-C可知,脯氨酸作为关键的渗透调节物质,在贮藏初期(5 d),不同温度下脯氨酸含量差异显著,M1时脯氨酸含量为新鲜花粉的21.94%;M3时仅为15.34%;当贮藏时间延长至7 d时,M2时脯氨酸含量占比为21.38%,M4时则降至6.50%,脯氨酸含量差异随贮藏时间推移逐步增大。推测在长期贮藏中,脯氨酸作为优先消耗的应激保护物质,其降解速率会随时间推移渐趋一致。
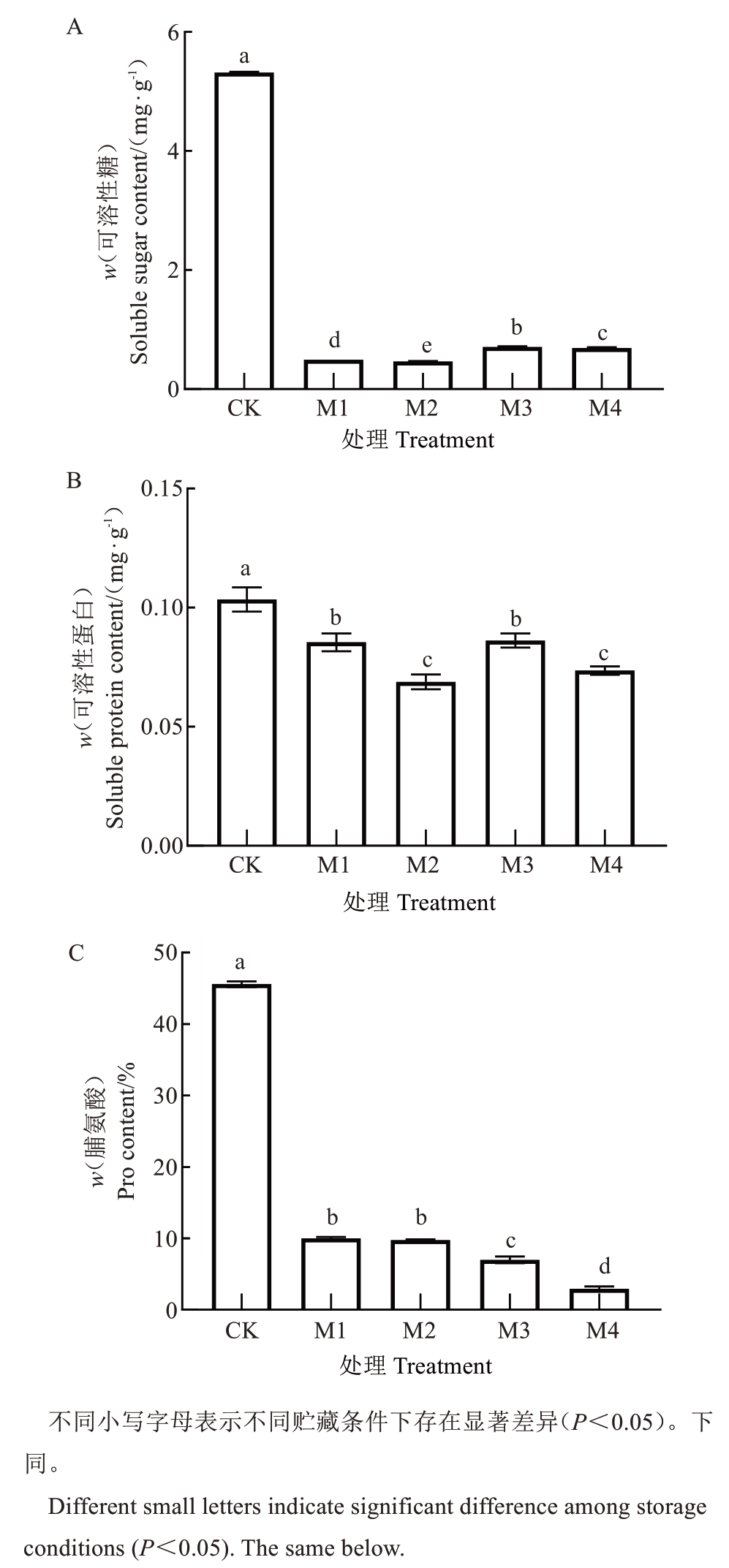
图4 不同贮藏条件下阳光玫瑰葡萄花粉中可溶性糖(A)、可溶性蛋白(B)和脯氨酸(C)含量的变化
Fig. 4 Changes of soluble sugar(A), soluble protein(B) and proline(C) content in Shine Muscat grape pollen under different storage conditions
综上所述,可溶性糖、可溶性蛋白和脯氨酸的含量变化,与花粉生活力的变化趋势高度一致。新鲜花粉因可溶性糖(提供能量)、可溶性蛋白(维持结构与功能)及脯氨酸(增强抗逆性)含量较高而表现出最强活力;-80 ℃贮藏条件能显著延缓可溶性糖和可溶性蛋白这两种物质的降解,尤其在贮藏前中期,这为花粉生活力的维持奠定了坚实的物质基础,这也解释了超低温贮藏的花粉萌发率为何始终高于4 ℃贮藏的花粉。该结果从物质代谢与抗逆储备角度,揭示了不同贮藏条件下调控花粉生活力的机制,为优化花粉保存技术提供了“维持物质含量→稳固代谢基础→延缓活力衰退”的理论依据与实践路径,建议长期贮藏优先采用-80 ℃超低温,以更有效地减少可溶性糖、可溶性蛋白及脯氨酸的降解。
2.3.2 不同贮藏条件下花粉中抗氧化酶活性的动态变化 超氧化物歧化酶(SOD)、过氧化物酶(POD)和过氧化氢酶(CAT)作为花粉抗氧化系统的核心酶类,其活性在不同贮藏条件下的动态变化与花粉生活力的维持密切相关。由图5-A可知,在4 ℃贮藏下,SOD活性在M1时升至新鲜花粉的111.28%,可能与短期低温应激诱导酶活性升高有关,但贮藏至7 d(M2)时,活性降至42.27%,降幅达58.73%。相比之下,-80 ℃超低温贮藏对SOD活性的保护作用更为显著,其活性在M3(144.14%)和M4(46.16%)时均高于4 ℃同期,这表明作为清除超氧阴离子的关键酶,SOD活性在长期贮藏中更易受4 ℃低温的破坏,而-80 ℃通过抑制酶结构失活,延缓活性衰减,为花粉提供更持久的抗氧化保护。由图5-B可知,在贮藏过程中POD活性的变化趋势与SOD类似,但波动幅度较小。在4 ℃贮藏下,POD活性在M1时升至新鲜花粉的120.01%,贮藏至7 d(M2)时,活性回落至100%;-80 ℃超低温贮藏下,POD活性的提升更为显著,其活性在M3(139.99%)和M4(120.01%)时均高于4 ℃同期。POD通过催化过氧化物分解参与抗氧化防御,其在-80 ℃超低温条件下的高活性水平,表明-80 ℃超低温能更有效地维持花粉的氧化损伤修复能力,这与花粉生活力的保持趋势一致。由图5-C可知,在贮藏过程中,CAT活性呈持续上升趋势,且-80 ℃贮藏下的升幅大于4 ℃贮藏。在4 ℃贮藏下,CAT活性在M1时升至新鲜花粉的110.79%,贮藏至7 d(M2)时,活性进一步升至162.23%。-80 ℃贮藏下,CAT活性的提升更为突出,其活性在M3(142.26%)和M4(174.15%)时均高于4 ℃同期,并在M4时达到所有处理中的最高值。作为清除过氧化氢的关键酶,CAT活性在-80 ℃超低温贮藏下更易被诱导升高,这可能与超低温抑制了过氧化氢的过度积累有关,进而减轻了对花粉细胞的氧化损伤。
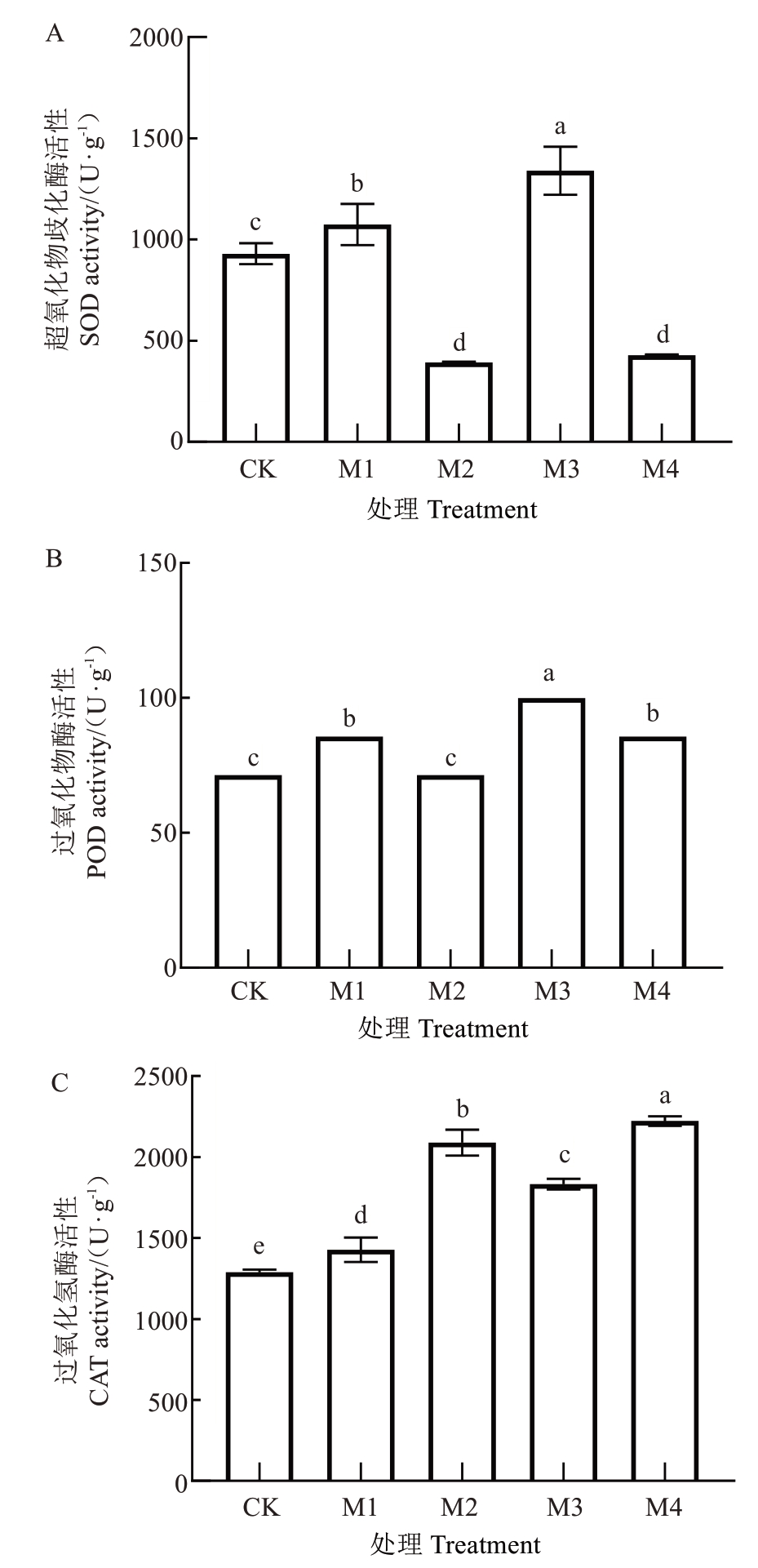
图5 不同贮藏条件下阳光玫瑰葡萄花粉中SOD(A)、POD(B)和CAT(C)活性的变化
Fig. 5 Changes of SOD(A), POD(B) and CAT(C) activities in Shine Muscat grape pollen under different storage conditions
综上所述,抗氧化酶系统(SOD、POD、CAT)通过清除活性氧(ROS)维持细胞内氧化还原平衡,其活性水平直接反映了花粉的抗逆能力。新鲜花粉的高酶活性与其最高萌发率表现一致,表明强抗氧化能力是维持花粉生活力的重要物质基础。在贮藏过程中,酶活性的下降伴随着花粉萌发率的降低,进一步证实了氧化应激是花粉生活力衰退的关键机制。-80 ℃超低温通过抑制代谢与氧化应激,能显著延缓SOD、POD、CAT活性的下降,其效果优于4 ℃贮藏。该结果从抗氧化防御角度,揭示了不同贮藏条件调控花粉生活力的机制,为优化花粉保存技术提供了“维持酶活性→增强抗逆性→延长活力”的理论依据与实际路径,建议长期贮藏优先采用-80 ℃超低温,以更好保留抗氧化酶功能。
2.3.3 生理指标与花粉萌发率的关联性分析 由表3可知,可溶性糖、可溶性蛋白、脯氨酸含量及抗氧化酶(SOD、POD、CAT)活性与花粉萌发率均呈极显著正相关(P<0.001),相关系数介于0.856~0.915之间,其中SOD活性与萌发率的相关性最高(r=0.915),可溶性蛋白含量与萌发率的相关性最低(r=0.856),表明上述生理指标均是影响花粉生活力的关键因子。可溶性糖作为能量代谢底物,为花粉萌发提供能量;可溶性蛋白的稳定性可通过维持酶的活性与细胞结构的完整性,进而影响花粉萌发率;脯氨酸作为渗透调节物质,其含量高低决定了花粉抵御低温胁迫的能力;抗氧化酶活性反映了花粉的抗逆能力。各项指标间存在协同作用:可溶性糖为酶促反应提供能量底物,可溶性蛋白可作为酶的功能载体,脯氨酸为酶促反应提供稳定环境,而抗氧化酶通过清除活性氧(ROS)保护前两者免受氧化损伤,这共同构成了花粉生活力的协同调控网络。-80 ℃超低温贮藏通过抑制代谢实现对上述指标的综合保护,为花粉生活力的评估和贮藏条件的优化提供了科学依据。
表3 阳光玫瑰葡萄花粉生理指标与花粉萌发率的相关性分析
Table 3 Correlation analysis between pollen physiological indices and pollen germination rate in Shine Muscat grape
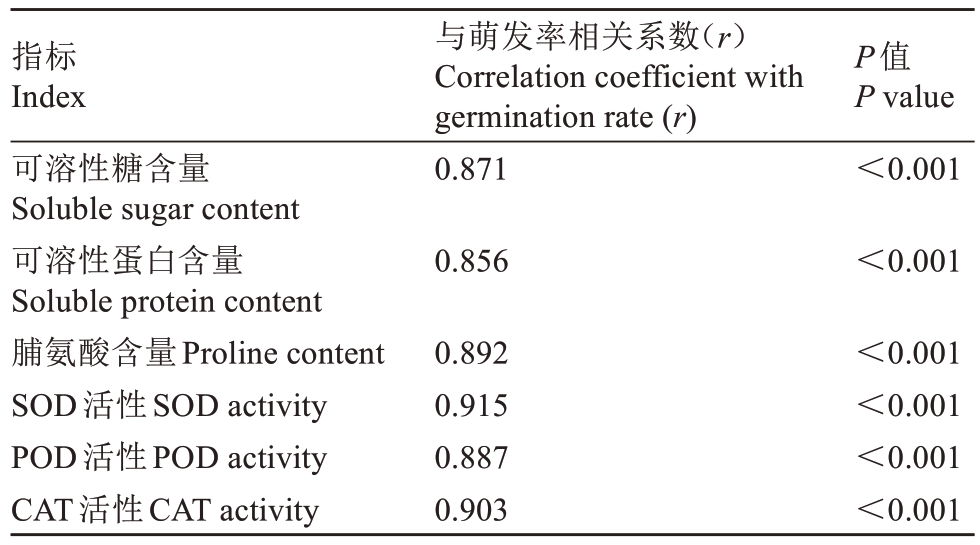
注:相关系数(r)表示各生理指标(可溶性糖、可溶性蛋白、脯氨酸含量及SOD、POD、CAT活性)与花粉萌发率的相关程度,P值表示相关性的显著水平,其中P<0.001表明各指标与花粉萌发率呈极显著正相关。
Note:The correlation coefficient (r) in the table indicates the degree of correlation between each physiological index (soluble sugar, soluble protein, proline content, and activities of SOD, POD, and CAT) and pollen germination rate. P represents the significance level of the correlation, and P<0.001 indicates an extremely significant correlation.
指标Index可溶性糖含量Soluble sugar content可溶性蛋白含量Soluble protein content脯氨酸含量Proline content SOD活性SOD activity POD活性POD activity CAT活性CAT activity与萌发率相关系数(r)Correlation coefficient with germination rate (r)0.871 P值P value<0.001 0.856<0.001<0.001<0.001<0.001<0.001 0.892 0.915 0.887 0.903
3 讨 论
3.1 关于花粉量影响因素的相关研究
本研究发现阳光玫瑰葡萄不同植株间花粉量差异显著,植株1的花粉量(24×104粒·花药-1)较植株2、3分别高出28.55%和38.49%,表明花粉量的差异可能与植株养分积累、冠层光照等因素相关,这一结果与Rane等[11]在葡萄属(Vitis spp.)基因型研究中的结论一致,发现不同葡萄品种花粉量存在显著基因型差异,且养分供应和冠层微环境(如光照强度)是关键影响因子。此外,Bayo等[15]在香蕉(Musɑ ɑcuminɑtɑ)研究中证实,同一物种不同基因型的花粉量差异可达30%~40%,与本研究中阳光玫瑰葡萄植株间的差异幅度(28.55%~38.49%)相近,表明花粉量的基因型分化是植物生殖特性的普遍现象。这些研究多关注于品种间的差异[11,15],本试验则补充了单一品种内植株间花粉量的差异研究,丰富了葡萄生殖生物学的研究维度。结合Baby等[26]提出的葡萄品种间坐果率差异与花粉量及活力直接相关的结论,进一步明确了本研究中选择高花粉量植株作为父本的实践意义,不仅能提高杂交授粉效率,还能为提升后代坐果率奠定基础,这一发现丰富了葡萄生殖生物学中花粉量与繁殖能力关联的研究。
3.2 关于培养基组分对花粉生活力影响的研究
本研究通过正交试验筛选发现,T4培养基(15%蔗糖+100 mg·L-1硼酸+20 mg·L-1氯化钙)对阳光玫瑰葡萄的花粉萌发具有最优调控效果,其新鲜花粉萌发率高达95.79%。这一结果证实,高浓度蔗糖与硼酸的协同作用是激活并维持花粉高活力的核心因素,该结论与多数葡萄品种及落叶果树花粉离体萌发的生理机制研究结果相吻合,即充足的碳源供给与适宜的硼素水平是保障花粉管极性生长的基础。李桂荣等[12]在火焰无核葡萄中报道,含10%蔗糖+50 mg·L-1硼酸的培养基可获得较高的花粉萌发率(78.3%),而本研究在阳光玫瑰葡萄中确定影响花粉生活力的最优蔗糖(15%)和硼酸(100 mg·L-1)浓度均高于该结果;Kelen等[17]的研究同样表明,蔗糖(10%~15%)和硼酸(50~100 mg·L-1)是葡萄花粉萌发的关键因子,但品种间最适浓度存在差异。同时,本研究首次在阳光玫瑰葡萄中明确氯化钙(20 mg·L-1)对花粉生活力具有一定的辅助作用,这与辛董董等[16]提出的“氯化钙对部分葡萄品种花粉萌发影响较弱”的研究结果形成对比,这也为针对性优化阳光玫瑰葡萄花粉生活力的培养基配方提供了新依据[27]。本研究优化的T4培养基既能提升花粉生活力评估效率,也为后续大规模杂交育种中花粉质量的快速筛选提供了技术支撑。
3.3 关于贮藏条件对花粉生活力及生理指标影响的研究
本研究证实-80 ℃超低温贮藏对阳光玫瑰葡萄花粉生活力的保持效果显著优于4 ℃,且花粉生活力与可溶性糖、可溶性蛋白、脯氨酸含量及SOD、POD、CAT活性呈极显著正相关。张少伟等[13]在无核葡萄研究中发现,-80 ℃贮藏7 d后花粉萌发率较4 ℃提高20%~30%,而本研究中阳光玫瑰葡萄在-80 ℃贮藏7 d后的萌发率增幅更显著,表明-80 ℃超低温贮藏对阳光玫瑰葡萄花粉的保护作用更突出。Du等[14]研究指出,超低温贮藏通过抑制代谢延缓芍药(Pɑeoniɑ spp.)花粉生活力的衰退,本研究进一步揭示了其生理机制:-80 ℃贮藏通过延缓可溶性糖(能量底物)、可溶性蛋白(结构与酶载体)和脯氨酸(渗透保护剂)的降解,并维持抗氧化酶活性,从而延缓花粉活力的衰退。这与Ren等[28]在芍药中研究表明超低温减少物质消耗、Dolce等[29]在兰花(Cohniellɑ cepulɑ)中研究表明-80 ℃贮藏60 d的花粉受精能力仍保持初始值70%以上的结论一致,表明超低温贮藏对花粉的繁殖功能具有普遍保护作用。
与戚行江等[30]在杨梅中仅定性描述生理指标与活力正相关不同,本研究建立的“花粉生活力-生理指标”定量关联模型(r=0.856~0.915),为葡萄花粉生活力的预测提供了量化依据。David等[31]提出“脯氨酸优先参与葡萄花粉的渗透调节”,与本研究中脯氨酸在贮藏初期(5 d)下降更快的结果相吻合;而Ban等[32]在葡萄种间杂交(Vitis lɑbruscɑnɑ × Vitis viniferɑ)中发现,父本花粉生活力是影响杂交后代结实率的关键性状,表明本研究中贮藏条件的优化对提升种间杂交成功率具有潜在价值。此外,本研究发现,脯氨酸含量在贮藏初期下降更快,而可溶性蛋白含量则在整个贮藏期保持稳定,这与David等[31]在葡萄中关于“脯氨酸优先参与渗透调节”的结论一致,进一步验证了葡萄花粉贮藏的代谢特性。
综上,本研究在前人关于花粉量基因型差异、培养基组分调控作用、超低温贮藏优势等核心结论的基础上,聚焦阳光玫瑰葡萄品种的特性,优化了技术参数,并通过关联分析,深化了其生理机制解析。相较于单纯的分子机制研究,本研究建立的“花粉生活力-生理指标”关联模型可直接指导杂交育种中的技术操作(如父本选择、花粉贮藏时长确定等),具有更强的田间应用价值,为阳光玫瑰葡萄杂交育种提供了更具实践意义的理论与技术支撑。
4 结 论
本研究优化了花粉采集、保存及授粉的技术体系,建立了“花粉生活力-生理指标”关联模型,初步解决了引言中提出的“多因素交互作用机制不明”“快速检测技术不完善”等问题。首次针对阳光玫瑰葡萄构建了花粉生活力与生理指标的定量关联模型,实现了对花粉生活力的精准评估与调控。研究结果为葡萄杂交育种中父本选择、花粉贮藏策略制定及授粉效率提升提供了理论依据,同时为应对气候变化导致的授粉难题提供了解决方案,对完善葡萄杂交授粉理论、推动产业提质增效具有重要实践意义。未来研究需进一步验证该模型在田间应用中的效果,以提高其实用性。
[1] 邢志淦,雷向朝,王浩臣,冯铭鑫,李靖雯,刘羽佳,房玉林,孟江飞. 不同砧木‘阳光玫瑰’葡萄幼树对盐与低温复合胁迫的生理响应[J] . 园艺学报,2025,52(3):693-704.XING Zhigan,LEI Xiangzhao,WANG Haochen,FENG Mingxin,LI Jingwen,LIU Yujia,FANG Yulin,MENG Jiangfei. Physiological response of Shine Muscat grape seedlings grafted with different rootstocks to combined stress of salt and low temperature[J] . Acta Horticulturae Sinica,2025,52(3):693-704.
[2] SABIR A. Xeniɑ and metaxenia in grapes:Differences in berry and seed characteristics of maternal grape cv. ‘Narince’ (Vitis viniferɑ L.) as influenced by different pollen sources[J] . Plant Biology,2015,17(2):567-573.
[3] ATAK A,ŞEN A. A grape breeding programme using different Vitis species[J] . Plant Breeding,2021,140(6):1136-1149.
[4] WANG Z L,HUI M,SHI X Q,WU D,WANG Y,HAN X,CAO X,YAO F,LI H,WANG H. Characteristics of the seed germination and seedlings of six grape varieties (Vitis viniferɑ)[J] .Plants,2022,11(4):479.
[5] LIU Z J,WANG N,SU Y,LONG Q M,PENG Y L,SHANGGUAN L F,ZHANG F,CAO S,WANG X,GE M Q,XUE H,MA Z Y,LIU W W,XU X D,LI C C,CAO X J,AHMAD B,SU X N,LIU Y T,HUANG G Z,DU M R,LIU Z Y,GAN Y,SUN L,FAN X C,ZHANG C,ZHONG H X,LENG X P,REN Y H,DONG T Y,PEI D,WU X Y,JIN Z X,WANG Y W,LIU C H,CHEN J F,GAUT B,HUANG S W,FANG J G,XIAO H,ZHOU Y F. Grapevine pangenome facilitates trait genetics and genomic breeding[J] . Nature Genetics,2024,56(12):2804-2814.
[6] WANG Z L,XUE T T,GAO F F,ZHANG L,HAN X,WANG Y,HUI M,WU D,LI H,WANG H. Intraspecific recurrent selection in V. viniferɑ:An effective method for breeding of high quality,disease-,cold-,and drought-resistant grapes[J] . Euphytica,2021,217(6):111.
[7] PUGLISI D,LAS CASAS G,FERLITO F,NICOLOSI E,DI GUARDO M,SCOLLO F,SAITTA G,LA MALFA S,GENTILE A,DISTEFANO G. Parents’ selection affects embryo rescue,seed regeneration and the heredity of seedless trait in table grape breeding programs[J] . Agriculture,2022,12(8):1096.
[8] 姜雪婷,杜玉虎,张绍铃,吴俊. 梨43个品种花粉生活力及4种测定方法的比较[J] . 果树学报,2006,23(2):178-181.JIANG Xueting,DU Yuhu,ZHANG Shaoling,WU Jun. Pollen viability of 43 pear cultivars and comparison of testing methods[J] .Journal of Fruit Science,2006,23(2):178-181.
[9] DAVARYNEJA G H,SZABO Z,NYEKI J,SZABO T. Phenological stages,pollen production level,pollen viability and in vitro germination capability of some sour cherry cultivars[J] .Asian Journal of Plant Sciences,2008,7(7):672-676.
[10] LUO S,ZHANG K,ZHONG W P,CHEN P,FAN X M,YUAN D Y. Optimization of in vitro pollen germination and pollen viability tests for Cɑstɑneɑ mollissimɑ and Cɑstɑneɑ henryi[J] . Scientia Horticulturae,2020,271:109481.
[11] RANE P,THAKRE M,VERMA M K,KUMAR C,PRAKASH J,SRIVASTAVA V,SHASHANK P R,MURUKAN N,CHAWLA G,MANDAL P K,KUMAR H,JADHAV A K,VARGHESE E,PATEL V B,SINGH S K. Studies on pollen micro-morphology,pollen storage methods,and cross-compatibility among grape (Vitis spp.) genotypes[J] . Frontiers in Plant Science,2024,15:1353808.
[12] 李桂荣,朱自果,李力,蔡祖国. 火焰无核葡萄花粉离体萌发试验[J] . 西北林学院学报,2012,27(6):93-97.LI Guirong,ZHU Ziguo,LI Li,CAI Zuguo. Studies on pollen germination of Vitis viniferɑ cv. Flame Seedless in vitro[J] . Journal of Northwest Forestry University,2012,27(6):93-97.
[13] 张少伟,李桂荣,朱自果,孙振元. 不同无核葡萄品种花粉贮藏及其生活力的测定[J] . 东北林业大学学报,2017,45(9):49-53.ZHANG Shaowei,LI Guirong,ZHU Ziguo,SUN Zhenyuan.Pollen storage condition and viability of different seedless grape cultivars[J] . Journal of Northeast Forestry University,2017,45(9):49-53.
[14] DU G C,XU J G,GAO C R,LU J,LI Q,DU J,LÜ M W,SUN X.Effect of low storage temperature on pollen viability of fifteen herbaceous peonies[J] . Biotechnology Reports,2019,21:e00309.
[15] BAYO S J,MASSAWE V,NDAKIDEMI P A,VENKATARAMANA P,MLAKI A,MDUMA H,JOMANGA K,SWENNEN R,BROWN A. Pollen amount and viability in mchare and selected wild (AA) banana (Musɑ ɑcuminɑtɑ) genotypes:Prospects for breeding[J] . HortScience,2024,59(5):632-638.
[16] 辛董董,朱自果,候行行,连艳会,闫丹丹,张洋,李桂荣. 不同葡萄品种花粉生活力、花粉量及柱头可授性的测定[J] . 江苏农业科学,2019,47(4):113-116.XIN Dongdong,ZHU Ziguo,HOU Hanghang,LIAN Yanhui,YAN Dandan,ZHANG Yang,LI Guirong. Determination of pollen viability,pollen quantity,and stigma receptivity for different grape cultivars[J] . Jiangsu Agricultural Sciences,2019,47(4):113-116.
[17] KELEN M,DEMIRTAS I. Pollen viability,germination capability and pollen production level of some grape varieties (Vitis viniferɑ L.)[J] . Acta Physiologiae Plantarum,2003,25(3):229-233.
[18] DINATO N B,VIGNA B B Z,DE MATTA F,FÁVERO A P. Increasing pollination possibilities in Pɑspɑlum species:In vitro and in vivo viability of cryopreserved pollen to address flowering asynchrony[J] . Biotechnology,2024,14(12):308.
[19] 郝梓瑶,宋杰,关文灵. 杜鹃园艺品种‘王妃’与黄杯杜鹃远缘杂交亲和性研究[J] . 植物学研究,2024,13(3):349-356.HAO Ziyao,SONG Jie,GUAN Wenling. Study on the compatibility of distant hybridization between Rhododendron horticultural varieties of‘Empress’ and R. wɑrdii[J] . Botanical Research,2024,13(3):349-356.
[20] 刘淑玟,郭素娟. 板栗‘燕山早丰’♀ב王钱大栗’♂适宜授粉时间的筛选[J] . 中南林业科技大学学报,2025,45(1):102-111.LIU Shumin,GUO Sujuan. Study on suitable pollination time screening of ‘Yanshanzaofeng’ ♀ × ‘Wangqiandali’ ♂[J] . Journal of Central South University of Forestry & Technology,2025,45(1):102-111.
[21] JIANG H Y,LI W,HE B J,GAO Y H,LU J X. Sucrose metabolism in grape (Vitis viniferɑ L.) branches under low temperature during overwintering covered with soil[J] . Plant Growth Regulation,2014,72(3):229-238.
[22] 杨正坤,王秀丽,龙施华,郝再彬,单展展,周菲菲. 考马斯亮蓝染色法测定大豆茎叶中蛋白质含量[J] . 湖北农业科学,2012,51(20):4610-4612.YANG Zhengkun,WANG Xiuli,LONG Shihua,HAO Zaibin,SHAN Zhanzhan,ZHOU Feifei. Determination of protein in soybean stems and leaves by Bradford method[J] . Hubei Agricultural Sciences,2012,51(20):4610-4612.
[23] TOIVONEN P M A,SWEENEY M. Differences in chlorophyll loss at 13 ℃ for two broccoli (Brɑssicɑ olerɑceɑ L.) cultivars associated with antioxidant enzyme activities[J] . Journal of Agricultural and Food Chemistry,1998,46(1):20-24.
[24] ZOU J N,JIN X J,WANG Y X Z C Y R M C Z M X. Effects of melatonin on photosynthesis and soybean seed growth during grain filling under drought stress[J] . Photosynthetica,2019,57(2):512-520.
[25] SRIVASTAVA O P,VAN HUYSTEE R B. Evidence for close association of peroxidase,polyphenol oxidase,and IAA oxidase isozymes of peanut suspension culture medium[J] . Canadian Journal of Botany,1973,51(11):2207-2215.
[26] BABY T,GILLIHAM M,TYERMAN S D,COLLINS C. Differential fruitset between grapevine cultivars is related to differences in pollen viability and amine concentration in flowers[J] .Australian Journal of Grape and Wine Research,2016,22(1):149-158.
[27] TELLO J,MONTEMAYOR M I,FORNECK A,IBÁÑEZ J. A new image-based tool for the high throughput phenotyping of pollen viability:Evaluation of inter- and intra-cultivar diversity in grapevine[J] . Plant Methods,2018,14:3.
[28] REN R F,GAO J Z,ZHOU H,ZHU M T,LIU Y. Changes of pollen viability after preservation of Pɑeoniɑ lɑctiflorɑ in different provenances[J] . Cryobiology,2022,105:10-19.
[29] DOLCE N R,MEDINA R D,MROGINSKI L A,REY H Y. Storage of Cohniellɑ cepulɑ (Orchidaceae) pollinia:Fertilizing ability and subsequent fruit and seed formation[J] . HortScience,2016,51(10):1265-1269.
[30] 戚行江,任海英,梁森苗,郑锡良,张振兰,邱立军. 贮藏温度和时间对杨梅和蜡杨梅花粉萌发率及保护酶活性的影响[J] . 果树学报,2014,31(3):460-467.QI Xingjiang,REN Haiying,LIANG Senmiao,ZHENG Xiliang,ZHANG Zhenlan,QIU Lijun. Effect of storage time and temperature on the germination rates and protective enzyme activities of Myricɑ rubicɑ and M. ceriferɑ pollens[J] . Journal of Fruit Science,2014,31(3):460-467.
[31] DAVID M,TIŢA A,TOMA I D,CIOBOTEA C M,BĂNUŢĂ M F. Pollen grain expression of osmotic adjustment as a screening method on drought tolerance in several wine and table grape genotypes (Vitis viniferɑ L.)[J] . Notulae Scientia Biologicae,2020,12(4):869-883.
[32] BAN Y,MITANI N,SATO A,KONO A,HAYASHI T. Genetic dissection of quantitative trait loci for berry traits in interspecific hybrid grape (Vitis lɑbruscɑnɑ × Vitis viniferɑ)[J] . Euphytica,2016,211(3):295-310.