猕猴桃(Actinidiɑ spp.)原产中国,种植面积和产量稳居世界首位,因其丰富的维生素C含量和香甜的口感,深受消费者喜爱[1-3]。近年来,随着我国猕猴桃产业迅速发展,消费者对高质量猕猴桃的需求量也越来越高[4]。猕猴桃采后软化进程迅速,不耐贮藏。因此,深入探究猕猴桃的软化机制,可为保鲜技术的研发提供理论依据。
果实软化是一种常见的生理现象,涉及物质代谢、细胞壁构成和基因表达的全面变化[5]。在猕猴桃中,果实后熟软化主要表现为淀粉的水解[6]。淀粉水解产生的葡萄糖和果糖,需经过已糖激酶(EC 2.7.1.1)和果糖激酶(EC 2.1.7.4)的磷酸化,生成己糖-6-磷酸,才能为下游的生理代谢途径提供原料[7-8]。研究表明,果糖激酶(fructokinase,FRK)是果糖磷酸化的特异性酶,对果糖的亲和力远高于已糖激酶[9]。此外,植物FRK在糖传感方面的功能可能与已糖激酶类似,其作为信号转导分子,调控植物的生长发育、淀粉积累和环境胁迫响应等过程[10-11]。目前,FRK在果实采后软化和衰老中的功能研究甚少。因此,对猕猴桃FRK基因家族和表达水平进行分析,有助于了解猕猴桃后熟软化过程中果糖的代谢机制,为提高猕猴桃果实品质提供理论依据。
植物FRK属于磷酸果糖激酶(phosphofructokinase type B,pfkB)家族,具有pfkB家族特异性区域(pfkB和ATP结合)和果糖激酶家族特征性底物识别区域[10]。目前,已经在多种植物中对FRK基因家族成员进行了分析,如番茄至少有4个FRK成员[12]、拟南芥有7个FRK成员[13]、苹果有9个FRK成员[14]、中国白梨有20个FRK成员[15]、木薯有7个FRK成员[16]、甘蔗有7个FRK成员[17]。Nardozza等[18]从猕猴桃EST数据库中鉴定出3个FRK成员(FK4、FK6和FK8),并发现其在不同基因型猕猴桃中有差异性表达,参与猕猴桃果实早期发育和淀粉代谢过程。然而,在猕猴桃基因组发布后,关于猕猴桃FRK基因家族成员的研究和报道却相对较少。
植物FRK的生化特性对果糖代谢的调控、不同逆境和激素信号的响应各不相同[9]。因此,笔者以红阳猕猴桃为试验材料,采用生物信息学方法对猕猴桃FRK基因家族成员进行鉴定;基于前期转录组测序结果及软化相关数据[19],分析AcFRK基因的表达丰度及其与果实软化的相关性;进一步分析Ac-FRK基因家族成员在果糖、葡萄糖和不同激素处理下的表达模式,以期为AcFRK基因在猕猴桃果糖代谢和软化过程中的功能研究提供参考依据。
1 材料和方法
1.1 材料与处理
红阳猕猴桃果实采自江西省宜春市奉新县猕猴桃果园(28.69° N,115.28° E)。采收时果肉可溶性固形物含量为7.0%~8.0%。采收当天运回实验室,挑选大小、形状一致、无机械损伤和病虫害的果实,进行试验处理。处理组1:己糖处理。用打孔器获取直径13 mm、厚5 mm的果肉圆片,将圆片均分为3组,每组约30 g。分别浸入含100 mmol·L-1甘露醇(对照)、100 mmol·L-1果糖和100 mmol·L-1葡萄糖的MES缓冲液(标准缓冲液为50 mmol·L-1 MES、5 mmol·L-1 CaCl2、5 mmol·L-1 MgCl2·6H2O、1 mmol·L-1 EDTA以及10 mmol·L-1抗坏血酸)中,于25℃ 100 r·min-1摇床中温育30 min。在0、4、12和24 h时取样,用于提取总RNA。处理组2:激素处理。将猕猴桃果实随机分成2份,第1份约360个果实,分别进行乙烯处理(ETH,100 μL·L-1乙烯熏蒸12 h)和对照处理(CK,常温密闭12 h);第2份约720个果实,包括4个处理:0.5 mmol·L-1脱落酸(ABA)、1 mmol·L-1乙酰水杨酸(AsA)、50 mg·L-1 α-萘乙酸(NAA)和清水(CS)浸泡5 min,自然晾干后于常温(20±1)℃、相对湿度85%的环境下贮藏10 d。每2 d取样1次,用于提取总RNA。每次取样以10个果实为1个生物学重复,共设置3个生物学重复。
1.2 AcFRKs基因家族成员鉴定
根据已有报道[12-13,16],从拟南芥TAIR网站(www.arabidopsis.org)和NCBI网站(https://www.ncbi.nlm.nih.gov)中分别下载7个拟南芥(Arɑbidopsis thɑliɑnɑ)AtFRK蛋白序列、4个番茄(Lycopersicon esculentum)LeFRK蛋白序列和6个木薯(Mɑnihot esculentɑ)蛋白序列作为诱饵,在红阳猕猴桃基因组数据库(https://kiwifruitgenome.org/organism/5)[20]中通过BLAST比对筛选FRK同源序列,e阈值设定为1e-5。使用HMMER在线软件(https://www.ebi.ac.uk/Tools/hmmer)对候选FRK基因家族成员进行保守结构域分析,鉴定上述候选成员是否存在完整的PF00294保守结构域(pfkB,磷酸果糖激酶B);使用NCBI-CDD网站(http://www.ncbi.nlm.nih.gov/Structure/cdd/cdd.shtml)进一步验证上述候选成员是否具有果糖激酶家族特征性结构域(substrate recognition,底物识别)[10-11]。据此,共鉴定得到6个AcFRK基因家族成员,按照其在染色体上的位置依次命名为AcFRK1~AcFRK6。
1.3 AcFRKs基因家族蛋白的理化特性分析
从猕猴桃基因组数据库中下载GFF3注释文件,使用TBtools软件[21]对6个AcFRK基因在染色体上的分布进行分析,利用Gene Location Visualize插件对各成员在染色体上的位置进行可视化。使用WoLF PSORT在线网站(https://www.genscript.com/wolf-psort.html)预测6个AcFRK蛋白的亚细胞定位,并通过基因组数据库中的亚细胞组分定位进行确认。理论等电点及平均分子质量使用在线网站(https://web.expasy.org/compute_pi/)进行预测。
1.4 AcFRKs基因家族蛋白的系统进化树和氨基酸序列分析
通过TAIR和NCBI网站下载拟南芥、番茄和木薯中已公布的FRK蛋白序列,利用ClustalX(version 1.81)进行多序列比对,比对结果采用Gendoc 32软件进行氨基酸序列分析;并在MEGA(version 5.05)软件中采用邻接法(neighbor-joining,NJ)构建系统进化树。
1.5 AcFRKs基因家族成员的保守基序及基因结构
使用MEME在线网站(https://meme-suite.org/meme/tools/meme)分析猕猴桃AcFRK1~AcFRK6蛋白的保守基序(motif),基序数设置为12,其余参数选择默认值。根据猕猴桃基因组注释文件,利用TBtools软件[21]分析AcFRK1~AcFRK6基因中外显子和非编码区的位置分布,并使用Visualize Gene Structure插件对AcFRK1~AcFRK6基因的结构特征进行可视化。
1.6 AcFRKs基因家族成员蛋白的二级结构与三级结构预测
利用SOPMA网站(https://npsa-prabi.ibcp.fr/cgi-bin/npsa_automat.pl page=npsa_sopma.ht-ml)进行氨基酸的二级结构预测。利用SWISS-MODEL网站(http://swissmodel.expasy.org/)构建蛋白质三级模型。
1.7 AcFRKs基因家族成员启动子的顺式作用元件分析
在猕猴桃基因组数据库中下载AcFRK1~Ac-FRK6基因上游2000 bp的启动子序列,在Plant-CARE在线网站(https://bioinformatics.psb.ugent.be/webtools/plantcare/html/)上分析启动子区顺式作用元件,重点关注植物生长发育、激素响应和胁迫响应元件,并对结果进行统计和可视化。
1.8 转录组测序及相关性分析
将常温贮藏第0天、第4天和第8天的猕猴桃果肉样品送至上海派森诺生物科技有限公司进行转录组测序,每个取样点设置3次重复。从转录组数据中获取上述6个AcFRK基因的FPKM值,经log2(FPKM+1)归一化处理后,使用Tbtools软件绘制基因表达热图。进一步分析AcFRK基因的FPKM值与果实软化的相关性,基于前期果实软化相关数据,即硬度、淀粉和还原糖含量[19],使用在线网站的相关性聚类标记热图工具(v 2.9.1,https://www.omicstudio.cn/tool/59)绘制相关性热图,皮尔逊相关系数值设定为0.5。
1.9 AcFRKs基因家族成员的表达分析
使用RNAprep Pure多糖多酚植物总RNA提取试剂盒(货号:DP441,北京天根生化科技有限公司)提取猕猴桃果肉总RNA,通过琼脂糖凝胶电泳检测总RNA的完整性,利用BioDrop超微量核酸蛋白分析仪(英国柏楉有限公司)检测总RNA纯度和浓度,使用反转录试剂盒(货号:11141ES60,上海翌圣生物科技有限公司)将RNA反转录成cDNA。基因表达通过实时荧光定量PCR(RT-qPCR)试验进行分析。利用Primer 3在线软件(https://primer3.ut.ee/)设计引物,详见表1,以AcActin(Actinidia06663)作为内参基因,根据溶解曲线验证引物的特异性。RT-qPCR反应体系、反应程序和基因表达计算参照笔者课题组之前的方法[19]。试验设置3个生物学重复,采用2-ΔΔCt方法计算基因的相对表达水平,将0 d的基因表达量设为1,作为参照。
表1 实时荧光定量PCR引物序列
Table 1 Primer sequences used for real-time quantitative PCR

基因名称Gene name AcFRK1 AcFRK2 AcFRK3 AcFRK4 AcFRK5 AcFRK6 AcActin上游引物序列(5′-3′)Forward primer (5′-3′)GAAGCTCCTCCTGGTCACTC GACAGGGGCCAGAAAGACTC TGCATTCCATGTCAAAACGGT GCCCGGGAGCACATTATGAG GGTGATGCCTTTGTTGGTGG GCTGCTGATGTCTCATTGGT TGGAATGGAAGCTGCAGGA下游引物序列(5′-3′)Reverse primer (5′-3′)CGTATCCACTGCTTTGACGTG GGTCCCCAACTTTACGTCCA GATGGCCCCACATGCATTTG TCTGCAACCTTTCTCACCAAG CGTAGGAAGGGCAGGAATGG CCATCGACTTGAGCAGAGCA CACCACTGAGCACAATGTTGC
1.10 数据统计与分析
试验数据均以平均值±标准误表示。采用SPSS软件(26.0版本)进行单因素方差检验,使用Duncan新复极差法进行差异显著性分析,并以字母标记法标示,使用Origin软件(8.0版本)处理数据和作图。
2 结果与分析
2.1 AcFRKs基因家族成员鉴定及分析
笔者从已公布的红阳猕猴桃基因组数据库(Hong Yang v3)中[20]鉴定出6个FRK基因家族成员,根据其在染色体上的位置依次命名为AcFRK1~Ac-FRK6。AcFRKs基因分布在5条不同的染色体(Lachesis group,LG)上,LG0、LG3、LG17和LG25染色体上各分布1个AcFRK基因,LG21染色体上有2个AcFRKs基因(图1)。亚细胞定位预测结果表明,AcFRK2和AcFRK6定位于叶绿体,其余4个均定位于细胞质(表2),表明FRK蛋白在叶绿体和细胞质中发挥不同的功能。进一步分析发现,6个AcFRKs蛋白中长度最短为168 aa(AcFRK1),最长为457 aa(AcFRK2),平均长度为304 aa;各AcFRKs蛋白质等电点最小为4.88(AcFRK4),最大为6.03(Ac-FRK5),平均等电点为5.47;AcFRKs蛋白质的分子质量最小为18.47 kDa(AcFRK1),最大为50.01 kDa(AcFRK2),平均分子质量为33.02 kDa。
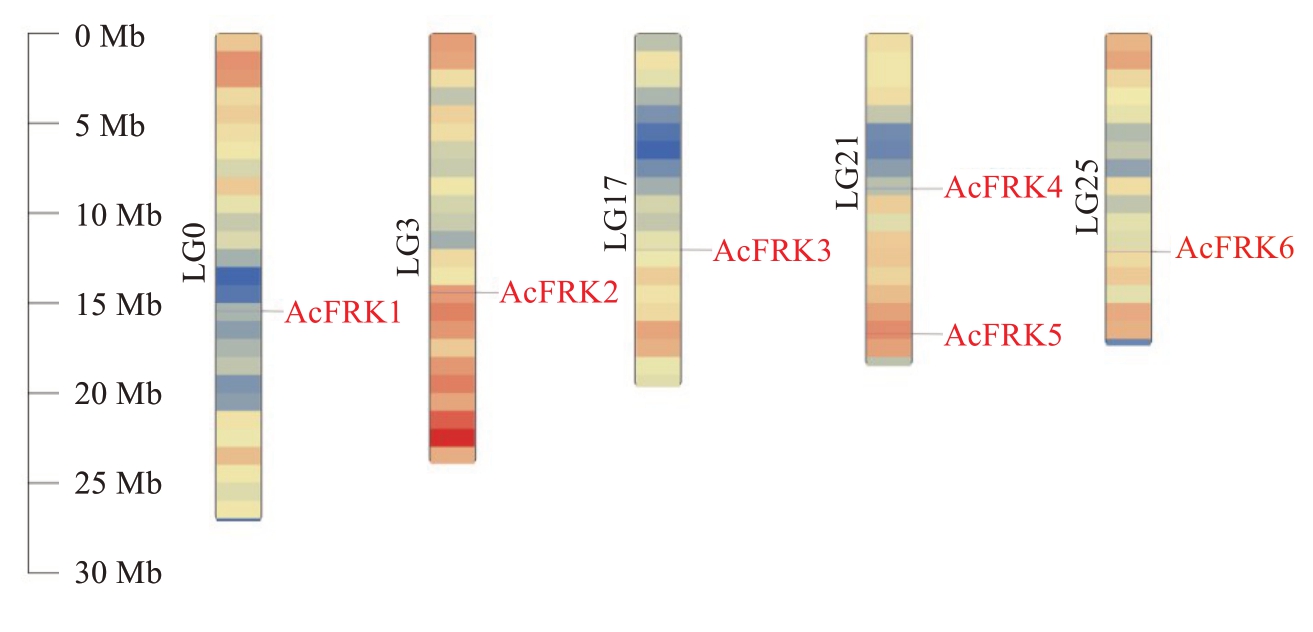
图1 AcFRKs基因家族染色体定位分析
Fig. 1 Chromosomal localization analysis of kiwifruit FRK gene family
表2 AcFRKs基因及其蛋白理化特性
Table 2 Characteristics of AcFRK genes and their deduced proteins
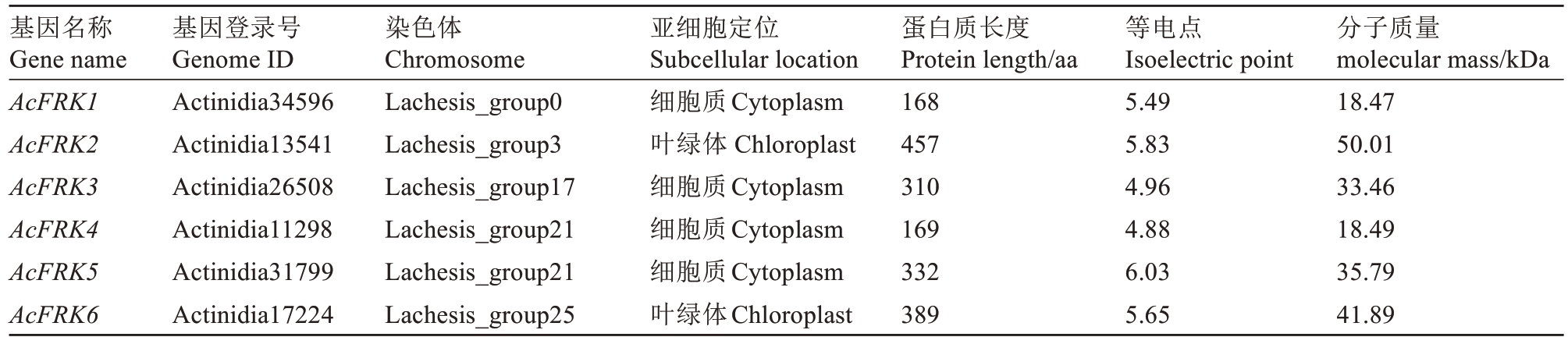
基因名称Gene name AcFRK1 AcFRK2 AcFRK3 AcFRK4 AcFRK5 AcFRK6基因登录号Genome ID Actinidia34596 Actinidia13541 Actinidia26508 Actinidia11298 Actinidia31799 Actinidia17224染色体Chromosome Lachesis_group0 Lachesis_group3 Lachesis_group17 Lachesis_group21 Lachesis_group21 Lachesis_group25亚细胞定位Subcellular location细胞质Cytoplasm叶绿体 Chloroplast细胞质Cytoplasm细胞质Cytoplasm细胞质Cytoplasm叶绿体Chloroplast蛋白质长度Protein length/aa 168 457 310 169 332 389等电点Isoelectric point 5.49 5.83 4.96 4.88 6.03 5.65分子质量molecular mass/kDa 18.47 50.01 33.46 18.49 35.79 41.89
2.2 AcFRKs基因家族成员蛋白系统进化树分析
为了阐明AcFRKs蛋白的功能和进化关系,选取猕猴桃(6个)、拟南芥(7个)、番茄(4个)和木薯(6个)的FRK蛋白序列构建了系统进化树。结果如图2所示,FRK可分为2个亚族(Group Ⅰ和GroupⅡ)。其中,第Ⅰ亚族有3个AcFRK成员,并与Me-FRK3、MeFRK4和LeFRK2聚为一类;第Ⅱa亚族有2个AcFRK成员,并与MeFRK2、AtFRK1和Le-FRK1聚为一类;第Ⅱb亚族有1个AcFRK成员,并与定位于质体的MeFRK1、AtFRK3和LeFRK3聚为一类。表明AcFRKs蛋白具有功能多样性,可能在质体和细胞质中发挥功能。
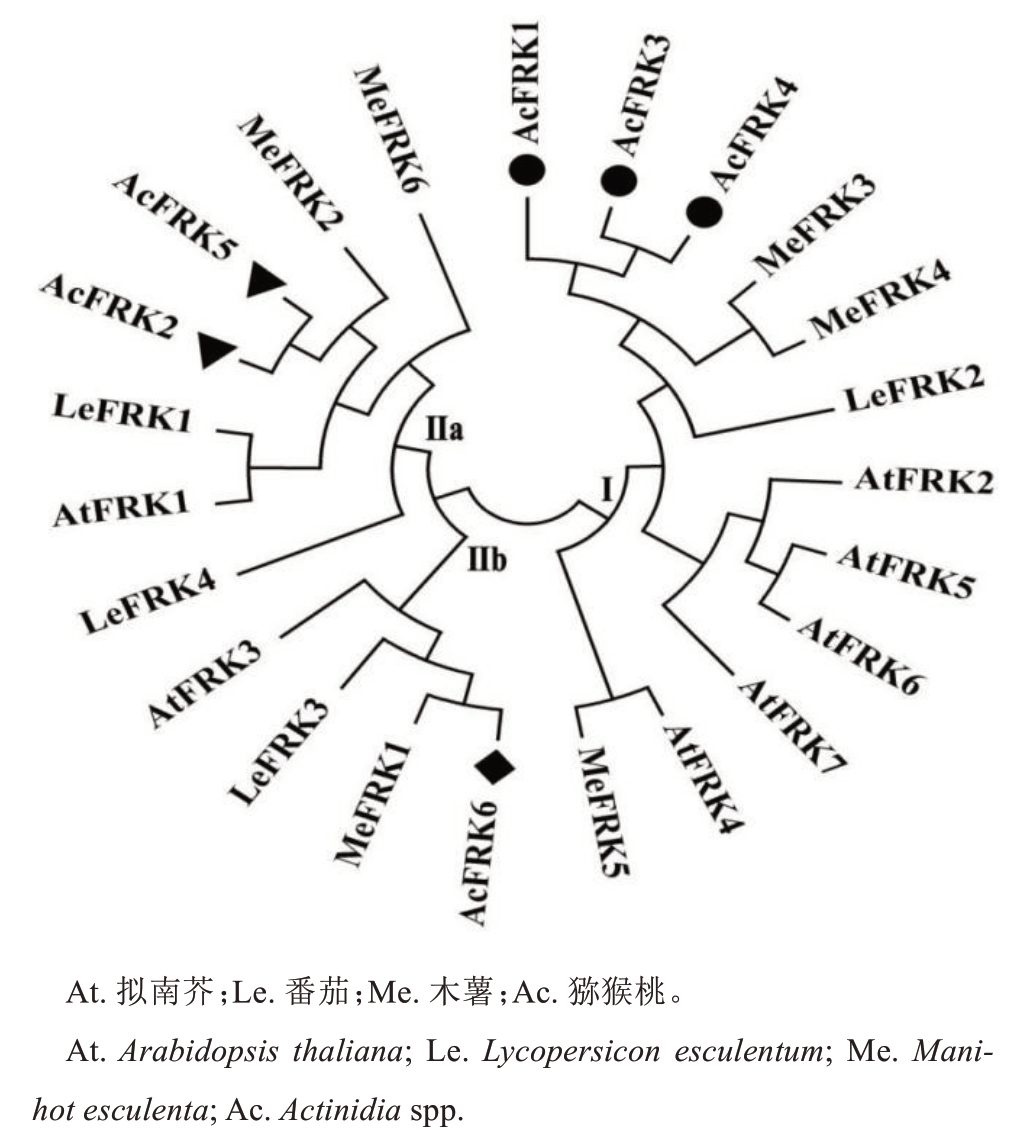
图2 猕猴桃与拟南芥、番茄和木薯FRK蛋白的进化树分析
Fig. 2 Phylogenetic analysis of the FRK proteins from kiwifruit, Arabidopsis, tomato, and cassava
2.3 AcFRKs基因家族成员氨基酸序列比对
对猕猴桃AcFRKs基因家族成员的氨基酸进行多序列比对分析,发现6个AcFRKs均具有pfkB家族特异性保守结构域,可以分为2种类型。AcFRK1和AcFRK4包括1个pfkB家族特异性区域、1个底物识别区域和1个ATP结合区域;AcFRK2、AcFRK3、AcFRK5和AcFRK6包括2个pfkB家族特异性区域,1个底物识别区域和1个ATP结合区域(图3)。由此可知,同一亚族中的成员具有高度相似的保守基序,该结果与系统发育树分类结果类似。

图3 AcFRKs与其他FRKs氨基酸序列分析
Fig. 3 Amino acid sequence analysis of AcFRKs and other FRKs
2.4 AcFRKs基因家族成员基因结构与保守基序分析
为进一步了解AcFRKs基因结构的异同,分析了外显子-内含子基因结构(图4-A)。结果表明,Ac-FRKs基因有0~3个非编码区(UTR)。AcFRK2、Ac-FRK5和AcFRK6有6~8个外显子,其编码的氨基酸长度较长;AcFRK1、AcFRK3和AcFRK4有3~4个外显子,其编码的氨基酸长度较短。
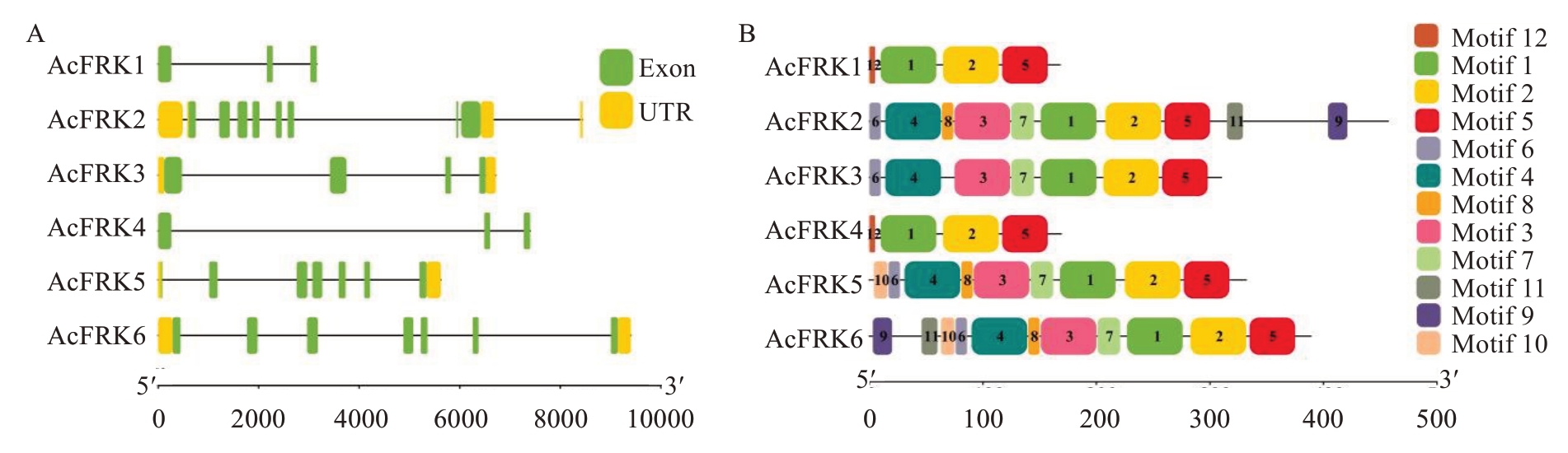
图4 AcFRKs基因结构(A)与保守基序(B)分析
Fig. 4 Structure (A) and conserved domain (B) of AcFRKs
通过MEME在线网站预测了FRK蛋白序列中的12个保守基序,结果如图4-B所示,AcFRK蛋白均含有motif 1和/或motif 7(底物识别;FRK家族特异性模块)、motif 2(ATP结合模块)和motif 5。除了AcFRK1和AcFRK4外,其他AcFRKs均含有motif 4(pfkB家族特异性模块)。AcFRK1和AcFRK4保守基序种类、数量和排列方式一致;AcFRK2、Ac-FRK3、AcFRK5和AcFRK6基因的主要保守基序较为一致。这些结果与氨基酸序列分析结果一致,表明同一亚族AcFRKs蛋白的保守性较高。
2.5 AcFRKs基因家族成员蛋白质结构分析
猕猴桃AcFRKs蛋白的二级结构如图5-A所示,6个AcFRKs蛋白序列主要含有α-螺旋、无规则卷曲、延伸链和β-转角。其中,α-螺旋(37.94%)占比最高,无规则卷曲(35.34%)次之,再次是延伸链(20.80%),β-转角(5.92%)占比最低(图5-B)。三维结构建模如图5-C所示,AcFRK1~AcFRK6蛋白质三维空间排列形成的蛋白质分子构象多种多样,其中AcFRK1、AcFRK3和AcFRK4(Group I)的蛋白质结构比较相似,AcFRK2、AcFRK5和AcFRK6(GroupⅡ)的蛋白质主体结构较为相似。
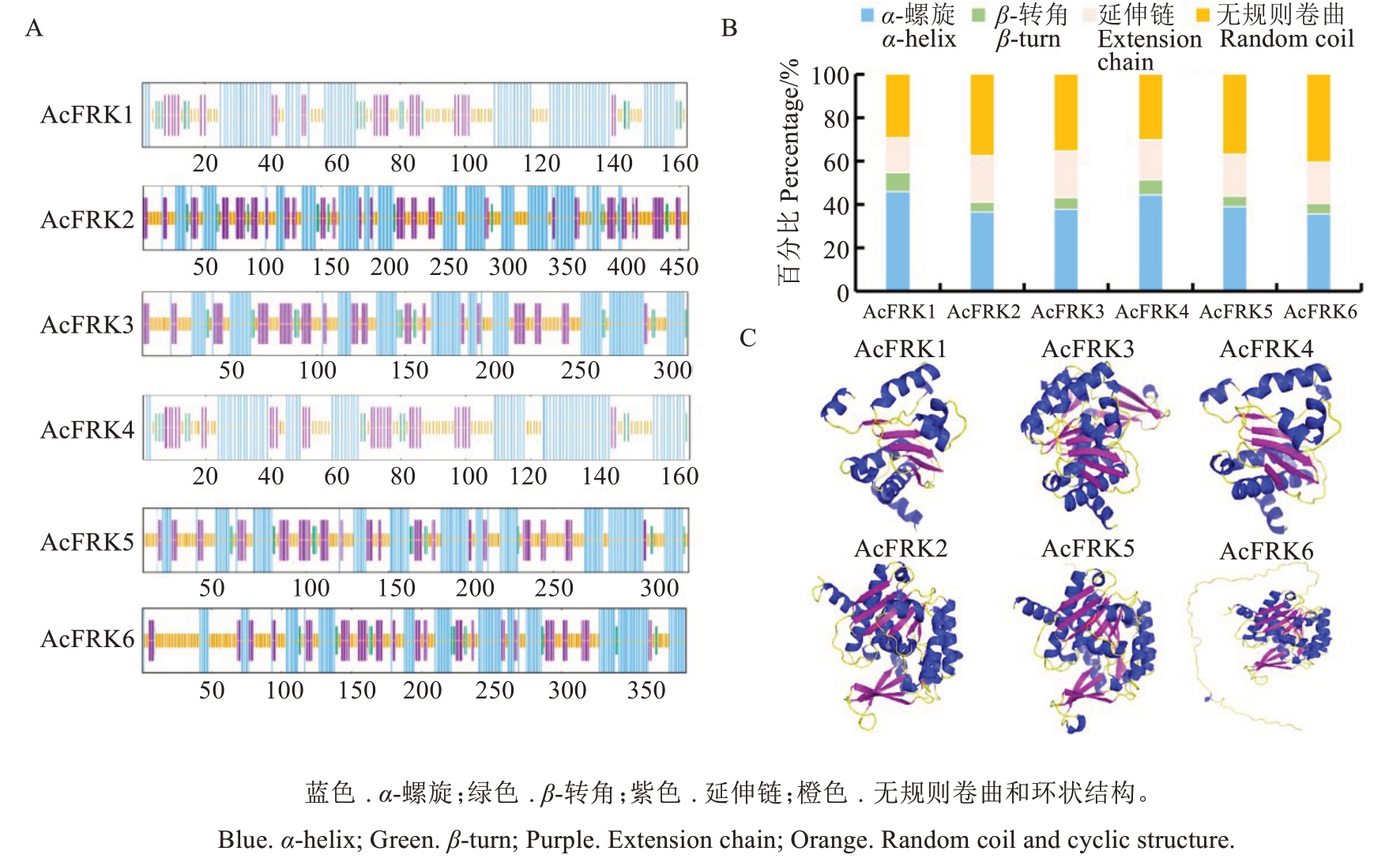
图5 AcFRKs蛋白质二级结构(A)、类型占比(B)和三级模型(C)
Fig. 5 Secondary structure (A), states percentage (B), and tertiary model (C) of AcFRK proteins
2.6 AcFRKs基因的启动子顺式作用元件分析
利用PlantCARE网站在AcFRKs基因启动子区域共鉴定出236个顺式作用元件,按功能可分为4种类型:生长发育、激素响应、胁迫响应和光响应元件,其中光响应元件未在图中显示(图6-A)。AcFRKs基因启动子区域存在14~33个顺式作用元件,Ac-FRK6基因最多(图6-B)。AcFRKs基因启动子上以激素响应元件(45.04%)最为丰富,其中以乙烯响应元件(ethylene response element,ERE)和脱落酸响应元件(abscisic acid responsivenss,ABRE)为主,推测AcFRKs基因极可能受到乙烯或脱落酸的诱导,进而参与调控猕猴桃后熟软化过程;其次是胁迫响应(42.75%),以渗透胁迫元件(osmotic stress response element,STRE)和氧化应激反应元件(as-1)为主,推测AcFRKs基因可能通过调节氧化应激反应以应对细胞内渗透压变化和猕猴桃后熟衰老进程。此外,AcFRKs基因还含有大量光响应元件,推测AcFRKs基因可能在植物的源和库中均发挥着重要作用。
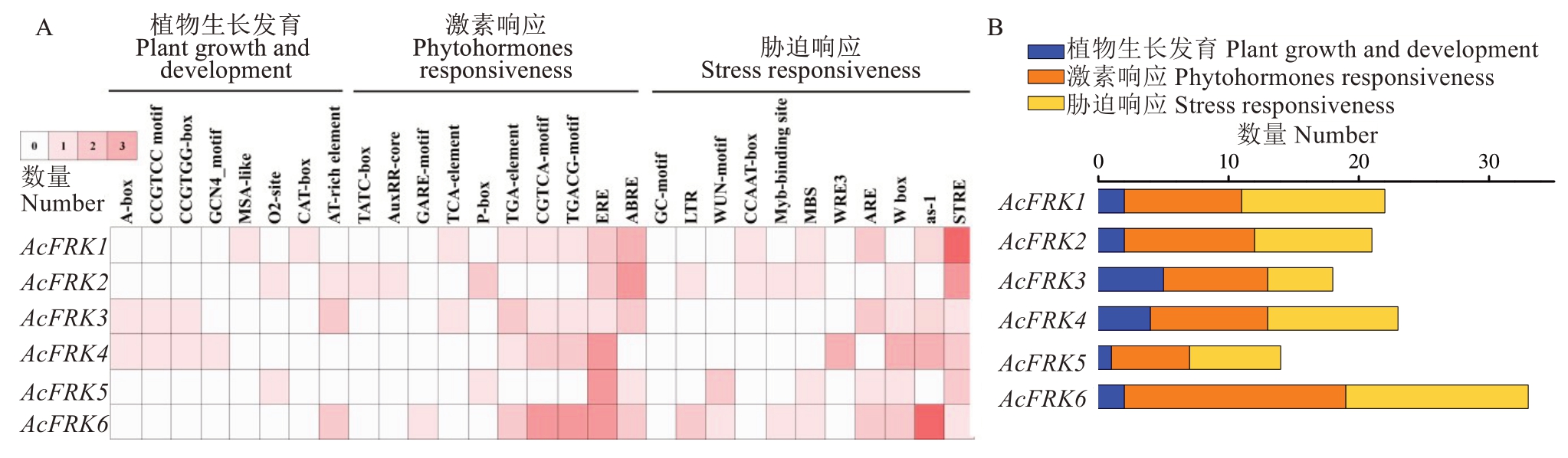
图6 AcFRKs基因启动子顺式作用元件特征(A)和数量(B)分析
Fig. 6 Characteristic (A) and quantitative (B) analysis of the promoters cis-acting element of AcFRKs
2.7 AcFRKs基因在猕猴桃后熟软化阶段的表达分析
为研究FRK基因家族成员在猕猴桃后熟软化过程中的表达模式,对红阳猕猴桃采后贮藏0、4和8 d的果肉样品进行转录组测序,并分析FRK基因表达丰度及其与果实软化的相关性,猕猴桃样品处理、硬度、淀粉和还原糖含量见前期报道[19]。表达量分析结果如图7-A所示,AcFRK1在猕猴桃后熟软化过程中几乎不表达;AcFRK3和AcFRK5随后熟时间的增加其表达量下调;AcFRK6表达量呈现先上升后下降的趋势,并在常温贮藏第4天达到峰值;Ac-FRK2和AcFRK4表达量随猕猴桃果实软化进程呈上升趋势,并在贮藏第8天达到峰值。进一步分析后熟过程中FRK表达量与软化的相关性,发现Ac-FRK2和AcFRK4的表达量与果实硬度和淀粉含量呈显著负相关,与还原糖含量呈显著正相关;而Ac-FRK3和AcFRK5的表达量则与果实硬度呈显著正相关(图7-B)。这些结果表明,猕猴桃FRK基因家族成员在猕猴桃后熟软化过程中存在不同的表达模式,并且AcFRK2和AcFRK4是促进果实软化的候选基因。
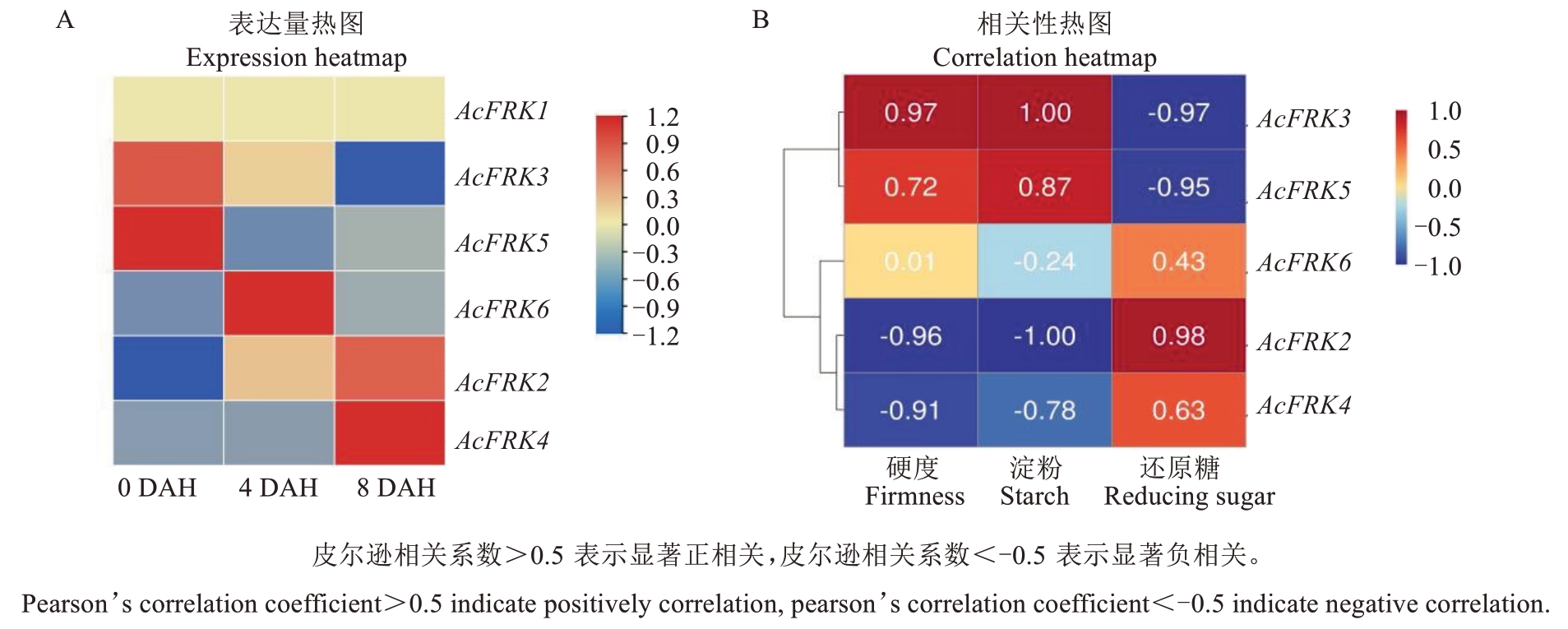
图7 AcFRKs家族成员表达量热图(A)和相关性热图(B)
Fig. 7 Heatmap of AcFRK gene family expression (A) and correlations (B)
2.8 AcFRKs基因响应己糖的表达模式
为进一步探讨AcFRK2和AcFRK4对己糖的响应机制,分析了这2个基因在不同浓度果糖和葡萄糖温育的猕猴桃果肉中的表达模式。结果如图8所示,在对照组和果糖组中,AcFRK2在处理前期不表达,后期(24 h)显著上调,但两组之间无显著差异;与对照和果糖相比,葡萄糖处理可显著上调贮藏4 h和12 h的AcFRK2表达量(P<0.05)。AcFRK4表达量随着贮藏时间的延长不断升高,果糖、葡萄糖处理均可显著上调其在贮藏4 h和12 h的表达量,其中,果糖处理表达量分别是对照组的2.54倍和1.44倍;葡萄糖处理则分别是对照组的1.91倍和1.42倍,但在贮藏后期无显著差异。这些结果表明,AcFRK2和AcFRK4基因的表达受到果糖和葡萄糖的调控,也进一步验证了AcFRK2和AcFRK4参与淀粉和糖代谢过程。
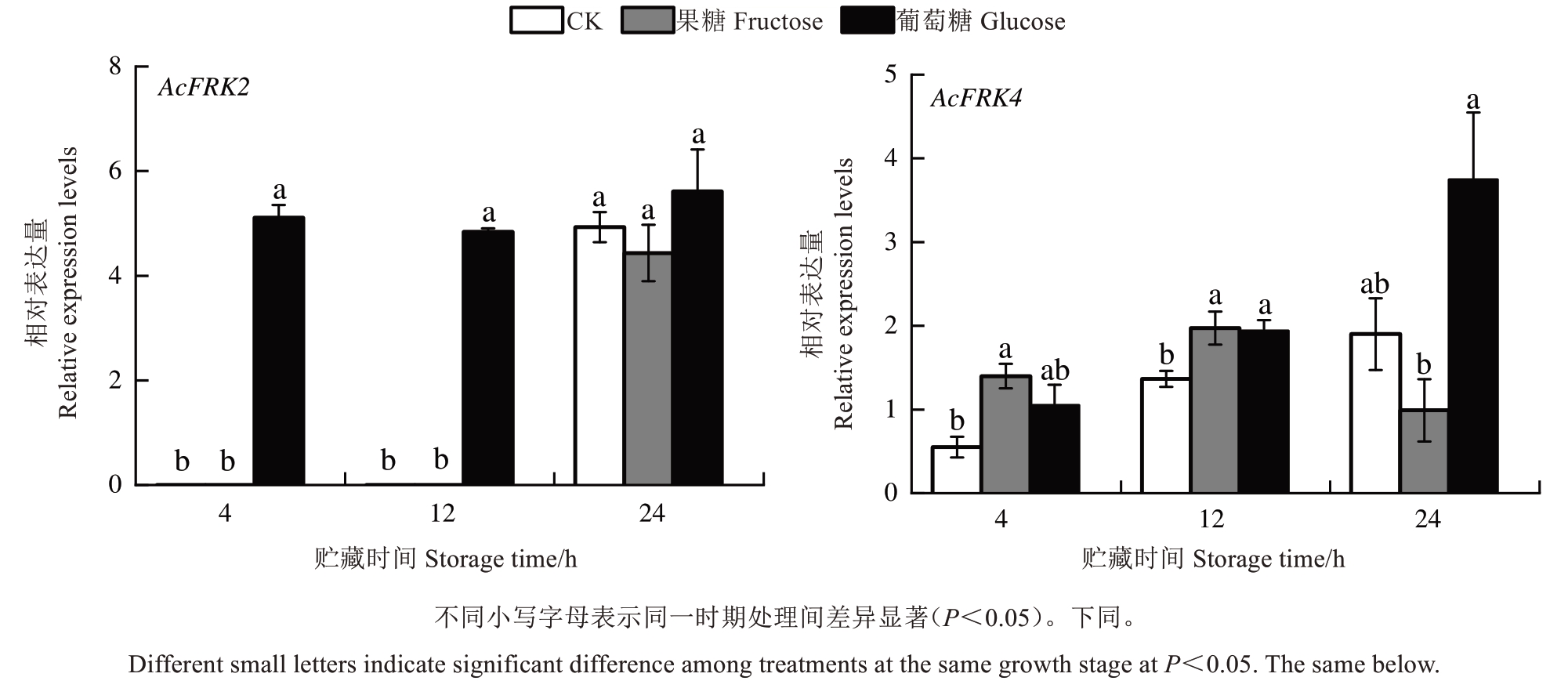
图8 果糖和葡萄糖温育对猕猴桃AcFRK2和AcFRK4基因表达的影响
Fig. 8 Gene expression levels of kiwifruit AcFRK2 and AcFRK4 under fructose and glucose incubation
2.9 AcFRKs基因响应外源激素的表达模式
笔者分析了不同激素即乙烯(ETH)、乙酰水杨酸(AsA)、脱落酸(ABA)和α-萘乙酸(NAA)处理下猕猴桃AcFRK2和AcFRK4的表达模式。结果如图9所示,在ETH处理下,与对照相比,AcFRK2在贮藏前期无表达,在贮藏后期被ETH显著诱导上调表达;AcFRK4的表达在贮藏过程中呈波动变化,但在贮藏后期(10 d),ETH显著诱导AcFRK4表达,其表达量是对照组的3.61倍。在ABA处理下,AcFRK2和AcFRK4的表达无规律性变化,但AcFRK4在贮藏第6天显著上调表达。AsA处理下,AcFRK2的表达变化无规律性,在贮藏第2天显著上调,但在贮藏第6天被显著抑制。而AcFRK4的表达在整个贮藏期被AsA诱导下调;AcFRK4在AsA诱导8 d后减幅最大,减少量为61.08%。NAA处理下,AcFRK2基本不表达。与对照相比,NAA处理降低AcFRK4的表达量;在NAA处理4 d后减幅最大,减少量为62.02%。因此,推测AcFRK2和AcFRK4可能通过响应ETH、NAA和AsA来参与猕猴桃后熟软化过程。
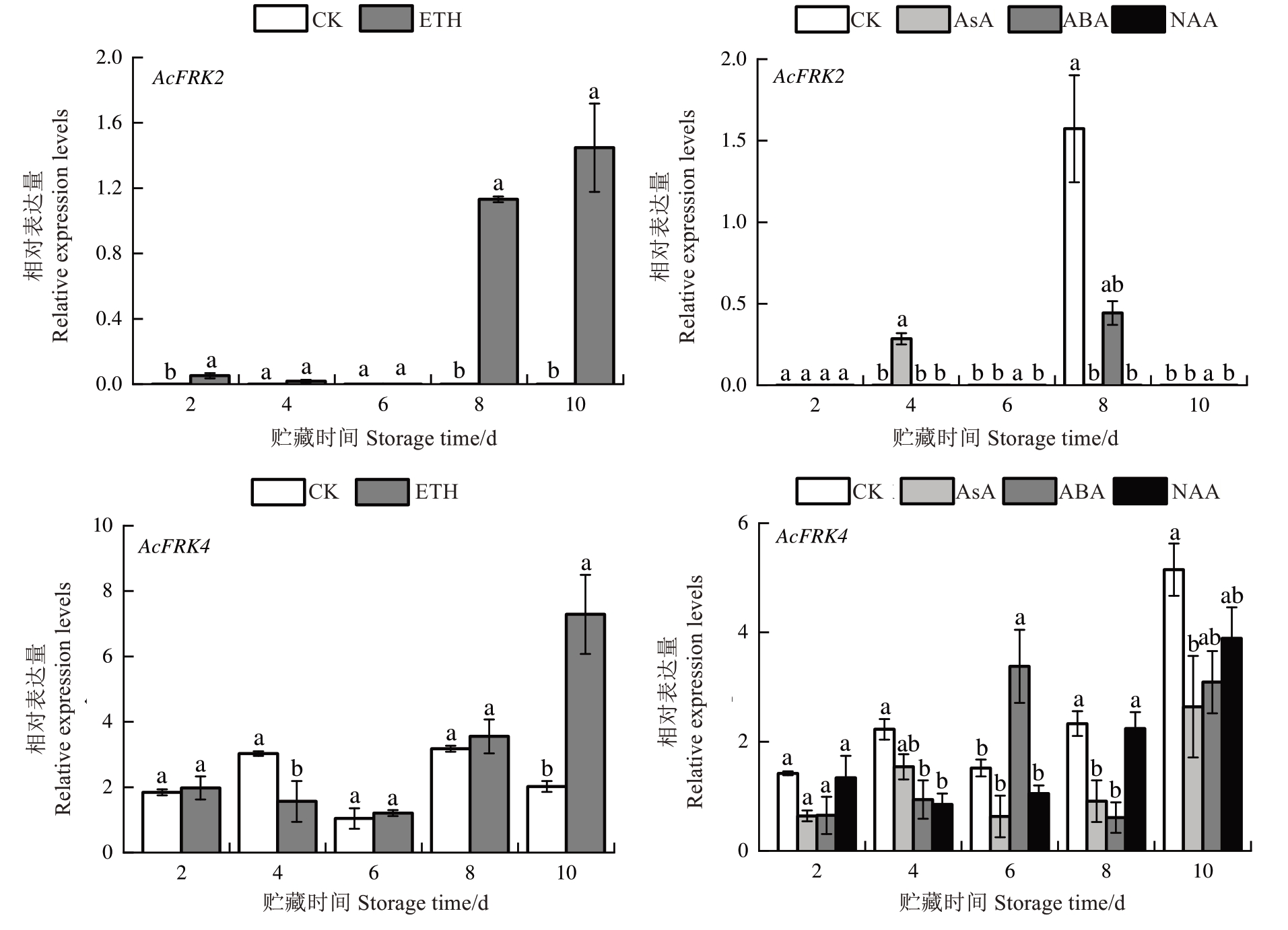
图9 激素处理对猕猴桃FRK2和FRK4基因表达的影响
Fig. 9 Gene expression levels of kiwifruit FRK2 and FRK4 after application of hormones
3 讨 论
FRK基因家族成员可介导植物细胞中果糖的流量,进而调节呼吸代谢途径[11]。研究表明,FRK基因在调控植物生长发育和胁迫响应过程中也发挥了重要作用[9-10]。笔者在猕猴桃基因组数据库中鉴定出6个AcFRK基因,不均匀地分布在5条染色体上,与Vizzotto等[22]的报道一致。系统进化树显示,Ac-FRKs蛋白分为2个亚族,且与拟南芥、番茄和木薯的聚类关系较近。其中,Ⅰ亚族定位于细胞质;Ⅱ亚族定位于细胞质或叶绿体,表明不同成员在特定部位中发挥作用,与前人[12-13,16]的研究结果较一致。基因结构分析发现,同一FRK亚族具有相似的结构和功能,其基因保守性较强。蛋白结构分析表明,Ac-FRKs蛋白二级结构主要由α-螺旋、无规则卷曲和延伸链组成,β-转角占比较少;三维结构模型显示同一类型FRK蛋白质结构更为相似,这也进一步表明了同一类型FRK可能具有相似的功能。对AcFRKs启动子序列分析表明,其区域富含多种激素响应元件,尤以乙烯和脱落酸响应元件最为丰富,推测AcFRKs基因的表达可能受ETH或ABA等诱导,进而参与猕猴桃糖代谢、果实成熟及逆境胁迫等过程。在苹果、木薯、甘蔗等其他植物的FRK基因启动子区域也发现了相同的顺式作用元件,受激素诱导而差异表达,并参与生物和非生物胁迫响应过程[14,17,23]。
FRK与植物库组织中的糖代谢密切相关,糖可作为碳源和信号分子调节下游基因的表达和代谢过程[9,24]。在枇杷果实中,EjFRK蛋白定位于细胞质,其转录水平可被100 mmol·L-1外源果糖和葡萄糖诱导上调,且无高浓度抑制效应[25]。在苹果中,Md-FRK2基因启动子活性和表达水平可被外源葡萄糖和果糖诱导上调,但在其启动子区并未发现已报道的糖响应元件[26]。与此类似,在本试验中AcFRK2主要被100 mmol·L-1葡萄糖诱导上调,而AcFRK4可同时响应葡萄糖和果糖。但在其启动子区域均未检测到糖响应元件,表明AcFRK2和AcFRK4存在未知的糖响应元件。AcFRK2和AcFRK4基因对葡萄糖和果糖的响应,可能在调控糖代谢并促进淀粉和蔗糖的高效利用中发挥作用[25,27]。
在猕猴桃采后贮藏过程中,淀粉降解为己糖(葡萄糖和果糖)。果糖主要被FRK磷酸化生成果糖-6-磷酸,进而启动糖酵解、呼吸代谢和其他次生代谢过程,加速果肉软化并缩短贮藏期[28-29]。因此,FRK在猕猴桃淀粉降解和软化过程中发挥重要作用。目前,关于植物FRK与淀粉代谢的研究,主要集中在淀粉积累和植物生长发育等方面[8,11],而对淀粉降解的研究相对较少。本研究结果表明,在猕猴桃后熟软化时期,AcFRKs基因呈现差异表达。进一步分析AcFRKs与软化的相关性,发现AcFRK2和AcFRK4基因表达水平与淀粉降解、果实软化呈正相关,推测这2个基因可能在猕猴桃采后果肉软化过程中起促进作用,但其具体功能还有待深入研究。
猕猴桃采后的成熟软化与激素信号存在紧密联系,尤其是ETH和ABA信号[30]。相关研究表明,外源激素可诱导FRK差异表达,而FRK可调节果糖信号转导,并参与植物糖代谢和生长发育过程[17,31-32]。笔者通过分析AcFRK2和AcFRK4对ETH、ABA、NAA和AsA处理的响应,发现AcFRK2和AcFRK4在ETH处理后期均显著上调表达,这与猕猴桃采后乙烯释放及软化的变化趋势相一致[30]。在ABA处理下AcFRK2和AcFRK4的表达无规律性变化,表明AcFRK2和AcFRK4主要被ETH诱导而非ABA来促进猕猴桃的后熟软化过程。AcFRK4在AsA处理第8天和NAA处理第4天显著下调表达,而1.0 mmol·L-1 AsA和50 mg·L-1 NAA处理可延缓猕猴桃的后熟软化过程[33-34],进一步表明AcFRK4表达与果实软化呈正相关。
4 结 论
笔者在猕猴桃基因组中共鉴定出6个FRK基因家族成员,分布于5条染色体上;亚细胞定位预测其主要定位于细胞质或叶绿体;系统进化分析将其分为2个亚族,同一亚族成员在基因和蛋白结构上相对保守;在FRK基因启动子序列上发现大量响应乙烯、脱落酸、渗透胁迫和氧化应激反应的元件。在猕猴桃后熟软化过程中,AcFRK2和AcFRK4表达水平上升;AcFRK2和AcFRK4可利用果糖和葡萄糖,并通过响应ETH、AsA和NAA等方式在猕猴桃后熟过程中调控糖代谢和软化。本研究结果为后续开展FRK功能验证、上游和下游调控机制等研究奠定了理论基础。
[1] PINTO T. Kiwifruit,a botany,chemical and sensory approach a review[J] . Advances in Plants & Agriculture Research,2018,8(6):383-390.
[2] 齐秀娟,郭丹丹,王然,钟云鹏,方金豹. 我国猕猴桃产业发展现状及对策建议[J] . 果树学报,2020,37(5):754-763.QI Xiujuan,GUO Dandan,WANG Ran,ZHONG Yunpeng,FANG Jinbao. Development status and suggestions on Chinese kiwifruit industry[J] . Journal of Fruit Science,2020,37(5):754-763.
[3] 郭琳琳,庞荣丽,王瑞萍,乔成奎,田发军,王彩霞,李君,庞涛,成昕,谢汉忠. 猕猴桃营养品质综合评价[J] . 果树学报,2022,39(10):1864-1872.GUO Linlin,PANG Rongli,WANG Ruiping,QIAO Chengkui,TIAN Fajun,WANG Caixia,LI Jun,PANG Tao,CHENG Xin,XIE Hanzhong. Comprehensive trait evaluation for kiwifruit nutritional quality[J] . Journal of Fruit Science,2022,39(10):1864-1872.
[4] 方金豹,钟彩虹. 新中国果树科学研究70年:猕猴桃[J] . 果树学报,2019,36(10):1352-1359.FANG Jinbao,ZHONG Caihong. Fruit scientific research in New China in the past 70 years:Kiwifruit[J] . Journal of Fruit Science,2019,36(10):1352-1359.
[5] PENG Z Z,LIU G S,LI H L,WANG Y X,GAO H Y,JEMRIĆ T,FU D Q. Molecular and genetic events determining the softening of fleshy fruits:A comprehensive review[J] . International Journal of Molecular Sciences,2022,23(20):12482.
[6] BURDON J,LALLU N. Kiwifruit (Actinidiɑ spp.)[M] //YAHIA E M. Postharvest biology and technology of tropical and subtropical fruits. Woodhead Publishing Inc.,2011:326-360.
[7] CLAEYSSEN É,RIVOAL J. Isozymes of plant hexokinase:Occurrence,properties and functions[J] . Phytochemistry,2007,68(6):709-731.
[8] GRANOT D,DAVID-SCHWARTZ R,KELLY G. Hexose kinases and their role in sugar-sensing and plant development[J] .Frontiers in Plant Science,2013,4:44.
[9] STEIN O,GRANOT D. Plant fructokinases:Evolutionary,developmental,and metabolic aspects in sink tissues[J] . Frontiers in Plant Science,2018,9:339.
[10] PEGO J V,SMEEKENS S C M. Plant fructokinases:A sweet family get-together[J] . Trends in Plant Science,2000,5(12):531-536.
[11] 叶香媛,周文彬. 植物果糖激酶研究进展[J] . 科学通报,2021,66(22):2820-2831.YE Xiangyuan,ZHOU Wenbin. Research advances in plant fructokinases[J] . Chinese Science Bulletin,2021,66(22):2820-2831.
[12] DAMARI-WEISSLER H,KANDEL-KFIR M,GIDONI D,METT A,BELAUSOV E,GRANOT D. Evidence for intracellular spatial separation of hexokinases and fructokinases in tomato plants[J] . Planta,2006,224(6):1495-1502.
[13] RIGGS J W,CAVALES P C,CHAPIRO S M,CALLIS J. Identification and biochemical characterization of the fructokinase gene family in Arɑbidopsis thɑliɑnɑ[J] . BMC Plant Biology,2017,17(1):83.
[14] SU J,ZHU L C,AO P X,SHAO J H,MA C H. Genome-wide identification,molecular evolution,and functional characterization of fructokinase gene family in apple reveal its role in improving salinity tolerance[J] . Journal of Integrative Agriculture,2024,23(11):3723-3736.
[15] CAO Y P,LI S M,HAN Y H,MENG D D,JIAO C Y,ABDULLAH M,LI D H,JIN Q,LIN Y,CAI Y P. A new insight into the evolution and functional divergence of FRK genes in Pyrus bretschneideri[J] . Royal Society Open Science,2018,5(7):171463.
[16] YAO Y,GENG M T,WU X H,SUN C,WANG Y L,CHEN X,SHANG L,LU X H,LI Z,LI R M,FU S P,DUAN R J,LIU J,HU X W,GUO J C. Identification,expression,and functional analysis of the fructokinase gene family in cassava[J] . International Journal of Molecular Sciences,2017,18(11):2398.
[17] CHEN Y H,ZHANG Q,HU W C,ZHANG X T,WANG L M,HUA X T,YU Q Y,MING R,ZHANG J S. Evolution and expression of the fructokinase gene family in Sɑcchɑrum[J] . BMC Genomics,2017,18(1):197.
[18] NARDOZZA S,BOLDINGH H L,OSORIO S,HÖHNE M,WOHLERS M,GLEAVE A P,MACRAE E A,RICHARDSON A C,ATKINSON R G,SULPICE R,FERNIE A R,CLEARWATER M J. Metabolic analysis of kiwifruit (Actinidiɑ deliciosɑ)berries from extreme genotypes reveals hallmarks for fruit starch metabolism[J] . Journal of Experimental Botany,2013,64(16):5049-5063.
[19] ZENG J K,WANG X H,DONG W J,XIANG M L,GAN Z Y,CHEN C Y,CHEN M,CHEN J Y. Transcriptome analysis reveals a regulatory role of hexokinase in kiwifruit postharvest softening[J] . LWT-Food Science and Technology,2025,223:117717.
[20] YUE J Y,LIU J C,TANG W,WU Y Q,TANG X F,LI W,YANG Y,WANG L H,HUANG S X,FANG C B,ZHAO K,FEI Z J,LIU Y S,ZHENG Y. Kiwifruit Genome Database(KGD):A comprehensive resource for kiwifruit genomics[J] .Horticulture Research,2020,7:117.
[21] CHEN C J,CHEN H,ZHANG Y,THOMAS H R,FRANK M H,HE Y H,XIA R. TBtools:An integrative toolkit developed for interactive analyses of big biological data[J] . Molecular Plant,2020,13(8):1194-1202.
[22] VIZZOTTO G,FALCHI R. Genetics of sugar and starch metabolism[M] //TESTOLIN R,HUANG H W,FERGUSON A R. The Kiwifruit genome. Cham:Springer International Publishing,2016:189-204.
[23] 吴金山,陆小静,王思琦,黄家权,张逸杰,贾迎雪,陈银华. 木薯FRK1类似基因的分离及表达分析[J] . 热带作物学报,2023,44(8):1525-1533.WU Jinshan,LU Xiaojing,WANG Siqi,HUANG Jiaquan,ZHANG Yijie,JIA Yingxue,CHEN Yinhua. Isolation and expression analysis of FRK1-like genes from cassava[J] . Chinese Journal of Tropical Crops,2023,44(8):1525-1533.
[24] ROSA M,PRADO C,PODAZZA G,INTERDONATO R,GONZÁLEZ J A,HILAL M,PRADO F E. Soluble sugars:Metabolism,sensing and abiotic stress:A complex network in the life of plants[J] . Plant Signaling & Behavior,2009,4(5):388-393.
[25] QIN Q P,CUI Y Y,ZHANG L L,LIN F F,LAI Q X. Isolation and induced expression of a fructokinase gene from loquat[J] .Russian Journal of Plant Physiology,2014,61(3):289-297.
[26] YANG J J,ZHAN R L,JIN Y R,SONG J Y,LI D X,AN G Y,LI M J. Functional analysis of the promoter of the MdFRK2 gene encoding a high-affinity fructokinase in apple (Mɑlus × domesticɑ)[J] . Scientia Horticulturae,2020,265:109088.
[27] KANAYAMA Y,GRANOT D,DAI N,PETREIKOV M,SCHAFFER A,POWELL A,BENNETT A. Tomato fructokinases exhibit differential expression and substrate regulation[J] .Plant Physiology,1998,117(1):85-90.
[28] 冉欣雨,黄文俊,钟彩虹. 猕猴桃果实淀粉代谢研究进展[J] .果树学报,2024,41(2):325-337.RAN Xinyu,HUANG Wenjun,ZHONG Caihong. Advance in starch metabolism research of kiwifruit[J] . Journal of Fruit Science,2024,41(2):325-337.
[29] YU J W,TSENG Y,PHAM K,LIU M,BECKLES D M. Starch and sugars as determinants of postharvest shelf life and quality:Some new and surprising roles[J] . Current Opinion in Biotechnology,2022,78:102844.
[30] LIN M F,GAO Z,WANG X L,MAO J P,PAN L Y,GONG X C,YAO D L,ZHONG H Q,HUO H Q. Identification of two postharvest ripening regulatory models in kiwifruit:Based on plant hormones,physiology,and transcriptome analysis[J] .BMC Plant Biology,2024,24(1):1121.
[31] CHO Y H,YOO S D. Signaling role of fructose mediated by FINS1/FBP in Arɑbidopsis thɑliɑnɑ[J] . PLoS Genetics,2011,7(1):e1001263.
[32] DU M,ZHU Y C,NAN H,ZHOU Y J,PAN X J. Regulation of sugar metabolism in fruits[J] . Scientia Horticulturae,2024,326:112712.
[33] 陈昆松,李方,张上隆,ROSS G S. ABA和IAA对猕猴桃果实成熟进程的调控[J] . 园艺学报,1999,26(2):81-86.CHEN Kunsong,LI Fang,ZHANG Shanglong,ROSS G S.Role of abscisic acid and indole-3-acetic acid in kiwifruit ripening[J] . Acta Horticulturae Sinica,1999,26(2):81-86.
[34] YIN X R,ZHANG Y,ZHANG B,YANG S L,SHI Y N,FERGUSON I B,CHEN K S. Effects of acetylsalicylic acid on kiwifruit ethylene biosynthesis and signaling components[J] . Postharvest Biology and Technology,2013,83:27-33.