刺葡萄(Vitis dɑvidii)隶属葡萄科(Vitaceae)葡萄属(Vitis)东亚种群,是一种尚未完全驯化的野生植物资源,在我国主要集中分布于湘西地区[1]。该物种对环境适应性强,尤其耐高温高湿环境,且抗病性突出,其果粒大小在东亚种群中最大,因此被视为极具价值的优良种质资源[2]。湘刺1号(又称甜刺葡萄)是由湖南农业大学葡萄课题组从怀化市中方县传统刺葡萄品种湘珍珠中选育出的新品种,现为该县刺葡萄产区的主栽品种。该品种果皮呈典型的紫黑色并覆有白色果霜,具有可溶性固形物含量高、可滴定酸含量低及丰产稳产等优良生物学特性,是兼具优良加工品质与栽培适应性的地方特色葡萄种质资源[3]。其母本湘珍珠葡萄已于2013年荣获国家地理标志保护产品称号,进一步彰显了该品种群的独特地域价值。
有机酸是水果酸度的主要成分,可通过可滴定酸(TA)含量和pH值衡量,它与可溶性糖协同作用,共同决定果实的风味轮廓与整体感官品质[4-6]。在果实中,有机酸在调节渗透压平衡、稳定pH值、增强抗逆性和提升水果感官品质方面发挥着不可或缺的作用[5,7]。大多数果实主要含有苹果酸和柠檬酸[8],而葡萄果实则主要含有酒石酸和苹果酸[9]。果实中有机酸主要积累于液泡中,其含量受合成、积累和消耗等多个因素的影响。此外,液泡内的有机酸强弱以及液泡膜上的离子泵、载体、通道蛋白等因素也对其积累存在影响[7]。液泡膜二羧酸转运蛋白(tDT)[10-11]、铝激活苹果酸转运蛋白(ALMT6和ALMT9/Ma1)[12-14]、液泡柠檬酸盐/H+同向转运体Cit1[15]以及液泡膜质子泵如液泡型ATPase(H+-ATPase/V-ATPase)、液泡型焦磷酸酶(H+-PPiase/VPPase)和P-ATPase(PH1和PH5等)共同驱动苹果酸和柠檬酸在液泡中积累[7,16-18]。已有研究表明,果实中苹果酸和柠檬酸的积累受合成代谢调控[19-20]。有机酸的合成始于糖酵解产生的磷酸烯醇式丙酮酸(PEP),经PEP羧化酶(PEPC)催化生成草酰乙酸(OAA);OAA在细胞质中被NAD依赖型苹果酸脱氢酶(NAD-cytMDH)还原为苹果酸储存于液泡,或参与三羧酸循环合成柠檬酸。目前,针对葡萄有机酸的研究主要集中于不同品种的组分、含量分析及其影响因素方面,而有关其合成代谢与运输机制的报道则相对有限[21]。
MYB、bHLH、NAC和WRKY等转录因子在果实有机酸积累的调控中发挥重要作用。在苹果中,R2R3-MYB转录因子MdMYB1/10、MdMYB44和Md-MYB73通过直接调控液泡膜定位的苹果酸转运蛋白基因(MdALMT9)和质子泵基因(MdVHA-A和MdVHP1)的表达,影响果实苹果酸的积累和液泡酸化过程[22-24]。MdbHLH3可以直接激活苹果酸脱氢酶基因MdcyMDH表达,促进果实苹果酸的积累;也可以与MdMYB1形成复合体,促进果肉花青素和苹果酸的积累[24-25]。在番茄中,SlWRKY42通过结合苹果酸转运蛋白基因ALMT9的启动子,调控苹果酸积累[26]。在柑橘中,CiWRKY1与CiNAC62相互作用,通过上调CiAco3基因表达,降低柠檬酸含量[27]。最新研究发现,苹果MdWRKY126和梨PbWRKY26均参与果实苹果酸的积累调控[24,28]。已有研究表明,在葡萄(V. viniferɑ)中,MdWRKY126和PbWRKY26的同源基因VvWRKY26可与VvMYB5ɑ/b、VvMYC1和VvWD1形成MBWW复合物,通过调控质子泵基因PH1/PH5的表达,进而参与液泡酸化过程[29]。果实中的柠檬酸和苹果酸主要通过液泡的“酸陷阱”机制实现特异性积累,即积累水平主要取决于它们从细胞质到液泡的运输效率[7,22]。综上,液泡酸化是驱动果实有机酸(尤其是苹果酸和柠檬酸)通过“酸陷阱”机制实现特异性积累的关键环节。基于此,本研究通过对VdWRKY26在不同组织中的表达模式进行分析,明确其亚细胞定位,并通过葡萄41B细胞稳定转化探究VdWRKY26在果实有机酸积累调控中的功能。该研究结果可为刺葡萄果实品质改良和种质创新提供候选靶基因,具有一定理论和应用意义。
1 材料和方法
1.1 试验材料
试验材料为刺葡萄湘刺1号品种,果实样品采自湖南省长沙市长沙县湖南农业大学长安基地,分别在刺葡萄花后7、13、20、26、33、39、49、54、60、68、74、80、88、96、103、109、116、123和130 d(DAFB)的果实发育阶段进行取样。每次取样均随机选取无病害、发育正常的果实。每个样品设置3个生物学重复,每个重复由3~4粒果实组成。采集后的样品经标记处理后立即用液氮速冻,并在低温条件下研磨成粉末,储存于-80 ℃超低温冰箱中备用。
葡萄41B悬浮细胞系是一种源自欧美杂交种(Vitis viniferɑ ‘Chasselas’ × V. berlɑndieri)花药的胚性细胞系。本研究使用的葡萄41B悬浮细胞由中国科学院植物研究所梁振昌实验室惠赠。
41B细胞培养方案分为两种,固体培养:每30 d更换一次GM培养基(更换周期不超过45 d,以免影响活性)。使用灭菌取样勺将细胞从旧培养基转移至新培养基表面,轻摊均匀以确保细胞与培养基充分接触,同时避免过度分散。培养条件为26 ℃,持续黑暗。液体悬浮培养:每7 d更换一次培养基。操作如下:向100 mL无菌三角瓶中加入30~40 mL GM液体培养基;随后接入0.5~1.0 mL 41B细胞悬浮液(使用5 mL移液管吸取细胞,移液管尖端紧贴瓶底缓慢排尽液体)。培养条件为26 ℃、120 r·min-1振荡、持续黑暗。GM培养基的配制参考Goebel-Tourand等[30]的方法。GM培养基配方:Glycerol(Duchefa G1345)4.6 g·L-1,Maltose(Duchefa M0811)18 g·L-1,N-Z-Amine A(Sigma C7290)1 g·L-1,Milieu MS 1/2 Macro(Duchefa M0232)2.18 g·L-1,Vitamines GM X1000 1 mL·L-1,NOA溶液(0.2 mg·mL-1,NaOH溶解,4 ℃保存)5 mL·L-1,pH=5.8。用于固体培养时添加7 g·L-1植物琼脂,并于121 ℃灭菌20 min。除NOA购自北京索莱宝科技有限公司外,其余试剂均购自Duchefa公司。
1.2 湘刺1号果实总RNA提取、cDNA合成及qP‐CR
总RNA提取使用植物快速RNA提取试剂盒(FastPure Universal Plant Total RNA Isolation Kit,诺唯赞,中国),具体操作步骤参照试剂盒说明书。提取的RNA通过1%琼脂糖凝胶电泳检测其完整性,并使用超微量分光光度计(Nano-530)测定RNA浓度。使用反转录试剂盒(HiScript Ⅱ Reverse Transcriptase,诺唯赞,中国),按照说明书将RNA反转录为cDNA。使用SnapGene软件对目标序列进行比对,并利用Primer-BLAST工具设计引物,筛选产物大小合适且特异性较高的引物序列,由北京擎科生物科技有限公司合成。试验中以葡萄Actin(Vitvi05_01chr04g23050)基因作为内参基因[31],定量引物序列详见表1(Actin_qPCR_F、Actin_qPCR_R、VdWRKY26_qPCR_F、VdWRKY26_qPCR_R)。荧光定量PCR反应使用预混型(perfectStɑrt® Green qPCR SuperMix,全式金,中国)试剂盒,反应体系按试剂盒说明书进行配制。反应程序设置为94 ℃预变性30 s;94 ℃变性5 s,60 ℃退火/延伸30 s,40个循环。荧光信号通过实时荧光定量PCR仪检测。
表1 引物序列
Table 1 Primer sequence

引物名称Primer name VdWRKY26-F VdWRKY26-R proVdWRKY26-F proVdWRKY26-R BP-F BP-R GFP-F T35S-R pro-F pro-R Actin_qPCR_F Actin_qPCR_R VdWRKY26_qPCR_F VdWRKY26_qPCR_R引物序列(5′-3′)Primer sequence (5′-3′)GGGGACAAGTTTGTACAAAAAAGCAGGCTGCATGGAGATTAAAGAGTCTGAGAGG GGGGACCACTTTGTACAAGAAAGCTGGGTTCATGGTTTCTCTTTATTCGTATGGGC GGGGACAAGTTTGTACAAAAAAGCAGGCTTCATGTCGTGTGTGGTGTACCTTG GGGGACCACTTTGTACAAGAAAGCTGGGTTTTCAATTGATTAATAGAGTGCTGC CGCGTTAACGCTAGCATGGATC TGTAACATCAGAGATTTTGAGACACG GCAAAGACCCCAACGAGAAGCG TGCTCAACACATGAGCGAAAC CTTCAACGTTGCGGTTCTGTCA CCGTCCAGCTCGACCAGGAT GATTCTGGTGATGGTGTGAGT GACAATTTCCCGTTCAGCAGT AATGTGCGCAAGCATGTGGA CCTGCATATCTGGTTCAGAG
1.3 刺葡萄不同发育时期VdWRKY26基因的表达分析
RNA-seq测序数据分析:将下机数据经过去除接头和过滤低质量序列后获得高质量测序数据(Clean Data),使用HISAT2软件将Clean Data比对到葡萄基因组数据库(http://grapegenomics.com)。随后,利用StringTie将成功比对的reads进行转录本组装,并通过最大流量算法计算基因表达量,以FPKM(每千个碱基的转录本每百万片段映射的片段数)作为基因表达水平的量化指标。差异表达分析使用DESeq2工具,筛选条件为表达倍数变化(Fold Change)≥2且错误发现率(FDR)<0.05。
相关性网络分析:提取VdWRKY26(Vitvi08g01134)在刺葡萄果实发育期的表达数据,并使用Tbtools软件绘制基因表达热图。使用R包psych计算与有机酸(酒石酸、苹果酸)相关基因的表达数据、有机酸含量皮尔逊相关系数及FDR值,并基于皮尔逊相关系数和FDR值,筛选出显著相关的基因与有机酸,使用Gephi 0.10软件绘制相关性网络图。
1.4 有机酸含量测定
将采集的样品经液氮快速冷冻研磨后,准确称取1 g粉末,置于50 mL离心管中;加入25 mL由超纯水配制的0.8% 1 mol·L-1磷酸溶液,于25 ℃恒温水浴中振荡浸提10 min;浸提完成后,在4 ℃、12 000 r·min-1条件下离心20 min。取上清液,经0.22 µm有机系滤膜过滤后置于1.5 mL进样瓶,通过高效液相色谱法(HPLC)测定苹果酸、酒石酸、柠檬酸的含量。每个时期设置3次生物学重复和2次技术重复。色谱柱:Agilent ZORBAX Eclipse C18色谱柱(250 mm×4.6 mm×5 mm);保护柱:Agilent C18保护柱;流动相:纯甲醇/0.1%磷酸(pH=2.8)=5.5/94.5;流速0.8 mL·min-1;柱温25 ℃;进样量10 μL;检测波长210 nm;洗脱梯度:等度洗脱。
1.5 VdWRKY26基因及启动子引物设计
从葡萄基因组数据库中获取VvWRKY26(Vitvi08g01134)的CDS区全长序列,与刺葡萄基因组中VdWRKY26序列比对后,利用Oligo 7软件设计编码区特异性引物VdWRKY26-F和VdWRKY26-F(表1)。从葡萄基因组数据库中获取VdWRKY26基因的启动子序列,并通过PlantCARE(https://bioinfor- mat-ics.psb.ugent.be/webtools/plantcare/html/)预测其启动子顺式作用元件的功能和位置。根据分析结果设计克隆引物proVdWRKY26-F和proVdWRKY26-R(表1),用于扩增VdWRKY26基因ATG上游2545 bp的启动子区域。
1.6 VdWRKY26基因克隆及表达载体构建
以刺葡萄果实组织RNA逆转录的cDNA为模板,利用含有ɑttB位点的特异性引物扩增Vd-WRKY26基因CDS序列。PCR产物经1.5%的琼脂糖凝胶电泳检测后,使用胶回收试剂盒(TS-INGKE TSP602-200 Trelief® DNA Gel Extraction Kit,擎科,中国)纯化回收,并利用Gateway系统(Gateway™BP Clonase™ Ⅱ,赛默飞世尔科技,美国)构建BP重组载体,将连接产物通过热激法转入大肠杆菌DH5α中,涂板培养1 d后挑取单菌落进行PCR鉴定,将阳性克隆送至生工生物工程(长沙)有限公司进行测序,经比对确认测序结果与目标序列一致后,保存阳性克隆并提取重组质粒。随后,利用Gateway系统(GatewayTM LR ClonaseTM Ⅱ,赛默飞世尔科技,美国)构建35S:GFP-VdWRKY26载体,将连接产物转入大肠杆菌DH5α,经测序验证正确后提取质粒。所用引物(BP-F、BP-R、GFP-F、T35S-R)序列信息见表1。
1.7 VdWRKY26氨基酸多重序列比对及系统进化树构建
通过对VdWRKY26的CDS进行测序并翻译,获得其氨基酸序列。同时通过NCBI数据库(https://www.ncbi.nlm.nih.gov/)获取欧亚种葡萄VvWRKY26、番茄SlWRKY44、苹果MdWRKY44和MdWRKY126、梨PyWRKY44和PbWRKY26、矮牵牛PhPH3、柑橘Cs-WRKY44以及拟南芥ATWRKY44的氨基酸序列,利用Tbtools和DNAMAN软件对上述蛋白序列进行多重比对分析,并通过MEGA 12.0软件构建系统进化树,计算模型为NJ,自展重复1000次。
1.8 VdWRKY26亚细胞定位
亚细胞定位试验参考Xie等[32]的方法并稍作改进。将测序验证正确的GFP-VdWRKY26重组质粒转化至农杆菌EHA105中,并在含有盐酸壮观霉素(spectinomycin,Spec)和利福平(rifampicin,Rif)的培养基上进行选择性培养。挑取阳性单菌落接种于含Rif(20 mg·L-1)和Spec(50 mg·L-1)的LB液体培养基中,28 ℃培养至OD600为0.6~0.8。离心收集菌体,经重悬液(10 μmol·L-1 MgCl2、10 μmol·L-1 MES、200 μmol·L-1 Acetosyringone,pH=5.6)悬浮后于28 ℃摇床,暗培养4 h。
以定位于细胞核的RFP-PhPH3载体作为对照[33],将GFP-VdWRKY26与RFP-PhPH3菌液按1∶1的比例重悬并混合均匀。使用1 mL一次性注射器将重悬菌液注射于生长健康的本氏烟草叶片背面。光照培养50 h后,通过激光共聚焦显微镜(Zeiss LSM710)观察烟草叶片中RFP和GFP融合蛋白荧光信号的分布情况,并保存图像。其中,GFP的激发波长为488 nm,RFP的激发波长为562 nm。
1.9 VdWRKY26基因启动子克隆及表达载体构建
从葡萄基因组数据库中提取VdWRKY26基因ATG上游启动子序列,以提取的刺葡萄组培苗叶片组织DNA作为模板,利用SnapGene软件设计特异性引物并进行扩增,PCR产物经1.5%的琼脂糖凝胶电泳检测后进行胶回收(TS-INGKE TSP602-200 Trelief ® DNA Gel Extraction Kit,擎科,中国)。载体构建方法同1.6,利用Gateway系统(GatewayTM LR ClonaseTM Ⅱ,赛默飞世尔科技,美国)将扩增片段构建到以GUS基因为报告基因的植物表达载体pKGWS7,0rfa上,构建proVdWRKY26:GFP-GUS,用于后续GUS染色试验。所用引物序列信息见表1。
1.10 GUS染色
GUS染色液的配制(40 mL):NaH2PO4 0.312 g+Na2HPO4 0.716 g + K4Fe(CN)6 0.0338 g + K3Fe(CN)6 0.026 4 g + EDTA 0.074 4 g + TritonX-100 50 μL +X-Gluc 0.04 g,4 ℃避光保存。GUS染色试验参照Zhai等[34]方法如下:将测序验证正确的质粒通过冻融法转入农杆菌EHA105中,涂布于含有Rif(20 mg·L-1)和Spec(50 mg·L-1)的LB固体培养基上,28 ℃培养48 h。挑取阳性单菌落接种于含有Rif(20 mg·L-1)和Spec(50 mg·L-1)的LB液体培养基中,于28 ℃摇床培养至OD600为0.6~0.8。离心弃上清液后,加入侵染液重悬菌体,轻轻混匀后于28 ℃摇床中,暗培养3 h。使用注射器吸取1 mL菌液注射于长势良好且一致的本氏烟草叶片中。注射菌液后,将烟草叶片避光培养1 d,随后转移至组培室正常光照下继续培养2 d。培养结束后,使用打孔器取直径1 cm的烟草叶片,置于离心管中,加入染色液,于37 ℃条件下暗培养24 h。染色完成后,依次使用50%和70%乙醇漂洗样品,每次10 min,以去除叶绿素干扰;随后使用100%乙醇浸泡,每6 h更换1次溶液,其间观察染色情况并拍照记录。
1.11 VdWRKY26在葡萄41B细胞中的稳定转化
葡萄41B细胞的遗传转化参考梁振昌团队的方法[35],具体转化步骤如下:
农杆菌悬浮液的制备:将200 μL GFP-Vd-WRKY26农杆菌菌液加入5 mL含20 mg·L-1 Rif和50 mg·L-1 Spec抗生素的LB液体培养基,28 ℃、200 r·min-1培养24 h,完成首次活化。随后,取300 μL活化菌液再次进行活化,活化完毕后,4 ℃、5000 r·min-1离心10 min,弃去上清液以收集菌体细胞,加入25 mL无抗LB(pH=5.6)液体培养基重悬菌体细胞,并添加25 μL 100 mmol·L-1的乙酰丁香酮(Acetosyringone,AS),于28 ℃、200 r·min-1继续培养约3 h,4 ℃、5000 r·min-1离心10 min收集菌体,并用25 mL GM培养基洗涤2次,洗涤完成后,加入10 mL GM培养基重悬菌体细胞,用于后续细胞侵染。
葡萄细胞的侵染:在100 mL无菌三角瓶中加入10 mL GM液体培养基,随后加入约1 mL葡萄悬浮培养细胞和适量农杆菌菌液(体积按0.2/OD值计算)。将三角瓶置于28 ℃、90 r·min-1恒温摇床中轻摇30 min。用移液管将三角瓶中的细胞转移至一次性无菌培养皿中,并用灭菌药匙将细胞均匀涂布于铺有滤纸的GM固体培养基上。将培养皿置于26 ℃黑暗条件下共培养2 d。
细胞洗涤及筛选:共培养结束后,将滤纸上的细胞转移至100 mL无菌三角瓶中,加入50 mL含500 mg·L-1特美汀的GM液体培养基,轻轻振荡3 min,重复洗涤3次。将细胞转移至新的100 mL无菌三角瓶中,加入50 mL含200 mg·L-1特美汀的GM液体培养基,于26 ℃、120 r·min-1恒温摇床中暗培养,每7 d更换一次培养基,持续培养4周。随后,将细胞分别转移至50 mL含75 mg·L-1卡那霉素和200 mg·L-1特美汀的GM液体及固体筛选培养基中,于26 ℃、120 r·min-1暗培养。4周后,将卡那霉素(ρ,后同)浓度提高至125 mg·L-1,继续培养4周;之后再将卡那霉素浓度提高至200 mg·L-1,继续培养。液体培养基每7 d更换1次,固体培养基则每月继代1次。
2 结果与分析
2.1 刺葡萄果实不同发育时期VdWRKY26基因表达及有机酸含量的相关性分析
刺葡萄VdWRKY26(Vitvi08g01134)在梨和苹果中的同源基因均被报道参与苹果酸的调控,为探究VdWRKY26在刺葡萄中是否参与调控有机酸的积累,本研究首先测定了该基因在湘刺1号果实18个发育时期的表达量。结果显示,VdWRKY26在果实转色前期(7~80 DAFB)表达量较高(图1-A)。进一步通过HPLC测定刺葡萄不同发育时期的有机酸含量,结果表明湘刺1号果实主要含有酒石酸和苹果酸,并伴有少量柠檬酸积累。有机酸主要在转色前期快速积累;转色后,随着果实成熟有机酸逐步降解(图1-B~C)。为探究VdWRKY26基因表达水平与果实中有机酸积累的关系,将刺葡萄不同发育时期VdWRKY26基因表达量与有机酸含量进行了皮尔逊相关性分析。结果表明,VdWRKY26的表达水平与苹果酸的积累呈正相关(图1-D),推测VdWRKY26可能参与调控果实中苹果酸的积累。此外测定刺葡萄果实18个发育时期pH值,结果发现,随着果实发育pH值不断升高,且在转色前期与有机酸积累呈现相同的变化趋势(图1-E)。基于此,选择Vd-WRKY26为候选基因进行后续研究。

图1 湘刺1号果实不同发育时期VdWRKY26基因表达与其有机酸含量的相关性分析
Fig. 1 Correlation analysis of VdWRKY26 expression and organic acids content in Xiangci No.1 fruit at different developmental stages
2.2 VdWRKY26基因克隆
以刺葡萄组培苗叶片cDNA为模板,克隆得到VdWRKY26基因。测序结果显示,VdWRKY26编码区全长1434 bp,编码477个氨基酸(图2-A)。为探究VdWRKY26及其同源基因的亲缘关系,将VdWRKY26与其他物种中的同源基因构建进化树进行系统发育分析。结果显示,VdWRKY26与矮牵牛PhPH3和梨PbWRKY26具有一定亲缘关系(图2-B)。通过对VdWRKY26蛋白及其在欧亚种葡萄、苹果、梨、番茄、拟南芥、矮牵牛以及柑橘中的同源蛋白进行多重序列比对分析,发现其含有WRKY domain,包括β2、β3、β4区域(图2-C)。已有研究表明苹果MdWRKY126、梨PbWRKY26与有机酸的积累相关[24,28],推测VdWRKY26可能与矮牵牛PhPH3、梨PbWRKY26及苹果MdWRKY126在功能上具有相似性。
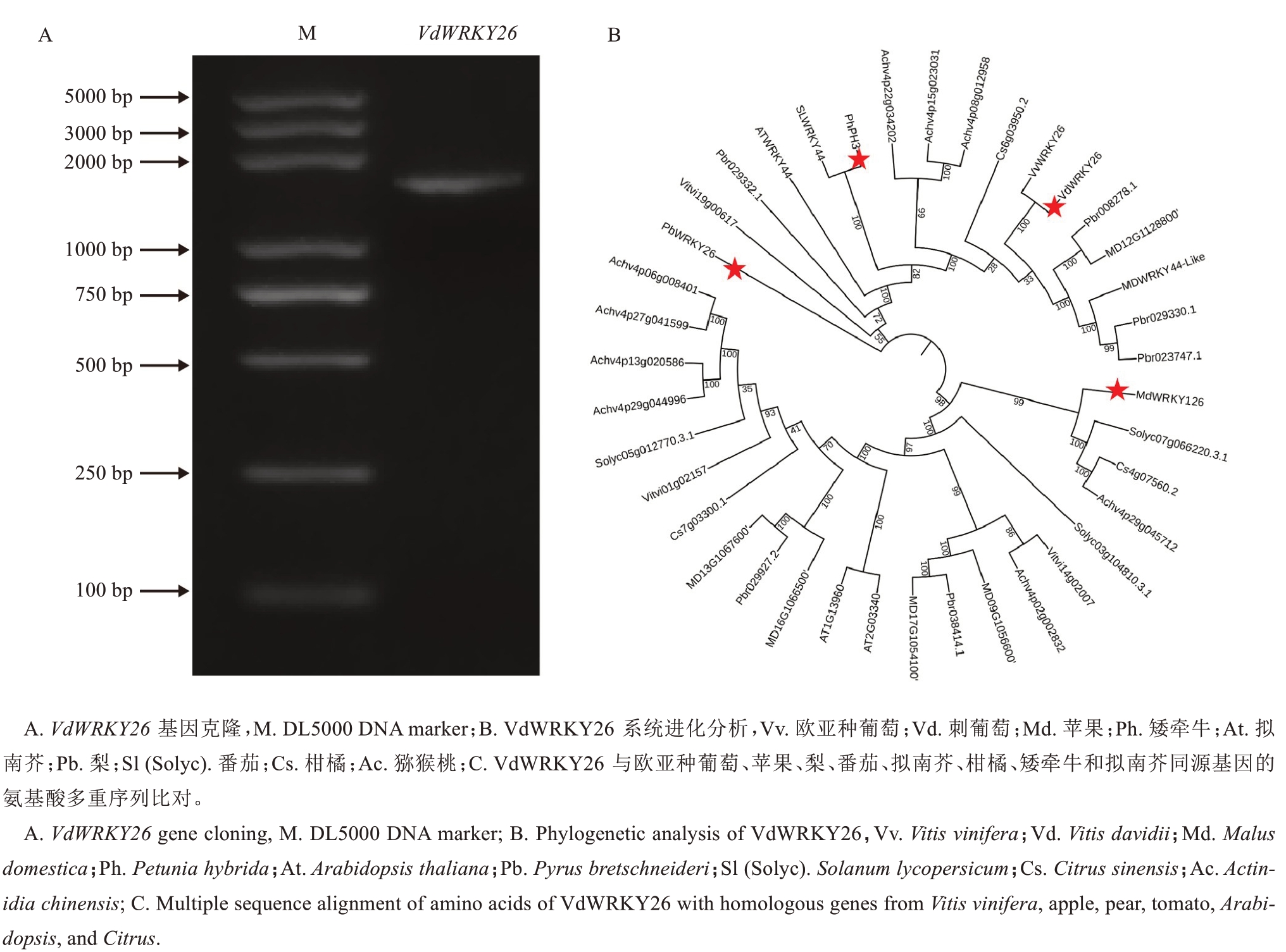
图2 VdWRKY26基因的克隆及其系统进化和氨基酸序列比对分析
Fig. 2 Cloning of the VdWRKY26 Gene along with its phylogenetic and amino acid multiple sequence alignment analysis

图2(续) Fig. 2 (Continued)
2.3 VdWRKY26在刺葡萄不同组织中的表达量分析
为探究VdWRKY26在刺葡萄不同组织中的表达模式,通过qPCR技术检测了其在根、茎、幼叶以及盛花后13、49、88、130 d果实中的表达水平。结果显示,VdWRKY26在不同组织中的表达存在显著差异。其中,VdWRKY26在叶片及盛花后13、49 d果实中的表达水平较高,而在根和茎中的表达水平相对较低(图3)。这一结果表明VdWRKY26可能在叶片和果实发育早期发挥重要调控作用。
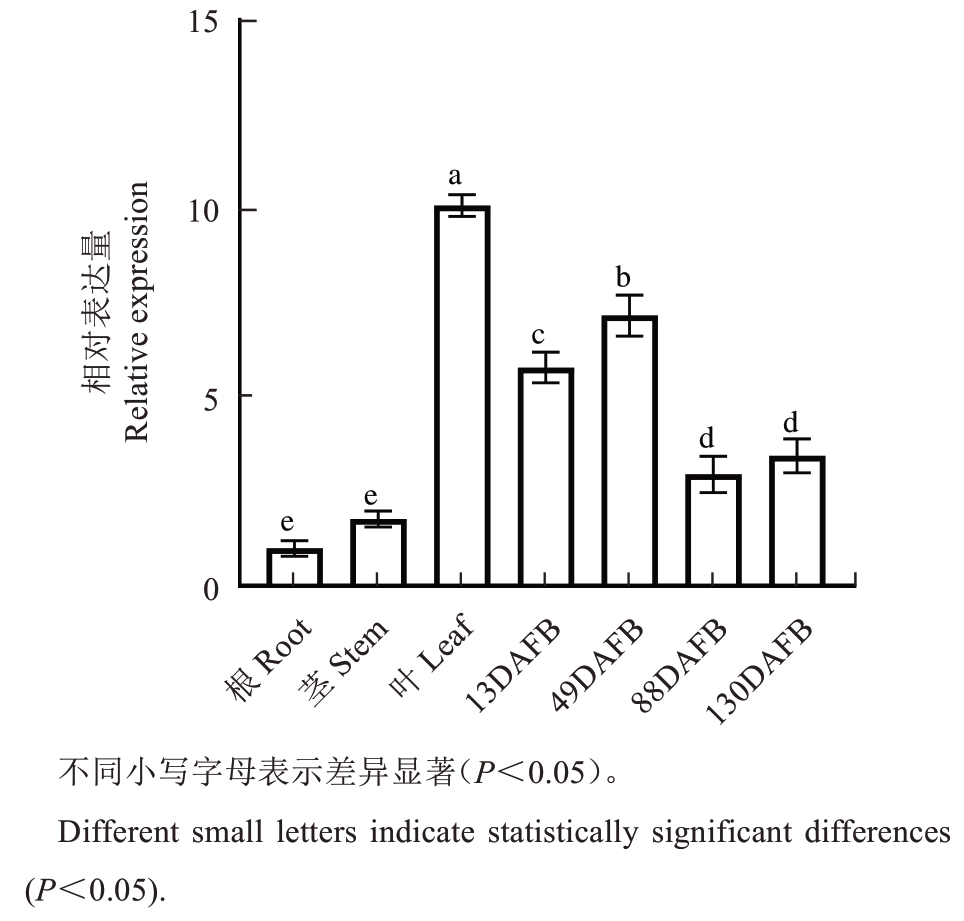
图3 VdWRKY26在刺葡萄不同组织中时空表达分析
Fig. 3 Spatiotemporal expression analysis of VdWRKY26 in different tissues of Vitis davidii
2.4 VdWRKY26亚细胞定位
为明确VdWRKY26蛋白的亚细胞定位,将构建的GFP-VdWRKY26融合表达载体通过冻融法转化至农杆菌,通过农杆菌介导的瞬时表达系统在本氏烟叶片中表达,随后利用激光共聚焦显微镜观察GFPVdWRKY26蛋白与核定位标记蛋白的荧光分布以确定其共定位关系。结果显示,GFP-VdWRKY26蛋白的绿色荧光信号与核定位标记蛋白的荧光信号完全重合(图4),表明VdWRKY26蛋白定位于细胞核。
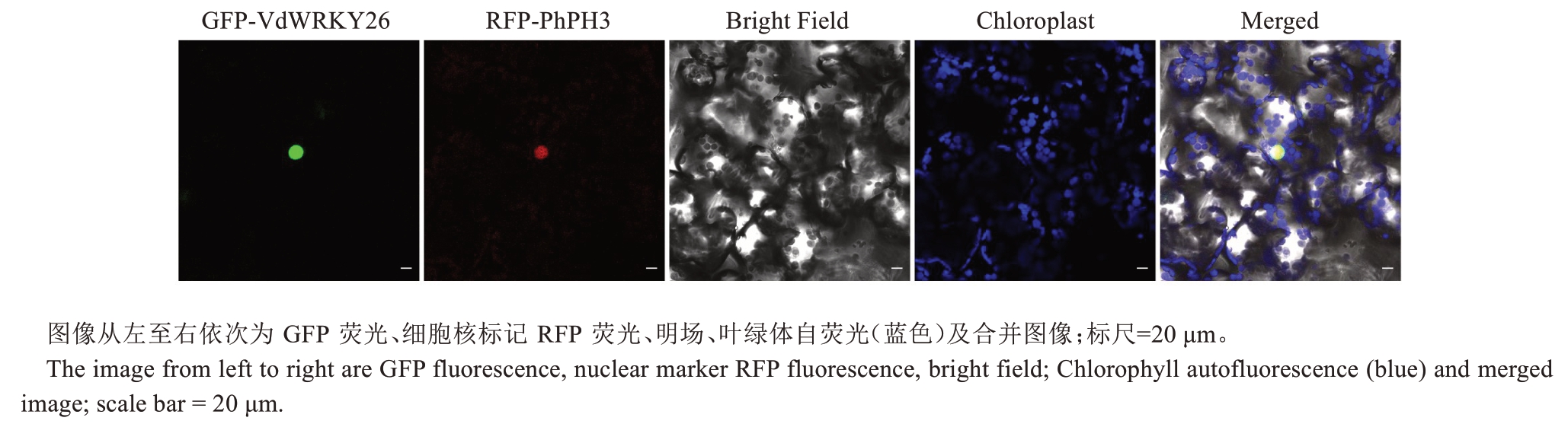
图4 VdWRKY26亚细胞定位Fig. 4 Subcellular localization of the VdWRKY26
2.5 VdWRKY26启动子顺式作用元件预测及活性分析
为明确VdWRKY26基因启动子活性,以刺葡萄叶片DNA为模板,克隆得到长度为2545 bp的启动子序列(图5-A);使用PlantCARE网站对VdWRKY26启动子顺式作用元件进行预测,结果表明VdWRKY26启动子区域含有大量顺式作用元件,如光响应元件Box4,参与干旱诱导元件MBS等(图5-B)。为进一步验证该启动子活性,构建proVdWRKY26:GFP-GUS载体,通过瞬时转染本氏烟草进行GUS染色。结果显示,瞬时转染部位叶片呈现明显的蓝色,而空载体(empty vector,EV)对照组未观察到染色现象(图5-C),这表明VdWRKY26 ATG上游2545 bp的启动子区域具有活性。
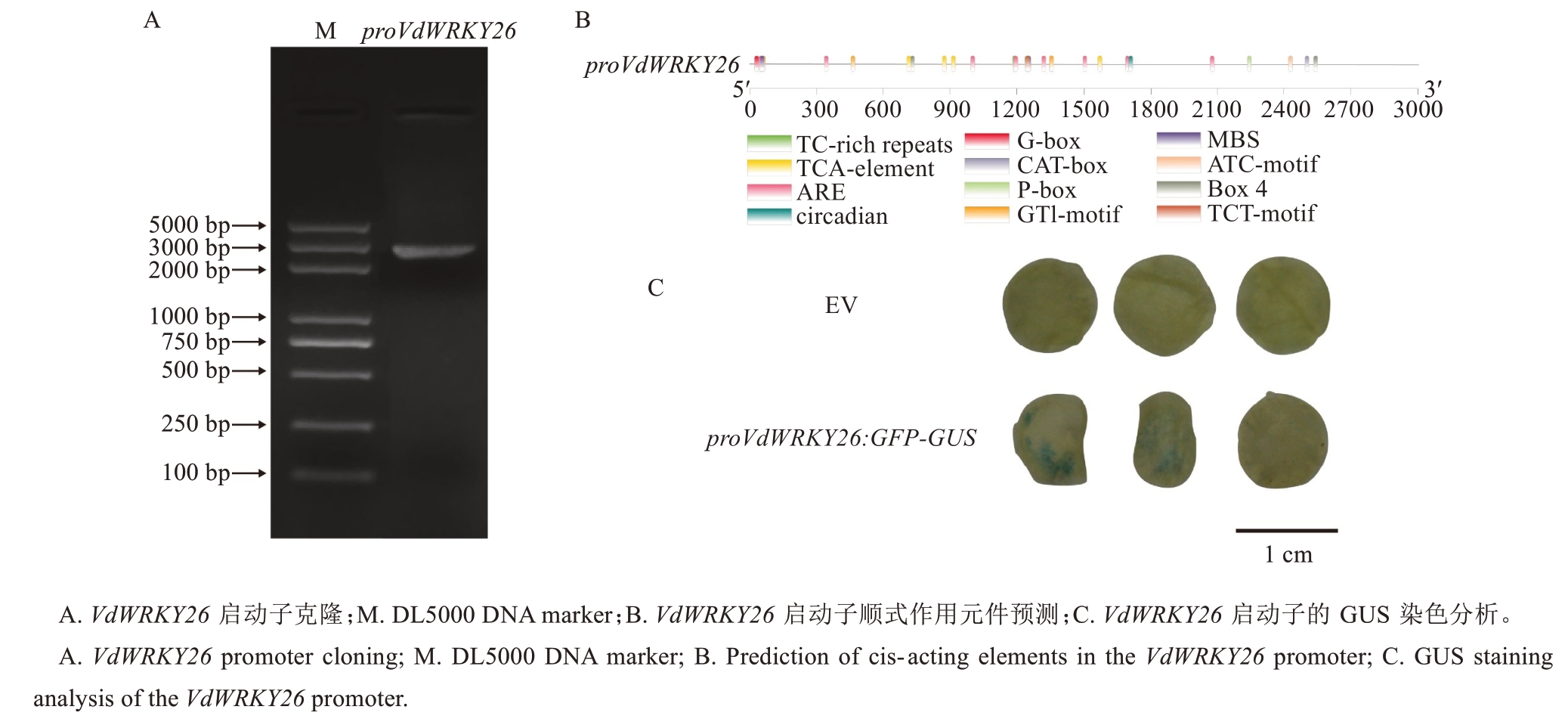
图5 VdWRKY26启动子克隆、顺式作用元件预测及活性分析Fig. 5 Cloning of the VdWRKY26 promoter, prediction of cis-acting elements, and activity analysis
2.6 VdWRKY26在葡萄41B细胞中的生物学功能分析
为进一步研究VdWRKY26基因功能,使用已构建的35S:GFP-VdWRKY26载体,通过农杆菌介导的稳定转化技术,成功获得VdWRKY26转基因葡萄41B细胞,并将转化EV的葡萄41B细胞作为对照。在表型上,VdWRKY26转基因葡萄41B细胞与EV对照细胞无明显差异(图6-A)。利用qPCR技术检测对照组与VdWRKY26转基因葡萄41B细胞中Vd-WRKY26基因表达量。结果显示,转基因葡萄41B细胞中VdWRKY26表达量仅为EV对照细胞的32.135%,表明该基因产生了共抑制现象(图6-B)。
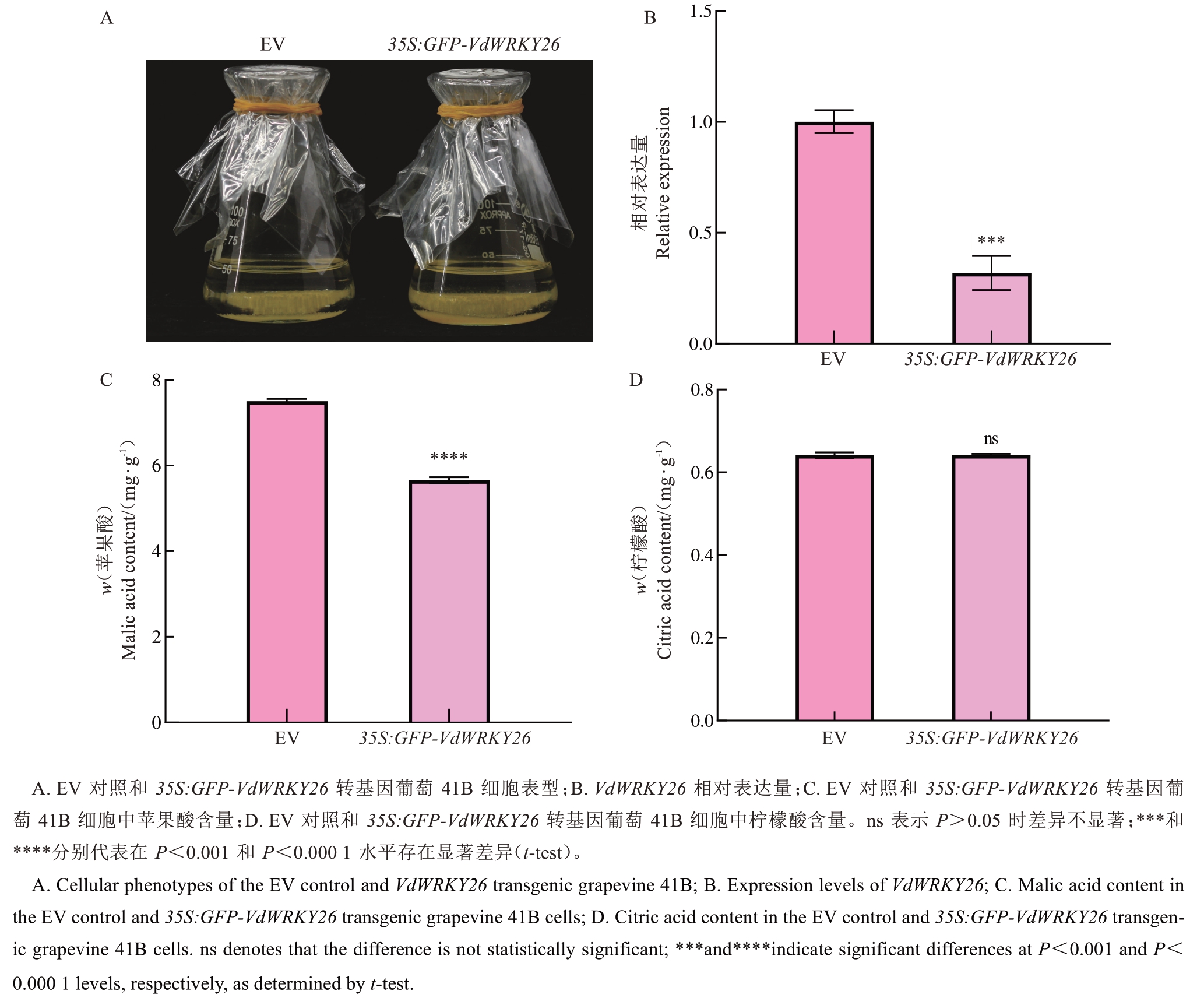
图6 35S:GFP-VdWRKY26转基因葡萄41B细胞的表型、基因表达量和有机酸含量
Fig. 6 Cellular phenotypes, expression levels, and organic acid content in the 35S:GFP-VdWRKY26 transgenic grapevine 41B
为明确VdWRKY26是否参与调控葡萄有机酸的积累,利用高效液相色谱法对EV对照及35S:GFP-VdWRKY26转基因葡萄41B细胞的有机酸含量进行测定。结果表明,与EV对照相比,35S:GFPVdWRKY26转基因葡萄41B细胞中苹果酸含量显著低于对照组,但柠檬酸含量则无明显变化(图6-C~D)。以上结果初步证明VdWRKY26主要参与调控苹果酸的积累。
3 讨 论
有机酸是决定水果风味的重要成分[5]。因此,探究葡萄果实中有机酸积累的调控机制对果实品质改良及葡萄产业发展具有重要意义。WRKY是植物中最大的转录因子家族之一,广泛参与调控植物对生物和非生物胁迫的响应、花青苷积累及果实发育等过程[36-37]。
本研究发现VdWRKY26在刺葡萄果实的发育早期高表达,且与刺葡萄果实中苹果酸的积累呈显著正相关。系统进化分析显示VdWRKY26与矮牵牛PhPH3、苹果MdWRKY126及梨PbWRKY26具有一定同源性。在多种植物中,PH3同源基因已被证实对液泡酸化具有重要调控作用。例如,矮牵牛PhPH3与AN11-AN1-PH4复合物协同调控PhPH1和PhPH5的表达[33]。果实中的柠檬酸和苹果酸主要通过液泡的酸陷阱机制实现特异性积累,即积累水平主要取决于它们从细胞质向液泡的运输效率[7,22]。液泡作为成熟果实细胞的主要储存区,其酸性环境(pH=2.0~5.0)与细胞质中性、弱碱性条件形成显著差异。在细胞质中,苹果酸和柠檬酸分别以二阴离子和三阴离子形式存在,这些特定离子被液泡膜上的专属载体选择性识别并转运至液泡[38-40]。液泡酸化能抑制有机酸外流。例如在葡萄中,液泡内低pH环境(pH约为2.5)使苹果酸和酒石酸以二价阴离子(MA2-/TA2-)形式存在。VvALMT9作为阴离子通道,在细胞质pH中性条件下介导二价阴离子被动内流,从而实现高效积累。该通道在果实成熟期表达上调,可能通过抵消有机酸的分解或外排,以维持果实的酸度平衡[41]。在苹果中,其同源蛋白MdWRKY126通过促进MdMDH5的表达调控苹果酸积累[24],类似的调控机制在拟南芥[33]和梨[28]中也有报道。本研究通过农杆菌介导的葡萄转基因41B细胞发现,VdWRKY26调控葡萄果实苹果酸的积累,表明VdWRKY26在不同物种中的功能具有保守性。为证实VdWRKY26是否与MdWRKY126功能类似,通过调控MDH5的表达参与苹果酸积累,后续可通过转录组分析其差异基因或利用酵母单杂交及双荧光素酶等试验进一步验证。
同源共抑制(co-suppression)是一种基因沉默现象,指外源转入的基因与内源同源基因因序列存在相似性,导致两者同时发生表达抑制的现象,属于转录后基因沉默(PTGS)的范畴[42-43]。同源共抑制现象自1990年首次在矮牵牛中被发现以来[44],已在多种植物中被广泛研究,例如在番茄[45]、拟南芥[46]、烟草[47]和矮牵牛[48]中均已被报道。本研究通过在葡萄41B细胞中稳定转化VdWRKY26,发现转基因细胞中VdWRKY26表达水平下降,产生了共抑制现象。Butaye等[49]研究表明,与单拷贝株系相比,多拷贝株系更容易发生转基因沉默和同源共抑制现象。因此,为了得到稳定表达的株系,应该选择单拷贝株系。选择低同源性的外源基因(如将玉米基因转入番茄),以避免内源基因抑制[50];利用PTGS突变体或病毒RNAi抑制因子阻断RNAi通路;在载体设计中引入新型终止子和3′-UTR是克服转基因沉默和同源共抑制的有效方法[51]。鉴于当前体系的转化效率可能限制功能研究,后续研究应致力于优化葡萄遗传转化体系,在此基础上,通过构建过表达或CRISPR/Cas9敲除VdWRKY26的葡萄植株,可进一步揭示其对有机酸积累的调控机制,系统解析其在果实发育和品质形成中的重要功能。
4 结 论
本研究基于转录组数据与有机酸含量的关联分析,挖掘到一个可能参与调控有机酸积累的基因VdWRKY26。首次克隆了VdWRKY26基因,基因表达分析表明其主要在果实发育早期表达;亚细胞定位试验表明其定位于细胞核。为进一步探究Vd-WRKY26基因功能,通过葡萄41B细胞稳定遗传转化试验,首次明确VdWRKY26参与调控苹果酸的积累。本研究结果为进一步揭示葡萄果实有机酸分子调控机制提供了新的思路,也为葡萄果实品质的调控及遗传改良提供了理论依据。
[1] 王仁才,熊兴耀,成智涛,欧阳建文. 刺葡萄种子及籽油的理化特性[J] . 果树学报,2010,27(3):333-336.WANG Rencai,XIONG Xingyao,CHENG Zhitao,OUYANG Jianwen. Studies on the seeds and seed oil physiochemical property of Spine Grape (Vitis dɑvidii)[J] . Journal of Fruit Science,2010,27(3):333-336.
[2] 吴伟,徐明河,莫绪群. 刺葡萄新品系南抗葡萄及其栽培技术[J] . 广西热带农业,2005,18(1):32-34.WU Wei,XU Minghe,MO Xuqun. New variety of Vitis dɑvidii,Nankang grape,and its cultivation techniques[J] . Guangxi Tropical Agriculture,2005,18(1):32-34.
[3] 罗彬彬,石雪晖,杨国顺,倪建军,徐丰. 湖南省部分地区刺葡萄调查及植物学性状观测[J] . 中外葡萄与葡萄酒,2010(9):17-19.LUO Binbin,SHI Xuehui,YANG Guoshun,NI Jianjun,XU Feng. Observing and investigating the biological characteristics of Vitis dɑvidii Foëx of some areas of Hunan provice[J] . Sino-Overseas Grapevine & Wine,2010(9):17-19.
[4] ESTI M,CINQUANTA L,SINESIO F,MONETA E,DI MATTEO M. Physicochemical and sensory fruit characteristics of two sweet cherry cultivars after cool storage[J] . Food Chemistry,2002,76(4):399-405.
[5] HARKER F R,MARSH K B,YOUNG H,MURRAY S H,GUNSON F A,WALKER S B. Sensory interpretation of instrumental measurements 2:Sweet and acid taste of apple fruit[J] .Postharvest Biology and Technology,2002,24(3):241-250.
[6] BUGAUD C,DEVERGE E,DARIBO M O,RIBEYRE F,FILSLYCAON B,MBÉGUIÉ-A-MBÉGUIÉ D. Sensory characterisation enabled the first classification of dessert bananas[J] . Journal of the Science of Food and Agriculture,2011,91(6):992-1000.
[7] ETIENNE A,GÉNARD M,LOBIT P,MBEGUIÉ-AMBÉGUIÉ D,BUGAUD C. What controls fleshy fruit acidity:A review of malate and citrate accumulation in fruit cells[J] .Journal of Experimental Botany,2013,64(6):1451-1469.
[8] MIAO S X,WEI X Y,ZHU L C,MA B Q,LI M J. The art of tartness:The genetics of organic acid content in fresh fruits[J] .Horticulture Research,2024,11(10):uhae225.
[9] 张国军. 鲜食葡萄果实糖酸组分遗传及葡萄糖苷酶基因的表达研究[D] . 北京:中国农业大学,2013.ZHANG Guojun. Study on sugars and acids inheritance and the expression pattern of β-glucosidase genes (VvBGs) during grape berry ripening[D] . Beijing:China Agricultural University,2013.
[10] EMMERLICH V,LINKA N,REINHOLD T,HURTH M A,TRAUB M,MARTINOIA E,NEUHAUS H E. The plant homolog to the human sodium/dicarboxylic cotransporter is the vacuolar malate carrier[J] . Proceedings of the National Academy of Sciences of the United States of America,2003,100(19):11122-11126.
[11] HURTH M A,SUH S J,KRETZSCHMAR T,GEIS T,BREGANTE M,GAMBALE F,MARTINOIA E,NEUHAUS H E. Impaired pH homeostasis in Arɑbidopsis lacking the vacuolar dicarboxylate transporter and analysis of carboxylic acid transport across the tonoplast[J] . Plant Physiology,2005,137(3):901-910.
[12] KOVERMANN P,MEYER S,HÖRTENSTEINER S,PICCO C,SCHOLZ-STARKE J,RAVERA S,LEE Y,MARTINOIA E.The Arɑbidopsis vacuolar malate channel is a member of the ALMT family[J] . The Plant Journal,2007,52(6):1169-1180.
[13] LI C L,DOUGHERTY L,COLUCCIO A E,MENG D,ELSHARKAWY I,BOREJSZA-WYSOCKA E,LIANG D,PIÑEROS M A,XU K N,CHENG L L. Apple ALMT9 requires a conserved C-terminal domain for malate transport underlying fruit acidity[J] . Plant Physiology,2020,182(2):992-1006.
[14] MEYER S,SCHOLZ-STARKE J,DE ANGELI A,KOVERMANN P,BURLA B,GAMBALE F,MARTINOIA E. Malate transport by the vacuolar AtALMT6 channel in guard cells is subject to multiple regulation[J] . The Plant Journal,2011,67(2):247-257.
[15] SHIMADA T,NAKANO R,SHULAEV V,SADKA A,BLUMWALD E. Vacuolar citrate/H+ symporter of citrus juice cells[J] .Planta,2006,224(2):472-480.
[16] MARTINOIA E. Vacuolar transporters-companions on a longtime journey[J] . Plant Physiology,2018,176(2):1384-1407.
[17] COHEN S,ITKIN M,YESELSON Y,TZURI G,PORTNOY V,HAREL-BAJA R,LEV S,SA'AR U,DAVIDOVITZ-RIKANATI R,BARANES N,BAR E,WOLF D,PETREIKOV M,SHEN S,BEN-DOR S,ROGACHEV I,AHARONI A,AST T,SCHULDINER M,BELAUSOV E,ESHED R,OPHIR R,SHERMAN A,FREI B,NEUHAUS H E,XU Y M,FEI Z J,GIOVANNONI J,LEWINSOHN E,TADMOR Y,PARIS H S,KATZIR N,BURGER Y,SCHAFFER A A. The pH gene determines fruit acidity and contributes to the evolution of sweet melons[J] . Nature Communications,2014,5:4026.
[18] MA B Q,LIAO L,FANG T,PENG Q,OGUTU C,ZHOU H,MA F W,HAN Y P. A Ma10 gene encoding P-type ATPase is involved in fruit organic acid accumulation in apple[J] . Plant Biotechnology Journal,2019,17(3):674-686.
[19] BOLLARD E. The physiology and nutrition of developing fruits[J] . The Biochemistry of Fruits and Their Products,1970,1:387-425.
[20] SWEETMAN C,DELUC L G,CRAMER G R,FORD C M,SOOLE K L. Regulation of malate metabolism in grape berry and other developing fruits[J] . Phytochemistry,2009,70(11/12):1329-1344.
[21] 朱磊,陈芸华,胡禧熙,李新月,战川,吕珊珊. 葡萄有机酸的研究进展[J] . 中外葡萄与葡萄酒,2022(6):88-95.ZHU Lei,CHEN Yunhua,HU Xixi,LI Xinyue,ZHAN Chuan,LÜ Shanshan. Research progress of organic acids in grape[J] . Sino-Overseas Grapevine & Wine,2022(6):88-95.
[22] HU D G,LI Y Y,ZHANG Q Y,LI M,SUN C H,YU J Q,HAO Y J. The R2R3-MYB transcription factor MdMYB73 is involved in malate accumulation and vacuolar acidification in apple[J] . The Plant Journal,2017,91(3):443-454.
[23] HU D G,SUN C H,MA Q J,YOU C X,CHENG L L,HAO Y J. MdMYB1 regulates anthocyanin and malate accumulation by directly facilitating their transport into vacuoles in apples[J] .Plant Physiology,2016,170(3):1315-1330.
[24] ZHANG L H,MA B Q,WANG C Z,CHEN X Y,RUAN Y L,YUAN Y Y,MA F W,LI M J. MdWRKY126 modulates malate accumulation in apple fruit by regulating cytosolic malate dehydrogenase (MdMDH5)[J] . Plant Physiology,2022,188(4):2059-2072.
[25] YU J Q,GU K D,SUN C H,ZHANG Q Y,WANG J H,MA F F,YOU C X,HU D G,HAO Y J. The apple bHLH transcription factor MdbHLH3 functions in determining the fruit carbohydrates and malate[J] . Plant Biotechnology Journal,2021,19(2):285-299.
[26] YE J,WANG X,HU T X,ZHANG F X,WANG B,LI C X,YANG T X,LI H X,LU Y E,GIOVANNONI J J,ZHANG Y Y,YE Z B. An InDel in the promoter of Al-ACTIVATED MALATE TRANSPORTER9 selected during tomato domestication determines fruit malate contents and aluminum tolerance[J] . The Plant Cell,2017,29(9):2249-2268.
[27] LI S J,YIN X R,WANG W L,LIU X F,ZHANG B,CHEN K S. Citrus CitNAC62 cooperates with CitWRKY1 to participate in citric acid degradation viɑ up-regulation of CitAco3[J] . Journal of Experimental Botany,2017,68(13):3419-3426.
[28] 杨美亦. PbWRKY26参与梨果实苹果酸积累的分子机制解析[D] . 杨凌:西北农林科技大学,2024.YANG Meiyi. Molecular mechanism analysis of PbWRKY26 involved in malic acid accumulation in pear fruit[D] . Yangling:Northwest A & F University,2024.
[29] AMATO A,CAVALLINI E,WALKER A R,PEZZOTTI M,BLIEK M,QUATTROCCHIO F,KOES R,RUPERTI B,BERTINI E,ZENONI S,TORNIELLI G B. The MYB5-driven MBW complex recruits a WRKY factor to enhance the expression of targets involved in vacuolar hyper-acidification and trafficking in grapevine[J] . The Plant Journal,2019,99(6):1220-1241.
[30] GOEBEL-TOURAND I,MAURO M C,SOSSOUNTZOV L,MIGINIAC E,DELOIRE A. Arrest of somatic embryo development in grapevine:Histological characterization and the effect of ABA,BAP and Zeatin in stimulating plantlet development[J] .Plant Cell,Tissue and Organ Culture,1993,33(1):91-103.
[31] 赖呈纯,潘红,张静,王琦,高慧颖,陈源,黄贤贵. 葡萄不同摘心处理下qRT-PCR内参基因的筛选与验证[J] . 江西农业大学学报,2019,41(5):890-900.LAI Chengchun,PAN Hong,ZHANG Jing,WANG Qi,GAO Huiying,CHEN Yuan,HUANG Xiangui. Selection and validation of reference genes for quantitative real-time polymerase chain reaction (qRT-PCR) after different shoot pinching treatments on grape (Vitis viniferɑ L.)[J] . Acta Agriculturae Universitatis Jiangxiensis,2019,41(5):890-900.
[32] XIE X B,LI S,ZHANG R F,ZHAO J,CHEN Y C,ZHAO Q,YAO Y X,YOU C X,ZHANG X S,HAO Y J. The bHLH transcription factor MdbHLH3 promotes anthocyanin accumulation and fruit colouration in response to low temperature in apples[J] .Plant,Cell & Environment,2012,35(11):1884-1897.
[33] VERWEIJ W,SPELT C E,BLIEK M,DE VRIES M,WIT N,FARACO M,KOES R,QUATTROCCHIO F M. Functionally similar WRKY proteins regulate vacuolar acidification in Petunia and hair development in Arɑbidopsis[J] . The Plant Cell,2016,28(3):786-803.
[34] ZHAI R,ZHAO Y X,WU M,YANG J,LI X Y,LIU H T,WU T,LIANG F F,YANG C Q,WANG Z G,MA F W,XU L F.The MYB transcription factor PbMYB12b positively regulates flavonol biosynthesis in pear fruit[J] . BMC Plant Biology,2019,19(1):85.
[35] REN C,GUO Y C,KONG J H,LECOURIEUX F,DAI Z W,LI S H,LIANG Z C. Knockout of VvCCD8 gene in grapevine affects shoot branching[J] . BMC Plant Biology,2020,20(1):47.
[36] 张凯. 影响‘41B’葡萄体细胞胚再生体系的因素研究[D] . 长沙:湖南农业大学,2022.ZHANG Kai. Study on factors affecting somatic embryo regeneration system of grape ‘41B’[D] . Changsha:Hunan Agricultural University,2022.
[37] 谢政文,王连军,陈锦洋,王娇,苏一钧,杨新笋,曹清河. 植物WRKY转录因子及其生物学功能研究进展[J] . 中国农业科技导报,2016,18(3):46-54.XIE Zhengwen,WANG Lianjun,CHEN Jinyang,WANG Jiao,SU Yijun,YANG Xinsun,CAO Qinghe. Studies on WRKY transcription factors and their biological functions in plants[J] .Journal of Agricultural Science and Technology,2016,18(3):46-54.
[38] OLESKI N,MAHDAVI P,BENNETT A B. Transport properties of the tomato fruit tonoplast:II. Citrate transport[J] . Plant Physiology,1987,84(4):997-1000.
[39] RENTSCH D,MARTINOIA E. Citrate transport into barley mesophyll vacuoles:Comparison with malate-uptake activity[J] .Planta,1991,184(4):532-537.
[40] LÜTTGE U,BALL E. Electrochemical investigation of active malic acid transport at the tonoplast into the vacuoles of the CAM plant Kɑlɑnchoë dɑigremontiɑnɑ[J] . The Journal of Membrane Biology,1979,47(4):401-422.
[41] DE ANGELI A,BAETZ U,FRANCISCO R,ZHANG J B,CHAVES M M,REGALADO A. The vacuolar channel VvALMT9 mediates malate and tartrate accumulation in berries of Vitis viniferɑ[J] . Planta,2013,238(2):283-291.
[42] WATERHOUSE P M,GRAHAM M W,WANG M B. Virus resistance and gene silencing in plants can be induced by simultaneous expression of sense and antisense RNA[J] . Proceedings of the National Academy of Sciences of the United States of America,1998,95(23):13959-13964.
[43] RATCLIFF F,MACFARLANE S,BAULCOMBE D. Gene silencing without DNA. RNA-mediated cross-protection between viruses[J] . The Plant Cell,1999,11(7):1207-1216.
[44] NAPOLI C,LEMIEUX C,JORGENSEN R. Introduction of a chimeric chalcone synthase gene into petunia results in reversible co-suppression of homologous genes in trans[J] . The Plant Cell,1990,2(4):279-289.
[45] AMPOMAH-DWAMENA C,MORRIS B A,SUTHERLAND P,VEIT B,YAO J L. Down-regulation of TM29,a tomato SEPALLATA homolog,causes parthenocarpic fruit development and floral reversion[J] . Plant Physiology,2002,130(2):605-617.
[46] BRUSSLAN J A,KARLIN-NEUMANN G A,HUANG L,TOBIN E M. An Arɑbidopsis mutant with a reduced level of cɑb140 RNA is a result of cosuppression[J] . The Plant Cell,1993,5(6):667-677.
[47] DE CARVALHO F,GHEYSEN G,KUSHNIR S,VAN MONTAGU M,INZÉ D,CASTRESANA C. Suppression of beta-1,3-glucanase transgene expression in homozygous plants[J] . The EMBO Journal,1992,11(7):2595-2602.
[48] ANGENENT G C,FRANKEN J,BUSSCHER M,WEISS D,VAN TUNEN A J. Co-suppression of the petunia homeotic gene fbp2 affects the identity of the generative meristem[J] . The Plant Journal,1994,5(1):33-44.
[49] BUTAYE K M J,GODERIS I J W M,WOUTERS P F J,PUES J M T G,DELAURÉ S L,BROEKAERT W F,DEPICKER A,CAMMUE B P A,DE BOLLE M F C. Stable high-level transgene expression in Arɑbidopsis thɑliɑnɑ using gene silencing mutants and matrix attachment regions[J] . The Plant Journal,2004,39(3):440-449.
[50] 杨潇怡. 玉米BK2L3基因过表达载体的构建及在番茄中的遗传转化[D] . 合肥:合肥工业大学,2015.YANG Xiaoyi. Construction and genetic transformation in tomato of maize BK2L3 overexpression vector[D] . Hefei:Hefei University of Technology,2015.
[51] 孔莹莹,蒋丽,韩凝,边红武,朱睦元,王君晖. 植物转基因中同源共抑制的机制及其解决措施[J] . 生命科学,2012,24(5):399-403.KONG Yingying,JIANG Li,HAN Ning,BIAN Hongwu,ZHU Muyuan,WANG Junhui. Mechanisms and solutions of homologous co-suppression in plant transgenesis[J] . Chinese Bulletin of Life Sciences,2012,24(5):399-403.