作为基因表达的核心调控元件,转录因子(transcription factor,TF)通过特异性识别并结合靶基因启动子区域的顺式作用元件,精确调控下游基因的转录与表达[1]。这类调控蛋白能在特定时空维度上动态激活或抑制下游靶基因,广泛参与调控植物生长发育、形态建成、果实成熟以及生物与非生物胁迫响应等关键生物学过程[1-2]。目前,植物界已鉴定出56个转录因子家族[2],包括NAC[3]、AP2/ERF[4]、WRKY[5]、MYB[6]、bHLH[7]、bZIP[8]、BBX[9]、MADSBox[10]和DOF[11]等,构成了复杂的基因调控网络。
AP2/ERF超家族是一类具有典型AP2保守结构域的植物特异性转录因子,其结构域含有60~70个氨基酸残基,由1个β-折叠和与之平行的α-螺旋组成。根据结构域的数量和特征,该家族可分为:(1)AP2(含2个AP2结构域);(2)DREB(含1个AP2结构域,第14和19位残基分别是缬氨酸Val和谷氨酸Glu);(3)ERF(含1个AP2结构域,第14和19位残基分别是丙氨酸Ala和天冬氨酸Asp);(4)RAV(含1个AP2结构域和1个B3结构域);(5)Soloist(含1个具有独特序列特征的AP2结构域)[4,12]。其中,AP2亚家族基于其核定位和氨基酸序列以及其他保守基序可以进一步分为三个进化分支euAP2、basalANT和euANT[13-14]。AP2/ERF家族成员通过与其他调控元件相互作用形成精密调控网络[15],既能作为转录激活因子又可行使抑制功能,动态协调植物生长与环境适应之间的平衡[16-17]。这种双重调控特性,加之其在胁迫响应中的核心作用,使AP2/ERF转录因子成为现代农业研究的热点和作物遗传改良的重要靶标[18]。
AP2亚家族通过调控花器官发育、胚胎发生、分生组织分化和叶片形态建成等关键生物学过程,在植物发育调控网络中展现出显著的多效性。模式植物拟南芥(Arɑbidopsis thɑliɑnɑ)中AP2基因被证实是决定花器官身份和调控重瓣花形成的核心调控因子[19]。Han等[20]发现月季(Rosɑ chinensis)中RcAP2基因的表达具有温度响应特性,表现为低温诱导、高温抑制;在拟南芥中异源过表达RcAP2后引起雄蕊瓣化现象,表明该基因可能作为温度信号与花器官发育的分子调控枢纽。BBM基因隶属于AINTEGUMENTA-LIKE(AIL)亚家族,是AP2/ERF转录因子家族中研究最为深入的成员之一。该基因最初在甘蓝型油菜(Brɑssicɑ nɑpus)中被鉴定,其显著功能是能够高效诱导体细胞胚胎发生(somatic embryogenesis)[21]。后续跨物种研究进一步揭示了BBM基因的多重生物学功能,包括促进体细胞胚胎发生[22]、提高遗传转化效率[23-24]和诱导无融合生殖[25]等。这些重要发现确立了BBM基因作为胚胎发育特异性分子标记和植物再生调控核心因子的重要地位。研究表明,在苹果中过表达转录因子MdAIL5可显著提高再生效率,其中叶片不定芽的再生效率提高4~6倍,不定根再生效率提高3~5倍,证实该基因是调控器官再生的关键基因[26]。拟南芥ANT和AIL6基因直接参与调控花的早期发育过程,其功能包括特化花器官的身份决定、植物生长调控以及维管系统发育等[27]。
李(Prunus sɑlicinɑ Lindl.)是蔷薇科李属的重要落叶果树,在我国具有广泛的栽培分布和重要经济价值[28]。其种植区域横跨我国南北,生态适应性极强。南至热带季风气候的西双版纳,北达寒温带的黑龙江沿岸,东至台湾省,西抵青藏高原边缘地区[29]。然而,目前关于李AP2基因家族的系统研究仍属空白。笔者基于3个代表性栽培品种三月李(Sanyueli)[30]、中李6号(Zhongli No. 6)[31]和巫山脆李(Wushancuili)[32]的参考基因组数据,利用生物信息学技术,筛选并鉴定出李AP2转录因子家族成员。系统分析李AP2家族成员的理化性质、基因结构、保守基序、染色体定位等特征,构建系统进化树,解析亚家族进化关系,并利用qRT-PCR技术分析了李AP2基因家族成员的组织特异性表达模式,旨在为后续深入解析李AP2基因家族的功能奠定基础。
1 材料和方法
1.1 数据来源
分别从拟南芥基因组数据库The Arabidopsis Information Resource(TAIR,https://www.arabidopsis.org)、蔷薇科基因组数据库Genome Database for Rosaceae(GDR,https://www.rosaceae.org/)和梨基因组数据库Pear Genome Database(PGDB,http://pyrusgdb.sdau.edu.cn/)中获取拟南芥、苹果(Mɑlus domesticɑ)、砀山酥梨(Pyrus bretschneideri)AP2基因家族成员的蛋白质序列。从GDR中下载三月李[30]、中李6号[31]和巫山脆李[32]基因组数据,包括全基因序列、蛋白质序列、基因组注释文件。三月李是源自我国南方地区的早熟黄肉李品种,是一个重要的地方栽培种;中李6号是由中国农业科学院郑州果树研究所自主选育的特色中国李品种;巫山脆李作为西南地区特色青脆李的典型代表,是从地方种江安大白李中选育出的优良品种。选择这3个品种正是基于它们在果实关键性状、生态适应性方面具有代表性差异。
1.2 李AP2基因家族成员筛选与鉴定、理化性质分析和亚细胞定位预测
以从TAIR数据库获取的14个拟南芥AP2蛋白序列作为参考,利用TBtools软件(v1.108)对三月李、中李6号和巫山脆李全基因组蛋白数据库进行Blastp同源比对(E-value<1e-5),初步筛选候选基因。随后,通过SMART在线工具(http://smart.embl.de)进行结构域验证,筛选出含有2个完整AP2保守结构域的基因,剔除结构域不完整或异常的假基因,最终获得3个品种的AP2家族成员:SYPsAP2(三月李)、WSPsAP2(巫山脆李)和ZLPsAP2(中李6号)。使用TBtools(v1.108)计算各家族成员的氨基酸残基数、分子质量(MW)、理论等电点(pI)、不稳定系数(II)和平均亲水性(GRAVY)等理化性质。采用Plant-mPLoc在线工具(http://www.csbio.sjtu.edu.cn/bioinf/plant-multi/)进行亚细胞定位预测,选用植物特异性预测模型,考虑所有可能的亚细胞定位,置信度阈值设置为70%以上。
1.3 李AP2基因家族成员系统发育树构建
整合三月李、中李6号和巫山脆李鉴定到的AP2家族成员蛋白序列,并选取拟南芥及蔷薇科重要果树苹果和梨的AP2家族成员同源序列作为参考序列,使用ClustalW(v2.0.11)进行多序列比对,以确保序列比对的准确性。基于比对结果,采用MEGA11软件(v11.0.13)构建系统进化树,选择邻接法(neighbor-joining method)作为建树方法,设置Bootstrap重复次数为1000次以评估节点支持度,并删除50%同源差异较大的序列以提高建树准确性。利用iTOL在线平台(https://itol.embl.de/)对进化树进行可视化优化,包括分支着色、节点标注等。参考拟南芥AP2基因家族已知的标准分类体系(euAP2、basalANT和euANT等亚族)对李AP2基因家族进行亚族分类。
1.4 李AP2基因家族成员的染色体定位与共线性分析
基于三月李、中李6号和巫山脆李的基因组注释文件,采用TBtools软件(v1.108)对AP2基因家族成员进行系统分析。首先,通过染色体定位可视化分析,确定各AP2基因在染色体上的物理位置,并按照其在染色体上的分布顺序对3个品种的AP2基因进行系统命名(SYPsAP2-n、ZLPsAP2-n和WSPsAP2-n)。随后,利用TBtools的MCScanX算法进行全基因组共线性分析,重点研究内容包括:(1)各品种内AP2基因家族的复制事件(SYPsAP2、ZLPsAP2和WSPsAP2)及其染色体分布特征;(2)三月李与中李6号、巫山脆李AP2基因间的共线性关系;(3)李AP2基因与梨AP2基因的进化保守性。相关参数:E-value<1e-10,比对覆盖度>70%。
1.5 李AP2基因家族成员基因结构与功能阈分析
通过MEME在线分析平台(http://meme-suite.org/tools/meme)对三月李、中李6号和巫山脆李AP2家族成员的氨基酸序列进行保守基序预测。参数设置为:最大基序数=10,基序宽度6~50个氨基酸,其他参数为默认值。使用NCBI的Web CD-Search Tool(https://www.ncbi.nlm.nih.gov/Structure/bwrpsb/bwrpsb.cgi)进行蛋白质保守结构域在线预测,分析参数采用默认设置。使用TBtools软件的Gene Structure View(Advanced)功能模块,将基因结构注释信息(外显子-内含子结构)、保守结构域预测结果和保守基序分析数据进行整合,生成综合可视化图谱。基于STRING数据库(https://string-db.org/)进行蛋白互作分析,参考物种为拟南芥,最小互作置信度(highest confidence)为0.700,网络类型为全基因组关联网络,其他参数为默认设置。
1.6 李AP2基因家族成员启动子顺式作用元件分析
使用TBtools软件提取各AP2基因转录起始位点上游2000 bp的启动子序列,将获得的序列文件提交至PlantCARE数据库(http://bioinformatics.psb.ugent.be/webtools/plantcare/html/)进行顺式作用元件预测分析。利用TBtools的heatmap功能对不同类型的顺式作用元件在各AP2基因启动子区的分布情况进行可视化,直观呈现不同品种AP2基因启动子元件的组成特征及其潜在调控模式。
1.7 李AP2基因家族成员的基因表达分析
以入选2024年农业农村部主导品种的仕坂晚柰(P. sɑlicinɑ Lindl. var. cordɑtɑ ‘Shibanwannai’)为研究对象。采样地点为福建省宁德市古田县仕坂村果园(E 118°70′8″,N 26°63′4″,海拔280 m)。选取6年生健壮植株(株行距3.5 m×4.0 m),分别于果实发育的8个关键时期(花后43、61、72、88、100、118、133和148 d),采集果肉和种子样品,提取RNA。每个时期从3株样树的主枝上随机采集30个果实,为1个生物学重复,共设置3个独立的生物学重复。样品经液氮速冻后保存于-80 ℃超低温冰箱备用。
采用qRT-PCR技术分析基因相对表达量。基于李AP2基因序列,利用Primer Premier 5设计特异性定量引物(表1),以Actin为内参基因,引物均由擎科伟业生物技术有限公司合成。采用RNAprep Pure多糖多酚植物总RNA提取试剂盒DP441(天根生化科技北京有限公司,北京)提取总RNA,经质检合格后,使用M5 Super plus qPCR RT kit with gDNA remover(北京聚合美生物科技有限公司,北京)进行cDNA合成。使用SYBR® Premix Ex Tɑq™ Ⅱ(Tli RNaseH Plus)试剂盒[宝生物工程(大连)有限公司,大连] 在CFX96 Touch Real-Time PCR C1000 Thermal Cycler system(Bio-Rad,Hercules,CA,USA)仪器上进行qRT-PCR分析,具体反应体系和反应程序根据说明书进行设置。采用2-ΔΔCT法计算基因相对表达量,每个样品设置3次技术重复以确保数据的可靠性。
表1 李AP2基因家族表达分析的实时荧光定量引物
Table 1 qRT-PCR primers for expression analysis of plum PsAP2 gene family

基因名称Gene name SYPsAP2-5 SYPsAP2-7 WsPsAP2-9 WsPsAP2-9 WsPsAP2-11 ZLPsAP2-15 ZLPsAP2-16 PsActin上游引物(5′-3′)Forward primer (5′-3′)ATTGGCGGAATCAAGGGTTT GTGCCCAGAAAGTCCGTTG TGGGATTGTGGGAAGCAAGT TTTGGGCTTGTTTGATACCG CGTGCCCAGAAAGTCCGTT TCAACTCCTCCTCCAACCTC GTGCCCAGAAAGTCCGTTG CTGGACCTTGCTGGTCGT下游引物(5′-3′)Reverse primer (5′-3′)GGGCTGGAGAATGAAGGTTG CTTCCCTTGCGAGTTTGTCC GGGTTCAGCTCGTTCTCGTAG TCGAGTTGCATTGAGGCAGA CTTCCCTTGCGAGTTTGTCC ATGGGCAGTGTCAAATCCTC TTCCCTTGCGAGTTTGTCC ATTTCCCGCTCAGCAGTG
2 结果与分析
2.1 李AP2基因家族鉴定与基本信息
本研究通过全基因组比对结合SMART数据库验证,系统鉴定了3个李品种的AP2转录因子家族成员,并对其蛋白理化性质进行了详细分析。在三月李、中李6号和巫山脆李基因组中分别鉴定出20、22和18个AP2家族成员,按照染色体定位顺序,依次命名为SYPsAP2-1~20、ZLPsAP2-1~22和WSPsAP2-1~18。
蛋白质理化性质分析结果显示(表2),三月李AP2基因家族成员的蛋白质长度范围为356~853 aa,分子质量为40.24~93.04 kDa;理论等电点为4.73~9.23,大部分为酸性蛋白(pI<7);除SYPsAP2-19外,其余成员均属于不稳定蛋白(不稳定系数>40);所有成员均为亲水性蛋白。中李6号AP2基因家族成员的蛋白质长度范围为356~731 aa,分子质量为40.24~80.10 kDa;理论等电点为4.96~9.24;16个成员为酸性蛋白,6个成员为碱性蛋白;所有成员均为不稳定蛋白(不稳定系数>40);所有成员均为亲水性蛋白。巫山脆李AP2基因家族成员的蛋白质长度范围为208~1272 aa(长度差异较大),分子质量跨度明显(24.34~142.55 kDa);理论等电点分布范围最广(4.85~9.96);12个成员为酸性蛋白,6个成员为碱性蛋白;所有成员均为不稳定蛋白(不稳定系数>40);所有成员均为亲水性蛋白。
表2 李AP2转录因子家族理化特征
Table 2 Physiochemical properties of PsAP2 transcription factor family

基因编号Gene ID基因名称Gene name氨基酸数Number of amino acids分子质量Molecular mass/kDa理论等电点Theoretical isoeletric point不稳定系数Instability index平均亲水性Grand average of hydropathicity亚细胞定位Subcellar localization PsSY0018335 PsSY0010454 PsSY0019705 PsSY0028242 PsSY0017633 PsSY0002842 PsSY0002299 PsSY0014184 PsSY0020533 PsSY0028320 PsSY0000856 PsSY0012262 SYPsAP2-1 SYPsAP2-2 SYPsAP2-3 SYPsAP2-4 SYPsAP2-5 SYPsAP2-6 SYPsAP2-7 SYPsAP2-8 SYPsAP2-9 SYPsAP2-10 SYPsAP2-11 SYPsAP2-12 552 479 520 688 546 474 853 670 428 356 548 583 60 725.48 52 437.92 57 373.87 76 737.68 60 411.25 52 000.81 93 047.95 73 532.72 48 183.83 40 246.76 59 711.22 64 587.84 6.25 6.25 6.14 6.35 6.22 6.70 6.33 6.70 9.23 7.65 7.87 4.84 46.95 51.79 58.96 54.72 58.32 63.08 45.44 50.90 70.45 44.13 45.14 50.20-0.699-0.662-0.734-0.817-0.908-0.479-0.800-0.632-0.750-0.768-0.697-0.669 PsSY0025324 PsSY0000247 PsSY0026981 PsSY0012537 PsSY0004032 PsSY0004053 PsSY0006987 PsSY0013402 SYPsAP2-13 SYPsAP2-14 SYPsAP2-15 SYPsAP2-16 SYPsAP2-17 SYPsAP2-18 SYPsAP2-19 SYPsAP2-20 522 403 405 362 583 399 522 583 57 757.90 45 393.05 45 804.58 40 587.80 64 062.06 45 010.60 57 736.88 64 702.03 4.73 6.37 8.24 8.90 6.43 5.99 4.73 4.89 40.43 62.61 64.48 47.08 54.43 58.70 39.75 50.24-0.647-0.830-0.818-0.888-0.857-0.925-0.630-0.677 evm.model.LG01.674 evm.model.LG01.2045 evm.model.LG01.4457 evm.model.LG01.4613 evm.model.LG02.2627 evm.model.LG03.220 evm.model.LG03.336 evm.model.LG03.1104 evm.model.LG03.2003 evm.model.LG03.2008 evm.model.LG06.292 evm.model.LG06.375 evm.model.LG06.514 evm.model.LG06.656 evm.model.LG06.756 evm.model.LG06.1981 evm.model.LG06.2183 evm.model.LG06.2854 evm.model.LG07.1944 ZLPsAP2-1 ZLPsAP2-2 ZLPsAP2-3 ZLPsAP2-4 ZLPsAP2-5 ZLPsAP2-6 ZLPsAP2-7 ZLPsAP2-8 ZLPsAP2-9 ZLPsAP2-10 ZLPsAP2-11 ZLPsAP2-12 ZLPsAP2-13 ZLPsAP2-14 ZLPsAP2-15 ZLPsAP2-16 ZLPsAP2-17 ZLPsAP2-18 ZLPsAP2-19 425 670 548 356 399 363 362 569 403 405 523 523 656 546 473 731 552 479 603 47 808.36 73 501.71 59 701.18 40 246.76 45 010.60 40 629.82 40 558.66 62 299.10 45 379.02 45 805.56 57 749.34 57 749.34 73 182.08 60 411.25 51 927.76 80 102.07 60 725.48 52 437.92 66 938.52 9.24 6.70 7.87 7.65 5.99 8.78 8.63 6.43 6.37 7.68 6.14 6.14 6.47 6.22 6.70 6.69 6.25 6.25 4.96 71.23 50.79 44.79 44.13 58.70 47.60 49.51 53.04 62.13 63.55 58.40 58.40 55.00 58.32 63.20 46.37 46.95 51.79 49.24-0.771-0.629-0.696-0.768-0.925-0.849-0.893-0.849-0.830-0.804-0.717-0.717-0.770-0.908-0.477-0.845-0.699-0.662-0.673 evm.model.LG07.1945 evm.model.LG07.2037 evm.model.LG07.2038 ZLPsAP2-20 ZLPsAP2-21 ZLPsAP2-22 692 692 548 77 259.10 77 147.02 61 094.29 5.25 5.35 5.00 46.37 45.45 51.72-0.758-0.742-0.668 evm.model.Chr1.703 WSPsAP2-1 548 59 701.18 7.87 44.79-0.696细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus叶绿体Chloroplast细胞核Nucleus过氧化物酶体Peroxisome细胞核Nucleus细胞核Nucleus细胞核Nucleus叶绿体Chloroplast细胞核Nucleus细胞核Nucleus细胞核Nucleus过氧化物酶体Peroxisome细胞核Nucleus细胞核Nucleus细胞核Nucleus叶绿体Chloroplast细胞核Nucleus叶绿体Chloroplast叶绿体Chloroplast细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus过氧化物酶体Peroxisome细胞核Nucleus细胞核Nucleus过氧化物酶体Peroxisome细胞核Nucleus
表2(续) Table 2 (Continued)

基因编号Gene ID基因名称Gene name氨基酸数Number of amino acids分子质量Molecular mass/kDa理论等电点Theoretical isoeletric point不稳定系数Instability index平均亲水性Grand average of hydropathicity亚细胞定位Subcellar localization evm.model.Chr1.841 evm.model.Chr1.2643 evm.model.Chr1.4020 evm.model.Chr2.193 evm.model.Chr2.790 evm.model.Chr2.2384 evm.model.Chr2.2512 evm.model.Chr2.2656 evm.model.Chr2.2758 evm.model.Chr2.3865 evm.model.Chr3.2427 evm.model.Chr5.368 evm.model.Chr5.945 evm.model.Chr5.2460 evm.model.Chr5.2462 evm.model.Chr6.1831 WSPsAP2-2 WSPsAP2-3 WSPsAP2-4 WSPsAP2-5 WSPsAP2-6 WSPsAP2-7 WSPsAP2-8 WSPsAP2-9 WSPsAP2-10 WSPsAP2-11 WSPsAP2-12 WSPsAP2-13 WSPsAP2-14 WSPsAP2-15 WSPsAP2-16 WSPsAP2-17 356 1272 670 551 479 523 689 402 459 853 399 579 368 208 406 590 40 246.76 142 558.30 73 532.72 60 640.37 52 437.92 57 721.28 76 824.76 44 033.24 50 258.85 92 842.59 45 010.60 63 602.51 41 304.71 24 348.30 45 757.43 65 102.46 7.65 8.94 6.70 6.25 6.25 6.06 6.35 5.77 7.22 6.31 5.99 6.43 8.74 9.96 6.16 4.85 44.13 41.80 50.90 46.79 51.79 58.40 54.94 50.35 62.33 44.97 58.70 54.78 49.19 68.44 62.17 49.12-0.768-0.523-0.632-0.704-0.662-0.715-0.817-0.863-0.503-0.802-0.925-0.870-0.840-1.062-0.801-0.635 evm.model.Chr6.1832 evm.model.LG01.674 evm.model.LG01.2045 evm.model.LG01.4457 evm.model.LG01.4613 evm.model.LG02.2627 evm.model.LG03.220 evm.model.LG03.336 evm.model.LG03.1104 evm.model.LG03.2003 evm.model.LG03.2008 evm.model.LG06.292 evm.model.LG06.375 evm.model.LG06.514 evm.model.LG06.656 evm.model.LG06.756 evm.model.LG06.1981 evm.model.LG06.2183 evm.model.LG06.2854 evm.model.LG07.1944 WSPsAP2-18 ZLPsAP2-1 ZLPsAP2-2 ZLPsAP2-3 ZLPsAP2-4 ZLPsAP2-5 ZLPsAP2-6 ZLPsAP2-7 ZLPsAP2-8 ZLPsAP2-9 ZLPsAP2-10 ZLPsAP2-11 ZLPsAP2-12 ZLPsAP2-13 ZLPsAP2-14 ZLPsAP2-15 ZLPsAP2-16 ZLPsAP2-17 ZLPsAP2-18 ZLPsAP2-19 695 425 670 548 356 399 363 362 569 403 405 523 523 656 546 473 731 552 479 603 77 762.98 47 808.36 73 501.71 59 701.18 40 246.76 45 010.60 40 629.82 40 558.66 62 299.10 45 379.02 45 805.56 57 749.34 57 749.34 73 182.08 60 411.25 51 927.76 80 102.07 60 725.48 52 437.92 66 938.52 5.47 9.24 6.70 7.87 7.65 5.99 8.78 8.63 6.43 6.37 7.68 6.14 6.14 6.47 6.22 6.70 6.69 6.25 6.25 4.96 44.52 71.23 50.79 44.79 44.13 58.70 47.60 49.51 53.04 62.13 63.55 58.40 58.40 55.00 58.32 63.20 46.37 46.95 51.79 49.24-0.713-0.771-0.629-0.696-0.768-0.925-0.849-0.893-0.849-0.830-0.804-0.717-0.717-0.770-0.908-0.477-0.845-0.699-0.662-0.673 evm.model.LG07.1945 evm.model.LG07.2037 evm.model.LG07.2038 ZLPsAP2-20 ZLPsAP2-21 ZLPsAP2-22 692 692 548 77 259.10 77 147.02 61 094.29 5.25 5.35 5.00 46.37 45.45 51.72-0.758-0.742-0.668叶绿体Chloroplast细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus叶绿体Chloroplast细胞核Nucleus细胞核Nucleus过氧化物酶体Peroxisome细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus叶绿体Chloroplast细胞核Nucleus叶绿体Chloroplast叶绿体Chloroplast细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus细胞核Nucleus过氧化物酶体Peroxisome细胞核Nucleus细胞核Nucleus过氧化物酶体Peroxisome
亚细胞定位预测结果显示,3个李品种的AP2基因家族成员主要定位于细胞核(三月李16个成员、中李6号17个成员、巫山脆李15个成员),少量分布于叶绿体和过氧化物酶体等细胞器,该分布特征与典型转录因子的亚细胞定位模式相符。
2.2 李AP2基因家族成员系统进化树构建
使用MEGA11软件,构建了包含三月李、中李6号、巫山脆李、拟南芥以及蔷薇科苹果和梨的AP2基因家族系统进化树。参考拟南芥AP2转录因子家族的分类标准,共分为13个亚族,包括AP2型、RAP2-7型、T11A7.19型、WRI1型、ADAP型、ANT型、AIL5型、AIL6型、AIL1型、BBM型、PLT1型、PLT2型和TOE型(图1)。

图1 三月李、中李6号、巫山脆李、苹果、梨和拟南芥AP2家族成员系统进化树
Fig. 1 Phylogenetic tree of AP2 gene family in Sanyueli, Zhongli No. 6, Wushancuili, Malus domestica, Pyrus bretschneideri and Arabidopsis thaliana
系统进化分析结果显示,TOE亚族为拟南芥特有,仅包含一个成员(AT5G67180.1)。T11A7.19亚族仅由苹果AP2基因家族成员组成。其余11个亚族均包含3个李品种的AP2基因家族成员,表明李AP2家族具有较高的遗传多样性。AP2型、RAP2-7型和WRI1型3个亚族呈现出明显的间隔分布模式,暗示这些成员虽然被划分为同一亚族,但它们在长期进化过程中可能发生了功能分化。从物种亲缘关系来看,3个李品种的AP2基因家族成员聚集成簇,与苹果和梨相比表现出更近的亲缘关系,这与它们的物种系统分类地位相符。
2.3 李AP2基因家族成员染色体定位
通过全基因组注释分析,系统鉴定了3个李品种AP2基因家族成员的染色体分布特征。结果显示,AP2家族成员在不同品种中呈现非均匀分布模式。三月李SYPsAP2基因家族成员分布于6条染色体(Chr1~5、Chr8),其中Chr1包含7个成员(35%),而Chr3、Chr5和Chr8仅包含1~2个成员,表现出明显的染色体偏好性(图2-A)。中李6号ZLPsAP2基因家族成员分布于5条染色体(Chr1~3、Chr6~7),Chr3和Chr6集中了超过50%的家族成员,而Chr2仅含有1个成员(图2-B)。巫山脆李WSPsAP2基因家族成员分布于5条染色体(Chr1~3、Chr5~6),呈现2个显著特征:Chr2集中分布了7个成员(38.9%),构成主要分布区域;而Chr3仅含有1个成员(图2-C)。
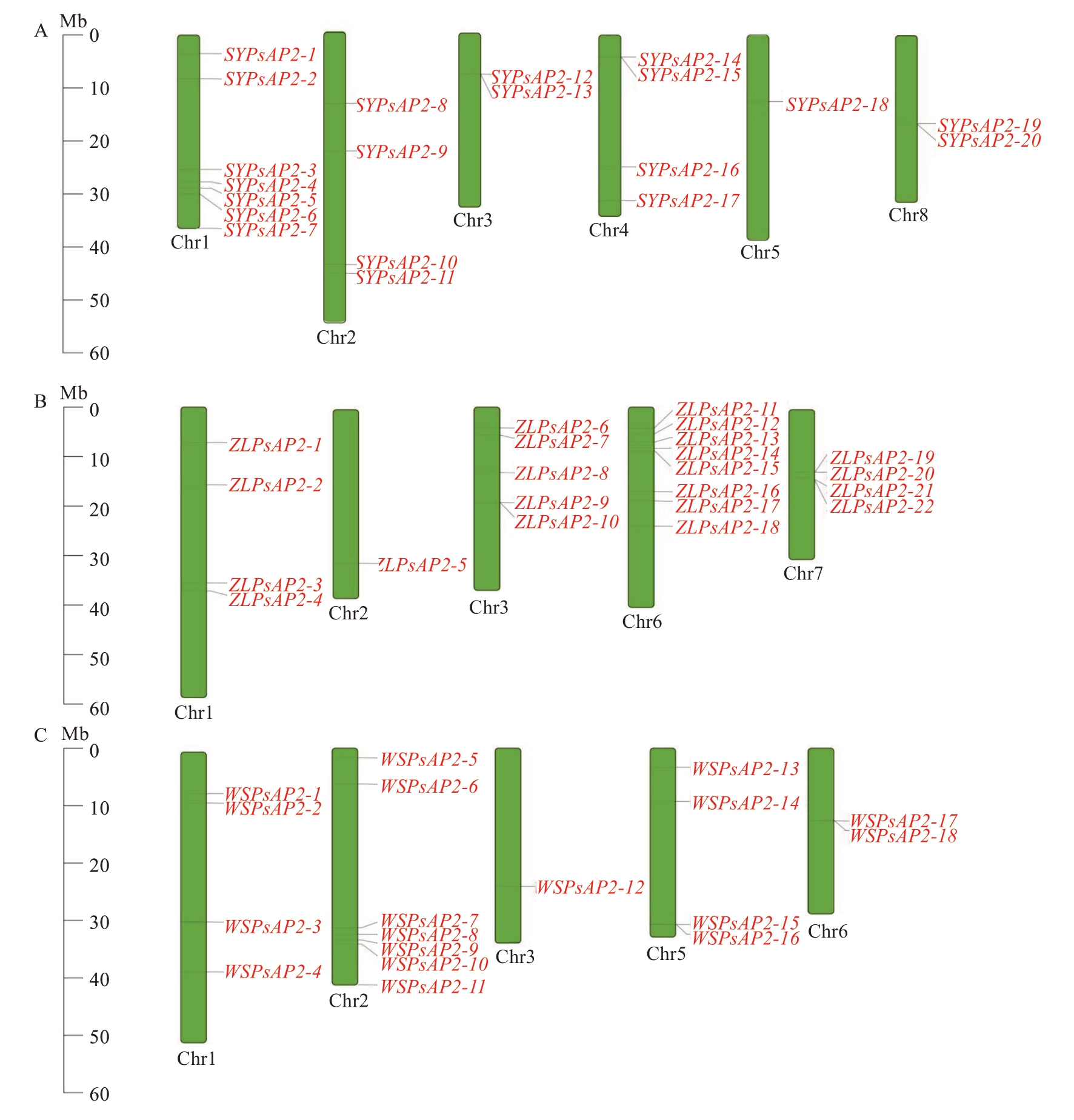
图2 李PsAP2基因家族成员在三月李(A)、中李6号(B)和巫山脆李(C)染色体上的分布位置
Fig. 2 The location distribution of PsAP2 gene family members across the chromosomes of Sanyueli (A), Zhongli No. 6 (B),and Wushancuili (C)
2.4 李AP2基因家族成员种内与种间共线性
种内共线性分析结果显示,三月李基因组鉴定到3对SYPsAP2共线性基因,包括SYPsAP2-4/SYPsAP2-8、SYPsAP2-9/SYPsAP2-14和SYPsAP2-12/SYPsAP2-19(图3-A)。中李6号表现出最丰富的共线性关系,共检测到7对ZLPsAP2共线性基因:ZLPsAP2-1/ZLPsAP2-9、ZLPsAP2-2/ZLPsAP2-13、ZLPsAP2-6/ZLPsAP2-7、ZLPsAP2-11/ZLPsAP2-12、ZLPsAP2-15/ZLPsAP2-18、ZLPsAP2-17/ZLPsAP2-19和ZLPsAP2-19/ZLPsAP2-21(图3-B)。巫山脆李鉴定到4对WSPsAP2共线性基因,分别为WSPsAP2-3/WSPsAP2-15、WSPsAP2-4/WSPsAP2-8、WSPsAP2-5/WSPsAP2-17和WSPsAP2-6/WSPsAP2-10(图3-C)。
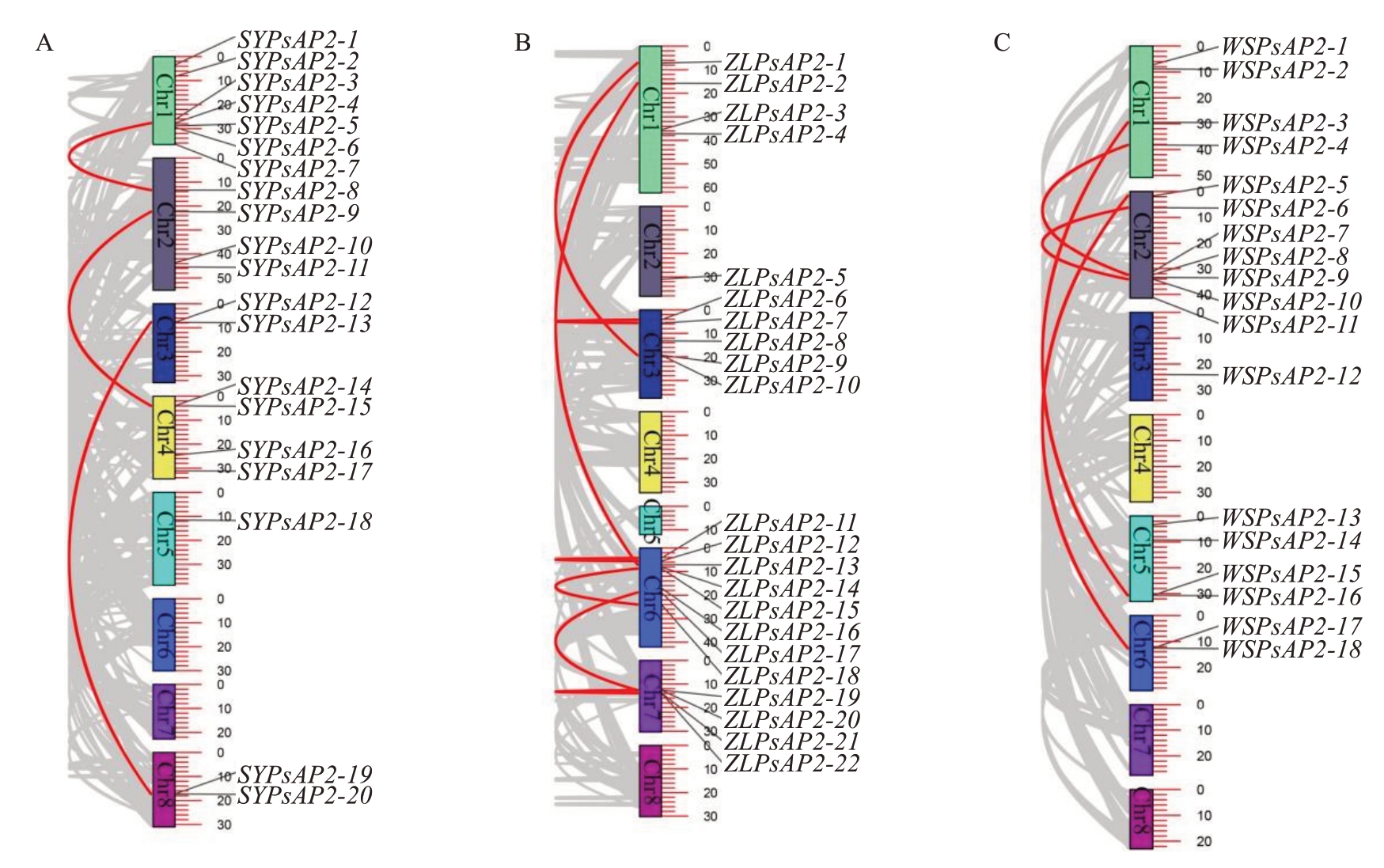
图3 李PsAP2基因家族成员在三月李(A)、中李6号(B)和巫山脆李(C)的种内共线性
Fig. 3 Collinearity analysis of PsAP2 gene family of Sanyueli (A), Zhongli No. 6 (B), andWushancuili (C)
种间共线性分析结果显示,三月李与中李6号存在25对共线性基因,显示出最高的同源保守性;与巫山脆李有19对共线性基因;与近缘种梨有21对共线性基因(图4)。
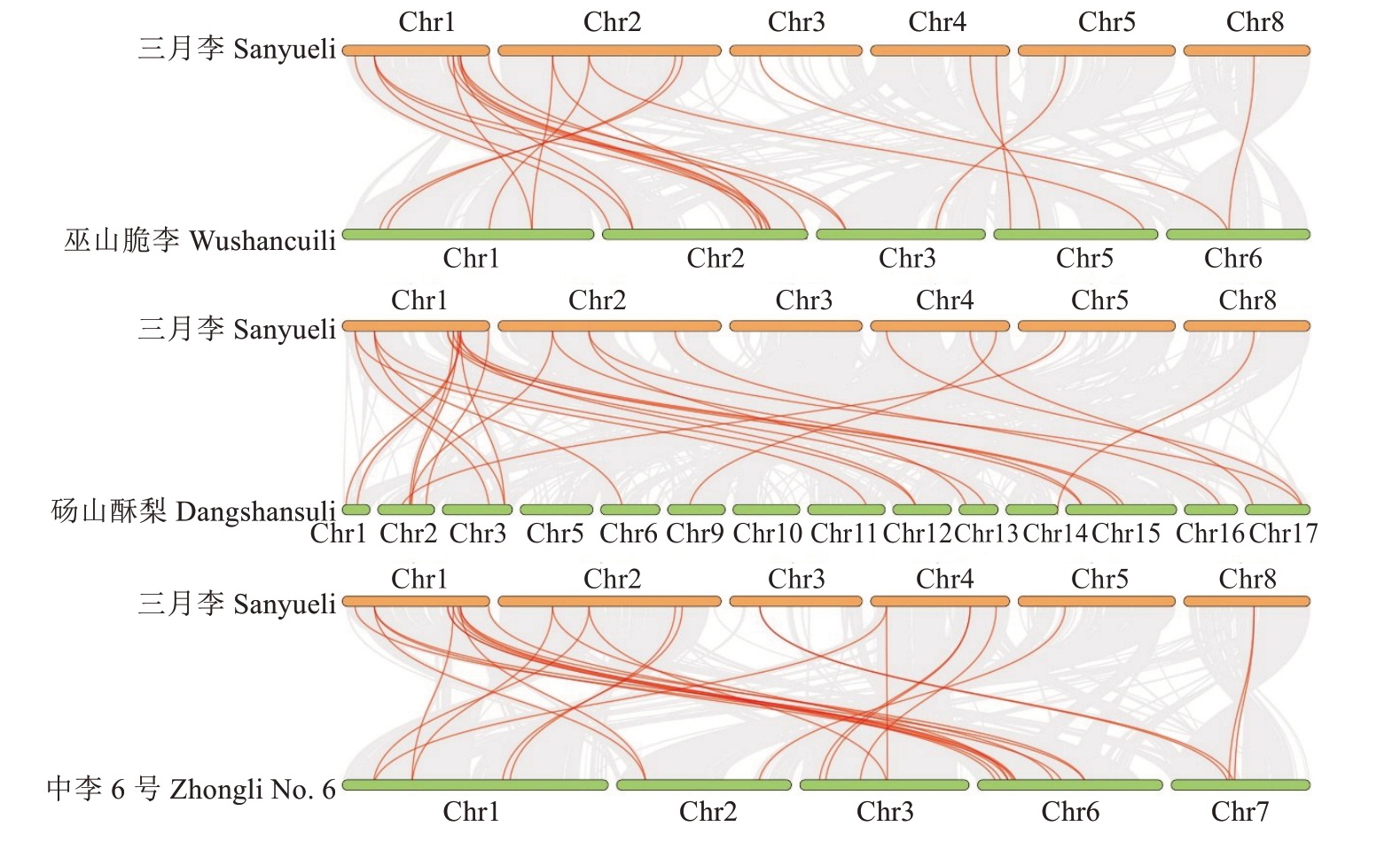
图4 李PsAP2基因家族成员在三月李与巫山脆李、砀山酥梨和中李6号的种间共线性
Fig. 4 Collinearity analysis of PsAP2 gene family between Sanyueli, Wushancuili, Dangshansuli and Zhongli No. 6
2.5 李AP2基因家族成员的保守结构域与基因结构
保守基序分析结果(图5-A)显示,motif 2为60个PsAP2成员共有,是最保守的核心基序。motif 2、motif 4、motif 1和motif 5出现频率最高,通常有序排列且偏向5'端分布,呈现保守特征。蛋白质保守结构域预测结果(图5-B)显示,PsAP2成员均含有典型的双AP2结构域,但存在2个特殊成员:WSPsAP2-3额外含有1对Amb_all和Pec_lyase_N结构域并间隔排列,SYPsAP2-19的C端具有dermokine超家族的保守结构域,其独特结构域暗示这2个基因可能演化出新的生物学功能。
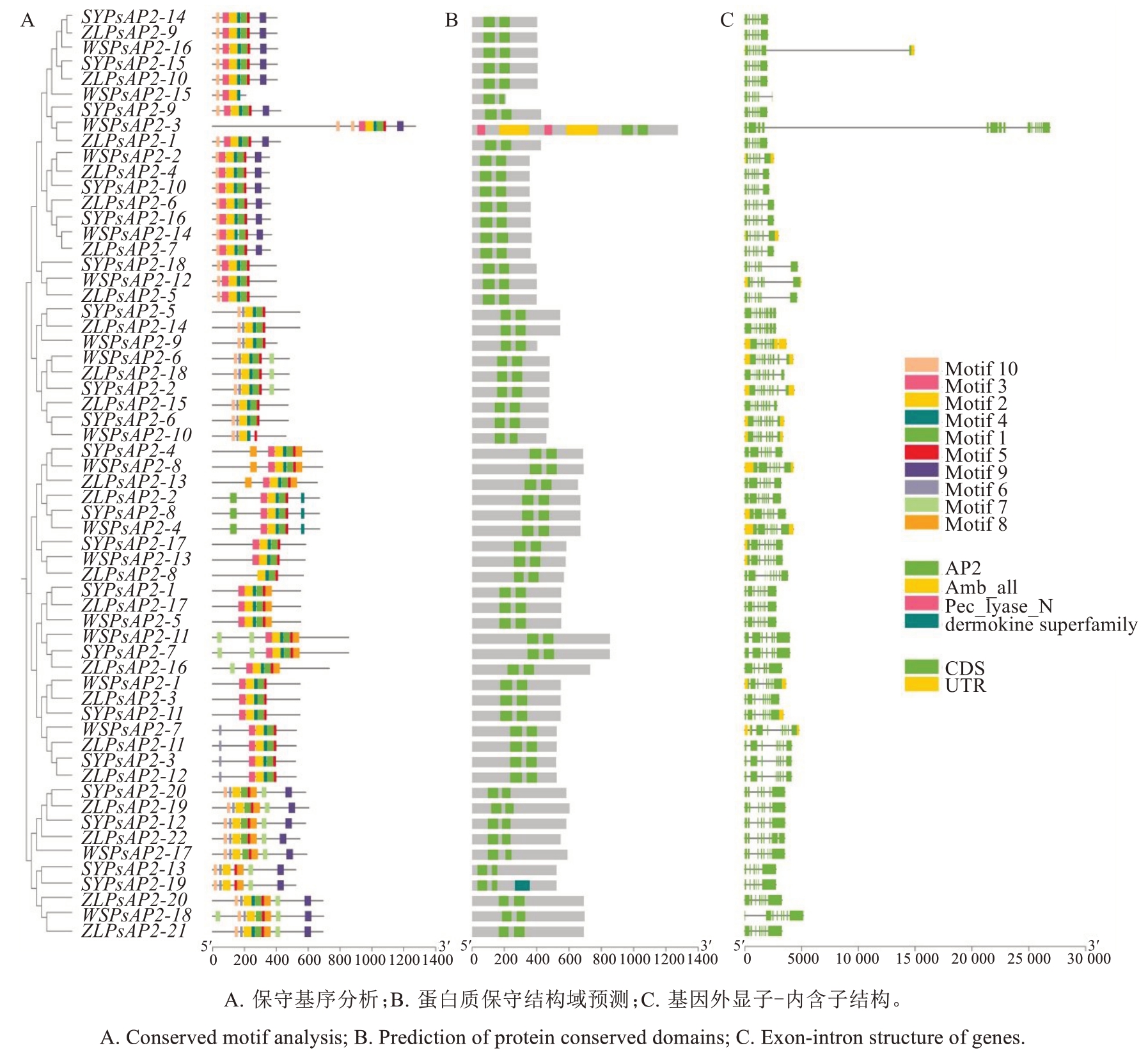
图5 李PsAP2家族成员的结构特征分析
Fig. 5 Structure characterization of AP2 gene family members in P. salicina Lindl.
基因结构分析结果(图5-C)显示,三月李SYPsAP2基因家族成员的外显子数目为6~10个,其中75%的成员具有7~9个外显子。中李6号ZLPsAP2基因家族中,仅ZLPsAP2-16具有6个外显子,其余成员为7~10个外显子。巫山脆李WSPsAP2基因家族中除WSPsAP2-3(15个外显子)和WSPsAP2-6(10个外显子)外,其余成员均具有7~9个外显子。AP2基因家族成员在3个李品种中均保持相对稳定的外显子数目。
2.6 李AP2基因家族成员的启动子顺式作用元件
启动子顺式作用元件分析结果(图6)显示,李AP2基因家族成员的启动子区显著富集多种响应元件。3个李品种共有的核心响应元件:光响应元件(SYPsAP2、ZLPsAP2和WSPsAP2基因家族分别为282、307和226个)、脱落酸响应元件(SYPsAP2、ZLPsAP2和WSPsAP2基因家族分别为66、62和52个)、茉莉酸甲酯响应元件(SYPsAP2、ZLPsAP2和WSPsAP2基因家族分别为40、48和32个)、赤霉素响应元件(SYPsAP2、ZLPsAP2和WSPsAP2基因家族分别为25、28和23个)、厌氧诱导响应元件(SYPsAP2、ZLPsAP2和WSPsAP2基因家族分别为52、57和49个)。
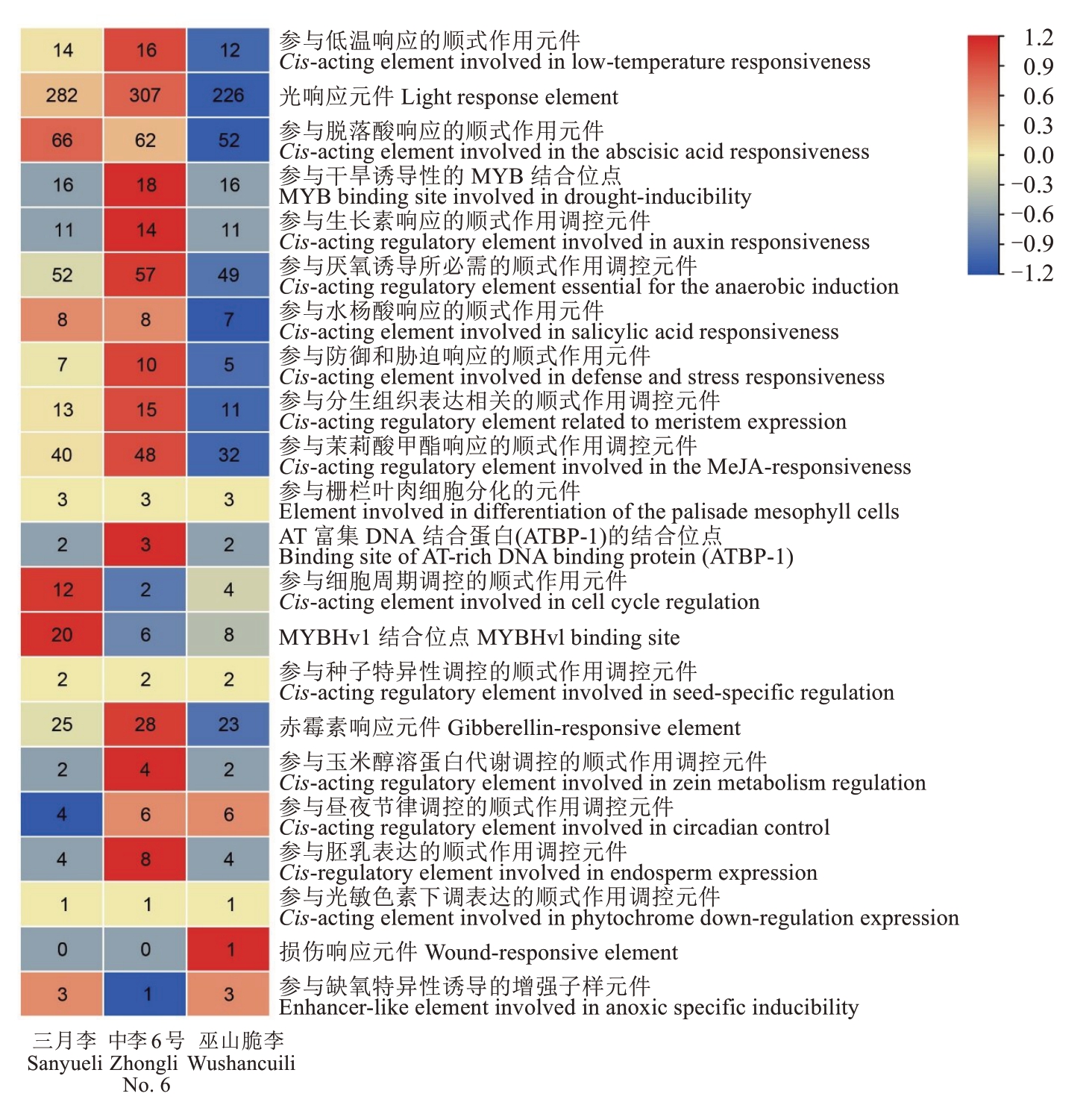
图6 李PsAP2家族成员的启动子顺式作用元件
Fig. 6 Cis-acting elements of AP2 gene family members in P. salicina Lindl.
3个李品种的特异性调控特征:三月李MYBHv1结合位点数量(20个)远多于中李6号(6个)和巫山脆李(8个),SYPsAP2可能在MYBHv1介导的调控通路中发挥重要作用。中李6号ZLPsAP2启动子区顺式作用元件的种类与数量最为丰富,中李6号AP2基因可能具有更复杂的调控网络。巫山脆李WSPsAP2含特有的创伤响应元件,可能参与植物创伤响应机制。
李AP2基因家族中的特定成员可能参与调控了种子发育和光信号转导过程。SYPsAP2-7、SYPsAP2-11、ZLPsAP2-3、ZLPsAP2-16、WSPsAP2-1和WSPsAP2-11具有种子特异性调控元件,SYPsAP2-2、ZLPsAP2-18和WSPsAP2-6具有光敏色素调控元件。
2.7 李AP2基因家族成员的表达模式
基于系统进化树和启动子顺式作用元件分析结果,选取了AP2和BBM两个功能亚族的6个代表性成员(AP2亚族:SYPsAP2-5、ZLPsAP2-15和WSPsAP2-9;BBM亚族:SYPsAP2-7、ZLPsAP2-16和WSPsAP2-11),系统分析了其在仕坂晚柰果实8个发育时期的表达特征。结果显示,这些基因表现出显著的组织特异性表达模式(图7)。
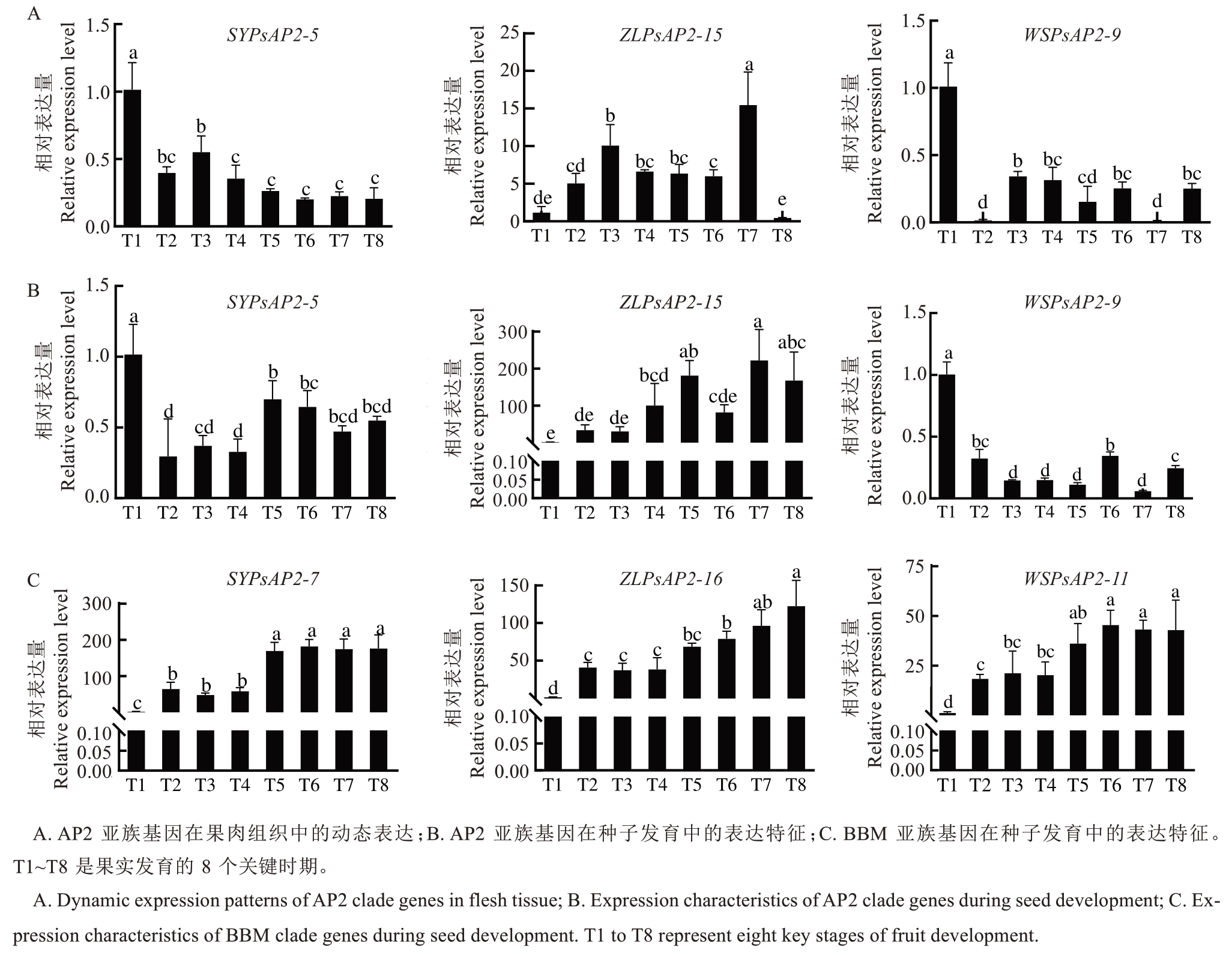
图7 李AP2基因家族在果实发育过程中的时空模式
Fig. 7 Spatiotemporal expression profiling of AP2 gene family members during fruit development in P. salicina Lindl. var. cordata ‘Shibanwannai’
在果肉组织中,AP2亚族成员的SYPsAP2-5在T1时期(幼果期)表达量最高,T2时期显著下降,T2~T3时期短暂回升后持续降低;WSPsAP2-9在T1时期达峰值,T2时期急剧下降,T8时期(成熟期)再次回升;而ZLPsAP2-15呈现出独特的双峰表达模式(在T2~T3和T6~T7出现表达高峰)。虽然SYPsAP2-5、WSPsAP2-9和ZLPsAP2-15同属AP2亚族,但ZLPsAP2-15的表达模式显著不同于前两者,可能与其在进化树中的特殊位置相关。经过多次RT-PCR重复验证,一致发现BBM亚族成员(SYPsAP2-7、ZLPsAP2-16和WSPsAP2-11)在果肉的各发育时期均无法检测到稳定的表达信号,即表达量极低或几乎不表达。
在种子发育过程中,AP2亚族的SYPsAP2-5和WSPsAP2-9的表达水平整体较低,而AP2亚族的ZLPsAP2-15与BBM亚族的SYPsAP2-7、ZLPsAP2-16和WSPsAP2-11在T5~T8时期持续高表达,且在T4~T5时期表达量急剧上升,维持高表达水平至果实成熟。
3 讨 论
3.1 李AP2基因家族的系统进化与功能分化
转录因子作为基因表达调控的核心元件,能够整合多种信号转导途径,在植物生长发育和环境适应中发挥枢纽作用[1]。AP2/ERF超家族作为植物特有的转录因子家族,在调控生长发育、形态建成和逆境响应等生物学过程中具有不可替代的功能[4,12,14-18]。其中,AP2亚家族通过精确调控花器官发育、胚胎发生、分生组织分化和叶片形态建成等关键生物学过程,展现出显著的分子多效性,是植物发育调控网络的核心组成部分[19-27]。
笔者首次对李AP2转录因子家族进行全基因水平的系统鉴定,从三月李、中李6号和巫山脆李中分别鉴定出20、22和18个成员,其数量在不同品种间存在差异,可能源于多个因素的综合作用。首先,各基因组组装与注释质量的差异会影响预测的完整性。三月李(282.38 Mb)[30]、中李6号(318.6 Mb)[31]和巫山脆李(302.17 Mb)[32]基因组大小存在差异,基因组组装与注释的质量及完整性也是导致基因数量预测出现差异的关键因素。其次,物种特有的基因家族扩增与收缩同样可能影响到AP2等特定基因家族。参考各基因组的基因家族进化分析数据[30-32],三月李:+1145,-2511;中李6号:+1009,-1743;巫山脆李:+359,-2941。其中,中李6号经历了最显著的基因家族净扩张(扩张数-收缩数的负值最小),这与其鉴定出最多AP2成员(22个)的结果相吻合;巫山脆李经历了最剧烈的基因家族净收缩,这可能是其AP2成员数量最少(18个)的重要原因。
与其他物种比较分析发现,李AP2基因家族的规模呈现出明显的物种特异性分布特征。与模式植物拟南芥(14个)[33]和主要粮食作物水稻(16个)[33]相比,李AP2基因家族数量较多,表明木本植物较草本植物可能具有更复杂的转录调控网络以适应多年生长习性。在蔷薇科植物中,李AP2基因数量显著少于苹果(51个)[34]和沙梨(38个)[35],而与核果类近缘种扁桃(20个)[36]、桃(21个)[37]和梅(20个)[38]等基本相当,表明核果类果树在进化过程中可能保持了相对保守的AP2基因家族规模。与其他果树类群相比,李AP2基因数量多于藤本果树百香果(10个)[39]和甜橙(14个)[40],少于猕猴桃(34个)[41],与葡萄(20个)[42]和克里曼丁橘(18个)[43]相近。李AP2基因数量也少于裸子植物火炬松(34个)[44]。这些比较结果表明,AP2基因家族的扩张与收缩可能与物种的进化历史和生态适应性密切相关,李AP2基因家族的规模既反映了蔷薇科植物的共同特征,也体现了李属植物的特异性适应,核果类果树相对保守的AP2基因数量可能与其特定的发育调控需求相关。
通过蛋白质保守结构域分析发现,三月李、中李6号和巫山脆李3个品种的AP2基因家族成员均包含1对典型的AP2结构域,这一特征与AP2/ERF超家族的定义相符[4,12]。笔者还鉴定到2个具有特殊结构域的成员:除AP2结构域外,WSPsAP2-3还含有1对Amb_all和Pec_lyase_N保守结构域,并间隔排列,形成独特的模块化结构;SYPsAP2-19在末端还含有dermokine superfamily保守结构域。前人研究表明,Amb_all结构域可能参与蛋白质互作,Pec_lyase_N保守结构域被认为是实现果胶裂解所必需的功能团[45-46],已知dermokine超家族结构域参与动物表皮分化,但在植物中的功能尚不明确。笔者首次报道了李AP2基因家族蛋白存在非典型结构域,为深入理解AP2转录因子的功能多样性提供了新的线索。
3.2 李AP2顺式作用元件的功能启示
3个李品种AP2基因家族成员启动子区顺式作用元件种类丰富,主要包括光响应元件、激素响应元件和逆境响应元件。其中,茉莉酸甲酯(MeJA)和脱落酸(ABA)响应元件数量最为丰富。MeJA是植物重要的防御激素和生长调节物质,能够激活多种防御相关基因的表达,参与调控根系发育、花粉育性、叶片衰老等过程。此外,MeJA与干旱、低温、盐胁迫等逆境响应密切相关,参与调控多种次生代谢产物的生物合成[47]。ABA作为植物生长发育的关键调控因子,在种子休眠与萌发、器官脱落以及逆境响应等生理过程中发挥核心作用[48]。因此,该结果为深入理解李AP2基因家族的转录调控机制和功能分化提供了重要线索,也为后续开展相关基因的功能验证研究奠定了理论基础。
3.3 AP2组织特异性表达模式的功能意义
BBM基因是细胞增殖、分化和形态发生的关键转录因子,尤其在胚胎发生过程中发挥重要作用[21-25]。BBM基因在拟南芥种子发育过程中呈现特异性高表达模式[21]。本研究中BBM亚族成员SYPsAP2-7、ZLPsAP2-16和WSPsAP2-11含有种子特异性调控元件,在T4~T8时期呈现显著的高表达特征。特别是其表达量急剧上升时期(T4~T5时期),与笔者长期观察到的仕坂晚柰种子败育发生的关键时期高度吻合,T5时期正是仕坂晚柰种子开始大量出现败育现象的发育阶段。该时空表达特征暗示这些BBM亚族成员可能参与调控了仕坂晚柰种子的败育过程,为揭示李种子发育的分子机制提供了新线索,也为探究蔷薇科植物种子败育问题提供了潜在的调控靶点。后续研究将通过基因敲除、过表达或基因编辑等技术进行直接的功能验证,以进一步明确这些基因在果实发育中的具体生物学功能。
4 结 论
笔者系统鉴定了李AP2转录因子家族,在三月李、中李6号和巫山脆李中分别鉴定出20、22和18个成员,其数量与核果类近缘种扁桃、桃和梅等相当,但少于苹果和沙梨,表明蔷薇科植物特异的进化特征。启动子顺式作用元件分析结果显示,李AP2转录因子富含ABA和MeJA响应元件,可能通过整合激素信号参与调控种子发育。基因表达分析结果表明,AP2亚族成员主要在果实发育早期活跃,BBM亚族成员(SYPsAP2-7、WSPsAP2-11和ZLPsAP2-16)在种子发育后期特异性高表达,呈现出组织特异性表达模式。本研究为解析李AP2基因家族的转录调控机制和功能分化提供了重要线索。
[1] STRADER L,WEIJERS D,WAGNER D. Plant transcription factors:Being in the right place with the right company[J] . Current Opinion in Plant Biology,2022,65:102136.
[2] BLANC-MATHIEU R,DUMAS R,TURCHI L,LUCAS J,PARCY F. Plant-TFClass:A structural classification for plant transcription factors[J] . Trends in Plant Science,2024,29(1):40-51.
[3] CHEN Y E,XIA P G. NAC transcription factors as biological macromolecules responded to abiotic stress:A comprehensive review[J] . International Journal of Biological Macromolecules,2025,308:142400.
[4] FENG K,HOU X L,XING G M,LIU J X,DUAN A Q,XU Z S,LI M Y,ZHUANG J,XIONG A S. Advances in AP2/ERF super-family transcription factors in plant[J] . Critical Reviews in Biotechnology,2020,40(6):750-776.
[5] MA Z M,HU L J. WRKY transcription factor responses and tolerance to abiotic stresses in plants[J] . International Journal of Molecular Sciences,2024,25(13):6845.
[6] ZHANG D W,ZHOU H P,ZHANG Y,ZHAO Y Q,ZHANG Y Y,FENG X X,LIN H H. Diverse roles of MYB transcription factors in plants[J] . Journal of Integrative Plant Biology,2025,67(3):539-562.
[7] GUO J R,SUN B X,HE H R,ZHANG Y F,TIAN H Y,WANG B S. Current understanding of bHLH transcription factors in plant abiotic stress tolerance[J] . International Journal of Molecular Sciences,2021,22(9):4921.
[8] LIU H T,TANG X,ZHANG N,LI S G,SI H J. Role of bZIP transcription factors in plant salt stress[J] . International Journal of Molecular Sciences,2023,24(9):7893.
[9] GANGAPPA S N,BOTTO J F. The BBX family of plant transcription factors[J] . Trends in Plant Science,2014,19(7):460-470.
[10] ZHANG Z H,ZOU W H,LIN P X,WANG Z X,CHEN Y,YANG X D,ZHAO W Y,ZHANG Y Y,WANG D J,QUE Y X,WU Q B. Evolution and function of MADS-box transcription factors in plants[J] . International Journal of Molecular Sciences,2024,25(24):13278.
[11] ZOU X M,SUN H M. DOF transcription factors:Specific regulators of plant biological processes[J] . Frontiers in Plant Science,2023,14:1044918.
[12] MA Z M,HU L J,JIANG W Z. Understanding AP2/ERF transcription factor responses and tolerance to various abiotic stresses in plants:A comprehensive review[J] . International Journal of Molecular Sciences,2024,25(2):893.
[13] SHIGYO M,HASEBE M,ITO M. Molecular evolution of the AP2 subfamily[J] . Gene,2006,366(2):256-265.
[14] 洪林,杨蕾,杨海健,王武. AP2/ERF转录因子调控植物非生物胁迫响应研究进展[J] . 植物学报,2020,55(4):481-496.HONG Lin,YANG Lei,YANG Haijian,WANG Wu. Research advances in AP2/ERF transcription factors in regulating plant responses to abiotic stress[J] . Chinese Bulletin of Botany,2020,55(4):481-496.
[15] YE B B,SHANG G D,PAN Y,XU Z G,ZHOU C M,MAO Y B,BAO N,SUN L J,XU T D,WANG J W. AP2/ERF transcription factors integrate age and wound signals for root regeneration[J] .The Plant Cell,2020,32(1):226-241.
[16] RITONGA F N,NGATIA J N,WANG Y R,KHOSO M A,FAROOQ U,CHEN S. AP2/ERF,an important cold stress-related transcription factor family in plants:A review[J] . Physiology and Molecular Biology of Plants,2021,27(9):1953-1968.
[17] SU Z L,LI A M,WANG M,QIN C X,PAN Y Q,LIAO F,CHEN Z L,ZHANG B Q,CAI W G,HUANG D L. The role of AP2/ERF transcription factors in plant responses to biotic stress[J] .International Journal of Molecular Sciences,2025,26(10):4921.
[18] XIE W,DING C Q,HU H T,DONG G J,ZHANG G H,QIAN Q,REN D Y. Molecular events of rice AP2/ERF transcription factors[J] . International Journal of Molecular Sciences,2022,23(19):12013.
[19] KUNST L,KLENZ J E,MARTINEZ-ZAPATER J,HAUGHN G W. AP2 gene determines the identity of perianth organs in flowers of Arɑbidopsis thɑliɑnɑ[J] . The Plant Cell,1989,1(12):1195-1208.
[20] HAN Y,TANG A Y,WAN H H,ZHANG T X,CHENG T R,WANG J,YANG W R,PAN H T,ZHANG Q X. An APETALA2 homolog,RcAP2,regulates the number of rose petals derived from stamens and response to temperature fluctuations[J] . Frontiers in Plant Science,2018,9:481.
[21] BOUTILIER K,OFFRINGA R,SHARMA V K,KIEFT H,OUELLET T,ZHANG L M,HATTORI J,LIU C M,VAN LAMMEREN A A M,MIKI B L A,CUSTERS J B M,VAN LOOKEREN C M M. Ectopic expression of BABY BOOM triggers a conversion from vegetative to embryonic growth[J] . The Plant Cell,2002,14(8):1737-1749.
[22] HEIDMANN I,DE LANGE B,LAMBALK J,ANGENENT G C,BOUTILIER K. Efficient sweet pepper transformation mediated by the BABY BOOM transcription factor[J] . Plant Cell Reports,2011,30(6):1107-1115.
[23] LOWE K,WU E,WANG N,HOERSTER G,HASTINGS C,CHO M J,SCELONGE C,LENDERTS B,CHAMBERLIN M,CUSHATT J,WANG L J,RYAN L,KHAN T,CHOW-YIU J,HUA W,YU M,BANH J,BAO Z M,BRINK K,IGO E,RUDRAPPA B,SHAMSEER P M,BRUCE W,NEWMAN L,SHEN B,ZHENG P Z,BIDNEY D,FALCO C,REGISTER J,ZHAO Z Y,XU D P,JONES T,GORDON-KAMM W. Morphogenic regulators Bɑby boom and Wuschel improve monocot transformation[J] . The Plant Cell,2016,28(9):1998-2015.
[24] MOOKKAN M,NELSON-VASILCHIK K,HAGUE J,ZHANG Z J,KAUSCH A P. Selectable marker independent transformation of recalcitrant maize inbred B73 and sorghum P898012 mediated by morphogenic regulators BABY BOOM and WUSCHEL2[J] . Plant Cell Reports,2017,36(9):1477-1491.
[25] KHANDAY I,SKINNER D,YANG B,MERCIER R,SUNDARESAN V. A male-expressed rice embryogenic trigger redirected for asexual propagation through seeds[J] . Nature,2019,565(7737):91-95.
[26] LIU K,YANG A,YAN J D,LIANG Z L,YUAN G P,CONG P H,ZHANG L Y,HAN X L,ZHANG C X. MdAIL5 overexpression promotes apple adventitious shoot regeneration by regulating hormone signaling and activating the expression of shoot development-related genes[J] . Horticulture Research,2023,10(11):uhad198.
[27] KRIZEK B A,BANTLE A T,HEFLIN J M,HAN H,FREESE N H,LORAINE A E. AINTEGUMENTA and AINTEGUMENTA-LIKE6 directly regulate floral homeotic,growth,and vascular development genes in young Arɑbidopsis flowers[J] . Journal of Experimental Botany,2021,72(15):5478-5493.
[28] 刘硕,徐铭,刘家成,章秋平,马小雪,刘宁,张玉萍,张玉君,赵海娟,刘威生. 世界李育种概况[J] . 中国农业科学,2023,56(9):1744-1759.LIU Shuo,XU Ming,LIU Jiacheng,ZHANG Qiuping,MA Xiaoxue,LIU Ning,ZHANG Yuping,ZHANG Yujun,ZHAO Haijuan,LIU Weisheng. An overview of the worldwide plum breeding[J] . Scientia Agricultura Sinica,2023,56(9):1744-1759.
[29] 张加延. 中国果树科学与实践-李[M] . 西安:陕西科学技术出版社,2015.ZHANG Jiayan. Chinese fruit tree science and practice:Plum[M] .Xi’an:Shaanxi Science & Technology Press,2015.
[30] FANG Z Z,KUI L W,DAI H,ZHOU D R,JIANG C C,ESPLEY R V,DENG C,LIN Y J,PAN S L,YE X F. The genome of low-chill Chinese plum ‘Sanyueli’ (Prunus sɑlicinɑ Lindl.) provides insights into the regulation of the chilling requirement of flower buds[J] . Molecular Ecology Resources,2022,22(5):1919-1938.
[31] HUANG Z Y,SHEN F,CHEN Y L,CAO K,WANG L R. Chromosome-scale genome assembly and population genomics provide insights into the adaptation,domestication,and flavonoid metabolism of Chinese plum[J] . The Plant Journal,2021,108(4):1174-1192.
[32] ZHOU K,WANG J W,PAN L,XIANG F,ZHOU Y,XIONG W,ZENG M,GRIERSON D,KONG W B,HU L Y,XI W P. A chromosome-level genome assembly for Chinese plum ‘Wushancuili’ reveals the molecular basis of its fruit color and susceptibility to rain-cracking[J] . Horticultural Plant Journal,2024,10(3):672-688.
[33] NAKANO T,SUZUKI K,FUJIMURA T,SHINSHI H. Genome-wide analysis of the ERF gene family in Arɑbidopsis and rice[J] . Plant Physiology,2006,140(2):411-432.
[34] GIRARDI C L,ROMBALDI C V,DAL CERO J,NOBILE P M,LAURENS F,BOUZAYEN M,QUECINI V. Genome-wide analysis of the AP2/ERF superfamily in apple and transcriptional evidence of ERF involvement in scab pathogenesis[J] . Scientia Horticulturae,2013,151:112-121.
[35] XU Y,LI X N,YANG X,WASSIE M,SHI H Y. Genome-wide identification and molecular characterization of the AP2/ERF superfamily members in sand pear (Pyrus pyrifoliɑ)[J] . BMC Genomics,2023,24(1):32.
[36] ZHANG D D,ZENG B,HE Y W,LI J G,YU Z F. Genomewide identification and comparative analysis of the AP2/ERF gene family in Prunus dulcis and Prunus tenellɑ:Expression of PdAP2/ERF genes under freezing stress during dormancy[J] .BMC Genomics,2025,26(1):95.
[37] ZHANG C H,SHANGGUAN L F,MA R J,SUN X,TAO R,GUO L,KORIR N K,YU M L. Genome-wide analysis of the AP2/ERF superfamily in peach (Prunus persicɑ)[J] . Genetics and Molecular Research,2012,11(4):4789-4809.
[38] DU D L,HAO R J,CHENG T R,PAN H T,YANG W R,WANG J,ZHANG Q X. Genome-wide analysis of the AP2/ERF gene family in Prunus mume[J] . Plant Molecular Biology Reporter,2013,31(3):741-750.
[39] LUO L J,ZHANG L P,GU R H,NI S H,YU J Y,GAO Y C,FANG C Y. Genome-wide identification and functional analysis of AP2/ERF gene family in Pɑssiflorɑ edulis Sims[J] . Plants,2025,14(5):645.
[40] 赵鑫悦,谢婧蘅,王天,杨莉,胡威,宋杰,匡柳青,刘勇,刘德春. 甜橙AP2亚家族转录因子的鉴定与分析[J] . 果树学报,2024,41(8):1490-1503.ZHAO Xinyue,XIE Jingheng,WANG Tian,YANG Li,HU Wei,SONG Jie,KUANG Liuqing,LIU Yong,LIU Dechun.Identification and analysis of AP2 subfamily transcription factors in sweet orange (Citrus sinensis)[J] . Journal of Fruit Science,2024,41(8):1490-1503.
[41] JIANG Q,WANG Z,HU G M,YAO X H. Genome-wide identification and characterization of AP2/ERF gene superfamily during flower development in Actinidiɑ eriɑnthɑ[J] . BMC Genomics,2022,23(1):650.
[42] LICAUSI F,GIORGI F M,ZENONI S,OSTI F,PEZZOTTI M,PERATA P. Genomic and transcriptomic analysis of the AP2/ERF superfamily in Vitis viniferɑ[J] . BMC Genomics,2010,11:719.
[43] XIE X L,SHEN S L,YIN X R,XU Q,SUN C D,GRIERSON D,FERGUSON I,CHEN K S. Isolation,classification and transcription profiles of the AP2/ERF transcription factor superfamily in citrus[J] . Molecular Biology Reports,2014,41(7):4261-4271.
[44] YE P Q,CHE X L,LIU Y,ZENG M,GUO W B,LONG Y B,LIU T Y,WANG Z. Genome-wide identification and characterization of the AP2/ERF gene family in loblolly pine (Pinus tɑedɑ L.)[J] . PeerJ,2024,12:e17388.
[45] 高华奇,王立芹,孙翠,黄凌霞. 采后跃变型果实软化与果胶降解的研究进展[J] . 果树学报,2022,39(10):1922-1934.GAO Huaqi,WANG Liqin,SUN Cui,HUANG Lingxia. Research progress on postharvest fruit softening and pectin degradation in climacteric fruits[J] . Journal of Fruit Science,2022,39(10):1922-1934.
[46] 温波,王亚兰,何丽丽,张峰,BOON-EK Y,柳士勇. 桃果胶裂解酶编码基因PpPL1的鉴定及其在果实成熟软化过程中的表达[J] . 核农学报,2020,34(8):1681-1689.WEN Bo,WANG Yalan,HE Lili,ZHANG Feng,BOON-EK Y,LIU Shiyong. Identification of peach pectate lyase coding gene PpPL1 and its expression during fruit ripening and softening[J] .Journal of Nuclear Agricultural Sciences,2020,34(8):1681-1689.
[47] LI C,XU M X,CAI X,HAN Z G,SI J P,CHEN D H. Jasmonate signaling pathway modulates plant defense,growth,and their trade-offs[J] . International Journal of Molecular Sciences,2022,23(7):3945.
[48] KAVI KISHOR P B,JR TIOZON R N,FERNIE A R,SREENIVASULU N. Abscisic acid and its role in the modulation of plant growth,development,and yield stability[J] . Trends in Plant Science,2022,27(12):1283-1295.