葡萄(Vitis viniferɑ L.)是葡萄科葡萄属多年生藤本植物,适应性强,栽培范围广。目前葡萄育种的主要途径是杂交育种,即通过双亲基因重组产生有利遗传效应,使后代兼具双亲的优良性状。现代分子生物学技术为利用与目标性状紧密关联的分子标记进行亲本筛选及杂种后代预鉴定提供了可能[1-2]。竞争性等位基因特异性PCR(kompetitive allele specific PCR,KASP)作为新一代的高通量自动化单核苷酸多态性(single nucleotide polymorphism,SNP)检测技术[3],具有速度快、准确度高等特点,已经广泛应用于小麦[4-5]、玉米[6]、水稻[7]、葡萄[8]等农作物中。Nguyen等[9]利用288个SNP对188个南瓜材料(包括杂交品种、自交品种及本地品种)进行基因分型与品种分类;在苹果中也开发了诸多不同性状的KASP标记[10];在葡萄中已经利用SNP标记对欧亚种葡萄进行品种鉴定,并确定了鉴定品种的标准位点[11]。利用KASP标记可以提高分子检测的可视化程度,推动作物分子育种的进程[12]。植物叶片(叶片大小)、果实(果实大小、果实硬度、果实糖含量、总酚含量及类黄酮含量等)等性状是多基因控制的性状[13-14],由复杂的基因网络调控。尽管KASP标记在多种作物中已成功应用,但针对葡萄叶片与果实性状的KASP标记研究仍较为匮乏。本研究通过对阳光玫瑰(Vitis viniferɑ×V. lɑbruscɑ ‘Shine Muscat’)×寒香蜜(V. viniferɑ×V. lɑbruscɑ ‘Suffolk Red’)杂交群体开展全基因组重测序,系统开发葡萄全基因组KASP标记,并筛选与叶片大小、果实性状显著关联的分子标记,为葡萄分子标记辅助育种提供技术支撑。
1 材料和方法
1.1 材料
阳光玫瑰×寒香蜜杂交群体:该群体于2018年进行杂交,种植于浙江省农业科学院杨渡科研基地,常规栽培管理。2023—2024年调查葡萄叶片与果实性状,选取150株杂交后代连同双亲委托北京诺禾致源科技股份有限公司进行全基因组重测序。
1.2 方法
1.2.1 DNA提取和PCR扩增 采用常规的CTAB法,提取阳光玫瑰、寒香蜜及其150株杂交后代新梢嫩叶的DNA,并检测DNA质量与浓度,采用Nano-Drop2000测定DNA浓度,1%琼脂糖凝胶电泳检测完整性,10 ng以上可较好地用于后续试验。PCR反应体系依据PARMS master mix说明书,20 μL反应体系含10 μL PARMS master mix、0.6 μL引物混合液(正向/反向引物各10 μmol·L-1)、2 μL DNA模板(10 ng·μL-1),ddH2O补足至20 μL。循环参数需根据引物和DNA浓度优化,采用35个循环实现高效分型。
1.2.2 荧光扫描 以FAM和HEX作为报告荧光,ROX作为参比荧光,利用Tecan F200多功能酶标仪进行荧光信号采集,检测通道覆盖上述3种荧光标记,实现基因型的高通量分析。
1.2.3 DNA文库构建及全基因组重测序 DNA样品检测合格后,通过Covaris超声破碎仪处理,获得350 bp左右的片段,采用NEB Next® Ultra™ Ⅱ DNA Library Prep Kit构建测序文库,流程包括末端修复、加ployA尾、接头连接、纯化及PCR扩增。构建完成的文库通过PE150模式在Illumina平台进行测序。
1.2.4 核心SNP标记筛选开发 对SNP分子进行筛选[15-17]:①深度过滤。单样本平均测序深度>9X,过滤掉低深度位点。②完整度过滤。筛选基因型覆盖≥95%的群体个数的标记。过滤掉MAF(最小等位基因频率)值低于0.1的位点、PIC(多态性信息含量)小于0.25的位点、HET(SNP杂合型率)值大于0.3的位点。③根据SNP位点的功能注释,筛选nonsynonymous、stopgain、stoploss变异的SNP位点。④非染色体过滤:去除掉scaffold上的SNP位点,只保留Chr上的SNP位点。⑤位置过滤:去除掉前后位置距离小于3 Mb的位点。
1.2.5 叶片表型测量及果实生理指标的测定 于2023—2024年7—8月采集父母本及150株后代的葡萄枝条第6节叶片及成熟果实样品,采用游标卡尺测量叶片的叶长、叶宽,并计算出叶片的叶面积(叶长×叶宽)。用电子天平测定果实单粒质量,使用游标卡尺测量果粒的横纵径;果实的硬度使用CT-3质构仪(美国Brookfield)进行测定,将果实中心位置置于探头正下方测定,设置3次重复;总酚、类黄酮含量参照曹建康等[18]的比色法测定;果实中糖组分含量按照Komatsu等[19]方法,用液相色谱仪(Waters公司,美国)测定,Water e2695-2414系统,Sugar-RakTM1色谱柱(6.5 mm×300 mm),流动相为超纯水,流速为0.5 mL·min-1。
1.2.6 数据处理分析 使用Excel 2019对数据进行统计整理,用SPSS 27.0软件处理性状数据,对数据进行方差分析、相关性分析和描述统计,并采用Origin 2022作图。
2 结果与分析
2.1 葡萄全基因组重测序和群体SNP检测
通过测序平台对阳光玫瑰和寒香蜜及其150个杂交后代进行全基因组重测序,共得到819 Gb高质量碱基(Clean Base),其中,阳光玫瑰的高质量碱基数为10.25 Gb,寒香蜜高质量碱基数为10.02 Gb,150个杂交后代高质量碱基总数为799 Gb。Q30均超过90%,GC含量均超过33%(表1)。通过BWA软件将测序数据与参考基因组比对,双亲及杂交后代的比对率分别为97.79%、96.79%和97.25%(表2),表明数据质量满足SNP分析要求。
表1 重测序数据汇总
Table 1 Summary of the resequencing data
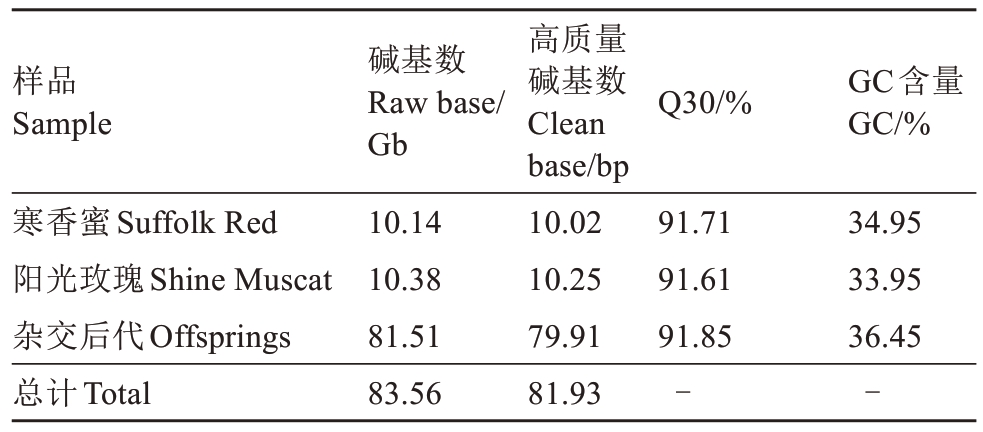
样品Sample Q30/%GC含量GC/%寒香蜜Suffolk Red阳光玫瑰Shine Muscat杂交后代Offsprings总计Total碱基数Raw base/Gb 10.14 10.38 81.51 83.56高质量碱基数Clean base/bp 10.02 10.25 79.91 81.93 91.71 91.61 91.85-34.95 33.95 36.45-
表2 测序深度及覆盖度统计
Table 2 Statistics of sequencing depth and coverage
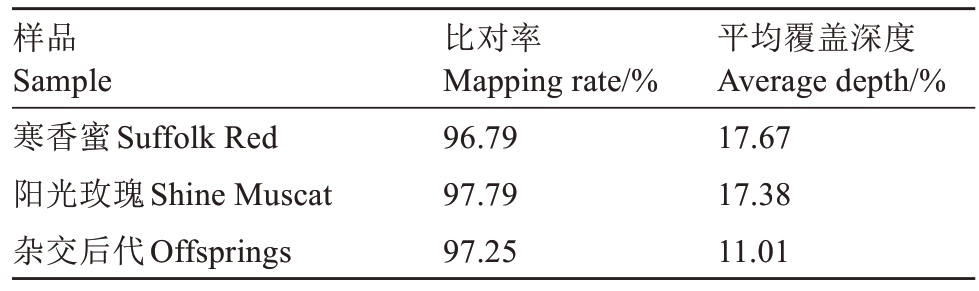
样品Sample寒香蜜Suffolk Red阳光玫瑰Shine Muscat杂交后代Offsprings比对率Mapping rate/%96.79 97.79 97.25平均覆盖深度Average depth/%17.67 17.38 11.01
2.2 SNP检测与功能注释
ANNOVAR能利用最新信息对由多个基因组检测出的基因变异进行功能注释[20]。结果表明,SNP变异位点以转换(ts)为主,颠换(tv)约占32.19%,碱基发生转换的频率是颠换的2.1倍。
对SNP检测结果注释的基因结构分布区域进行分析,结果(图1-A)显示,148 379个SNP位点分布在基因间区,214 504个SNP位点分布于基因区。对基因区的SNP位点进行分析,7292个SNP位点位于基因上游1 kb区域,11 136个SNP位点位于基因下游1 kb区域,有202个SNP位点变异于剪接位点,变异于内含子区域的SNP位点有109 303个,变异于外显子区域的SNP位点则有68 792个,而分布在其他区域的SNP位点有19 027个。针对变异于外显子区域的SNP位点(图1-B),有32 550个导致同义变异,34 961个导致非同义变异,有658个位点使基因获得终止密码子,此外有39个SNP位点使基因失去终止密码子。
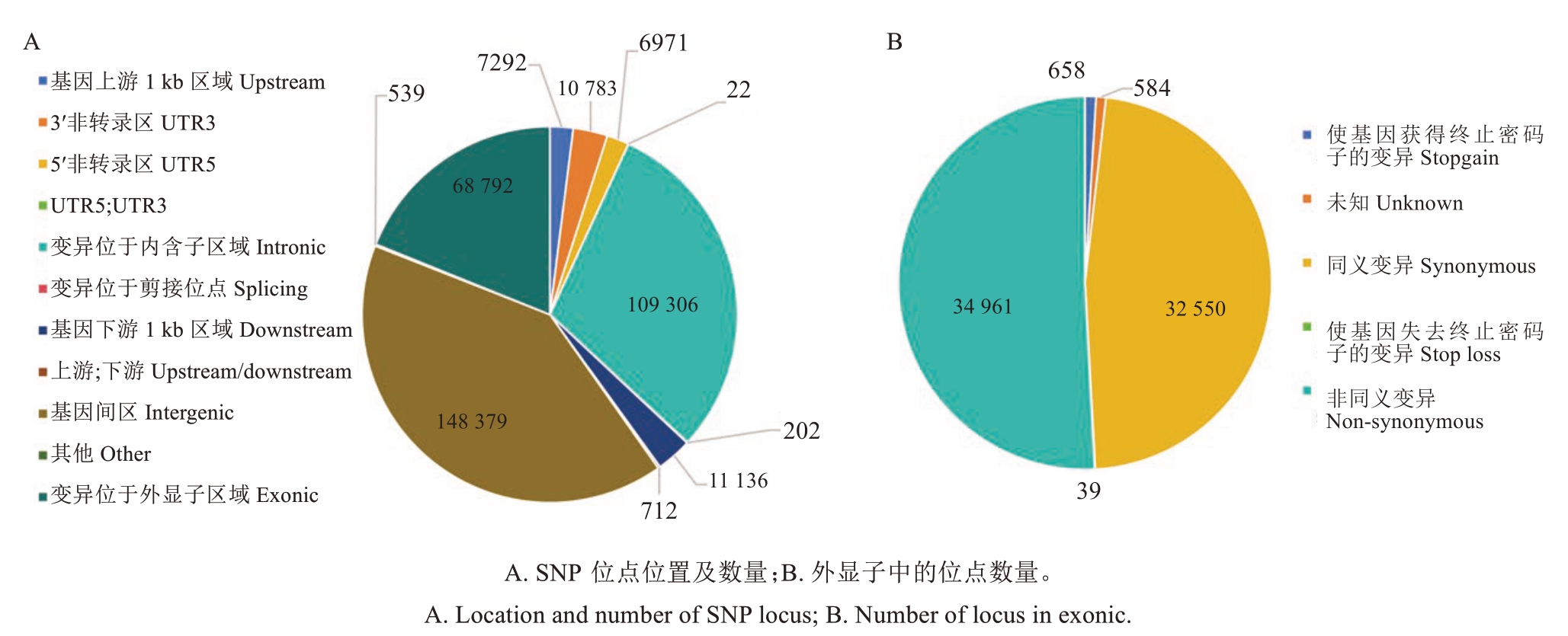
图1 SNP位点分布注释分析结果
Fig. 1 Annotation analysis results of SNP locus distribution
2.3 杂交群体遗传结构分析
基于对开发的KSAP标记进行杂交群体分析,通过主成分分析(图2-A),可以得到统一PC1贡献率为10.39%,没有明显的主成分能够区分杂交后代。由于该群体为杂交群体,有共同亲本,且遗传性状相似,所以并不易区分。利用系统发育分析杂交后代之间的关系(图2-B),显示双亲及150个后代中有7个后代与父本寒香蜜组成一个分支,有6个后代与母本阳光玫瑰组成一个分支,关系比较密切,其余后代分为其他分支,说明了杂交后代间存在一定的遗传变异。
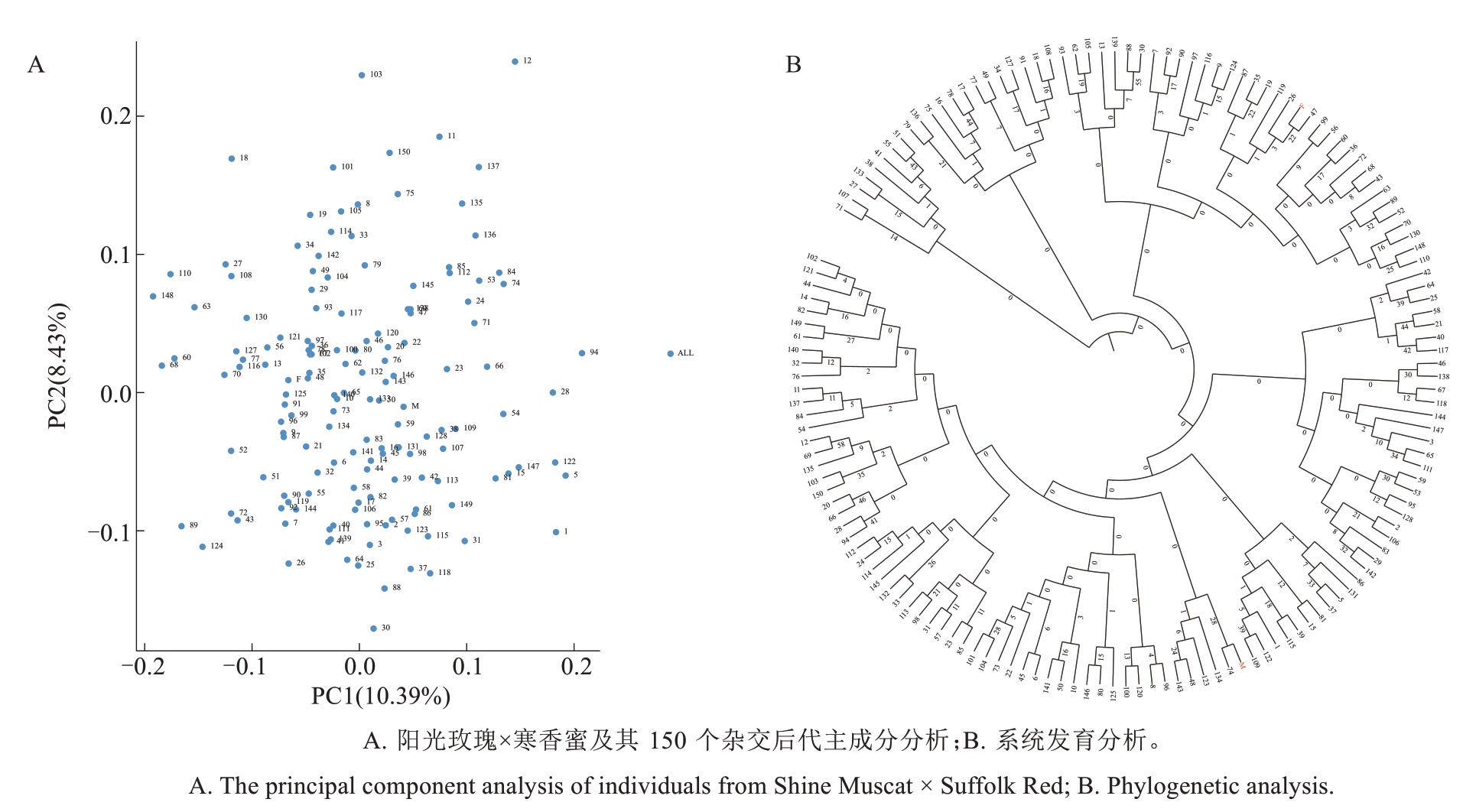
图2 阳光玫瑰×寒香蜜及其杂交后代亲缘关系遗传结构分析
Fig. 2 Genetic structure analyses depicting the relationships among hybrids of Shine Muscat × Suffolk Red
2.4 核心SNP标记筛选
依据深度(>9X)、完整度(≥95%)、遗传参数(MAF≥0.1,PIC≥0.25,HET≤0.3)及功能注释等标准,最终筛选获得74个核心SNP位点。其缺失率为0.010~0.055,MAF主要分布于0.15~0.19,PIC为0.260~0.295,杂合型率为0.275~0.300(图3)。
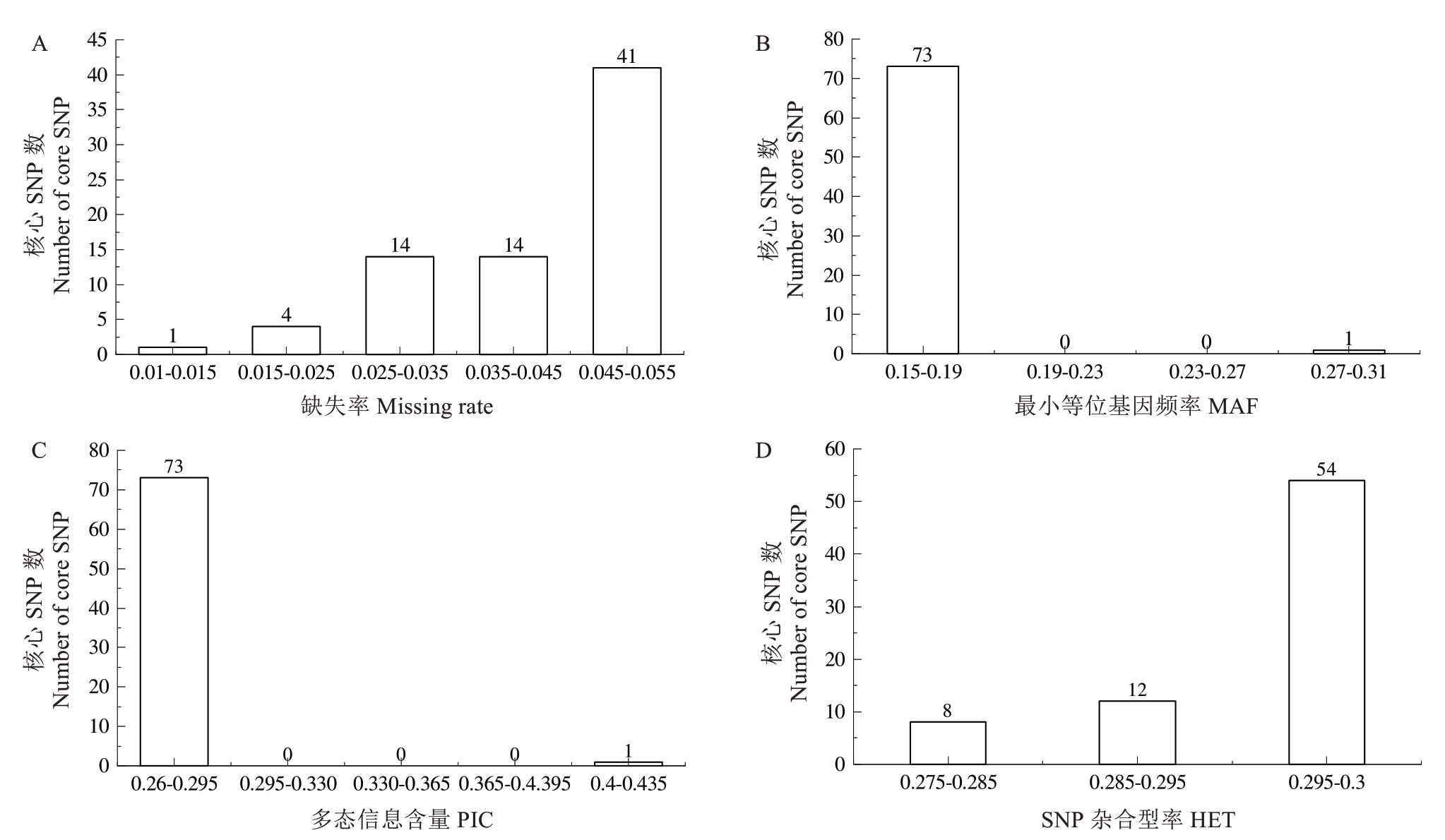
图3 74个SNP核心位点的缺失率(A)、最小等位基因频率(B)、多态信息含量(C)和SNP杂合型率(D)
Fig. 3 Missing rate (A), MAF (B), PIC (C) and HET (D) of 74 SNP loci
2.5 KASP标记开发与验证
对43个样本进行位点的开发,待开发的点位有21个,其中有2个标记(NC_081805.1_15375754、NC_081808.1_22289816)无法进行引物设计,其余19个KASP标记在43个样品中成功地进行了引物设计。根据试验的验证结果,共成功开发19个KASP位点,其染色体分布位置如图4所示。其中杂合率为0.295~0.300的有14个,占比73.7%;缺失率为0.048~0.055的有10个,占比52.6%;遗传多样性指数大多分布于0.250~0.287;PIC值大多分布于0.260~0.295(图5)。
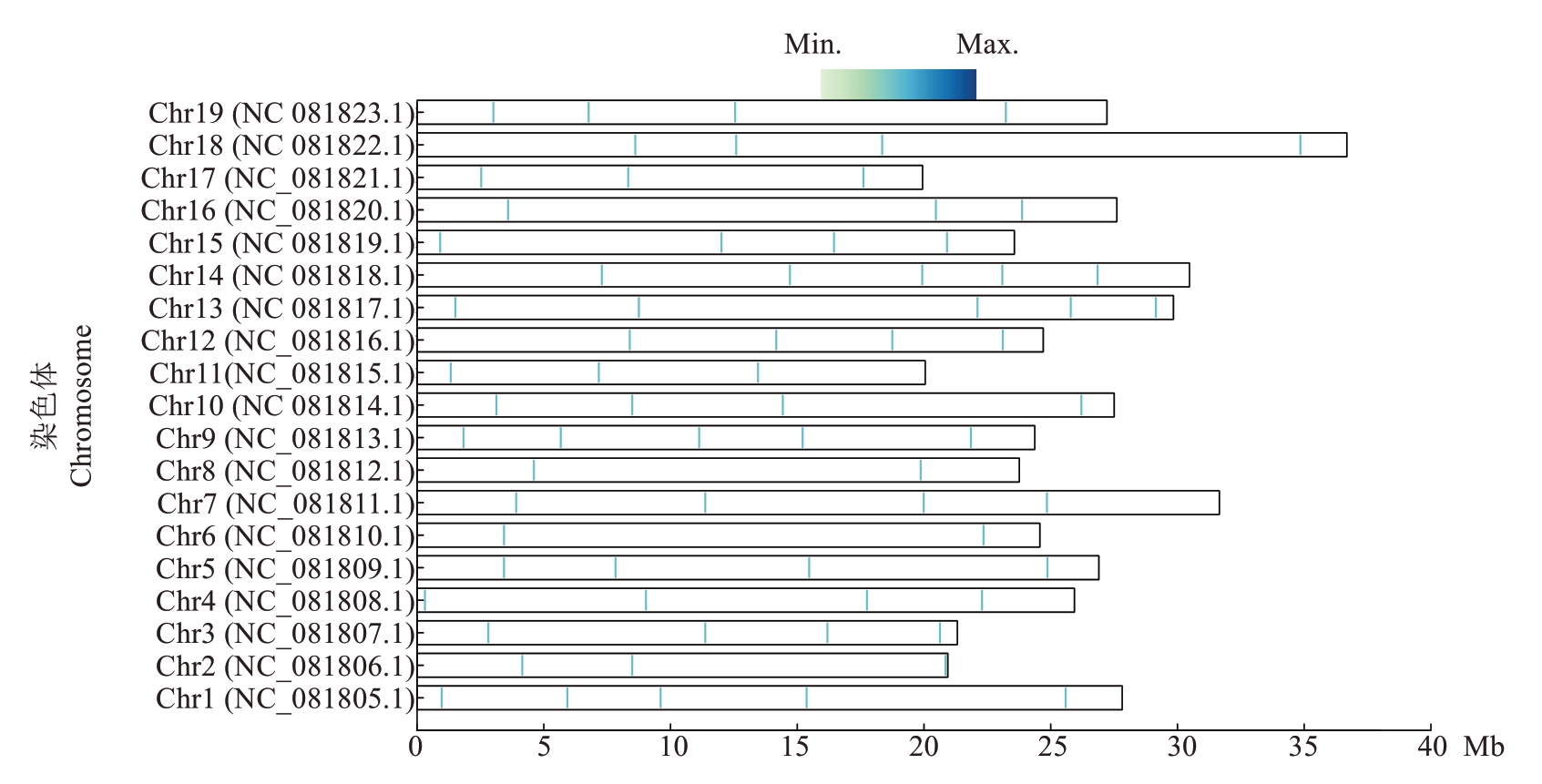
图4 核心SNP标记在染色体上的分布图
Fig. 4 Distribution of core SNP in chromosome
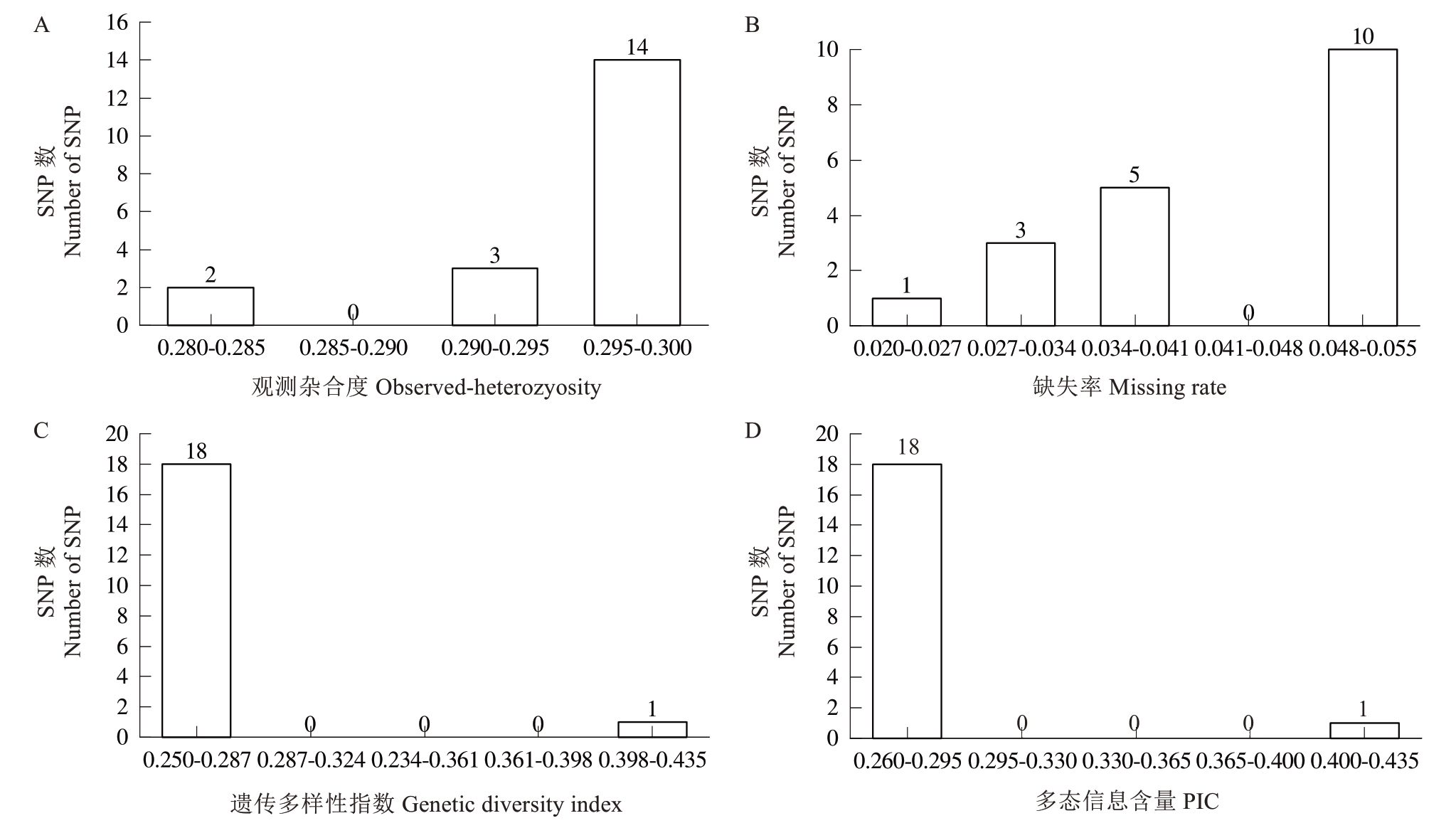
图5 19个KASP标记的观测杂合度(A)、缺失率(B)、遗传多样性指数(C)和多态信息含量(D)变化分布
Fig. 5 Observed-heterozyosity (A), missing rate (B), genetic diversity index (C) and PIC (D) of 19 KASP makers
2.6 KASP标记基因富集分析
为全面了解基因功能信息,基于阳光玫瑰和寒香蜜及其150个杂交后代全基因组重测序数据,在GO数据库中注释到6631个候选基因(图6),在KEGG数据库中注释到9个基因。图7为KEGG差异基因富集最显著的几个途径,其中黄酮和黄酮醇的生物合成的富集因子为0.045,其他的依次为果糖和甘露糖代谢,戊糖和葡萄糖醛酸的相互转换,植物-病原体的相互作用。这些通路可以为果糖、葡萄糖含量和总酚、类黄酮含量等相关性状的研究提供参考。
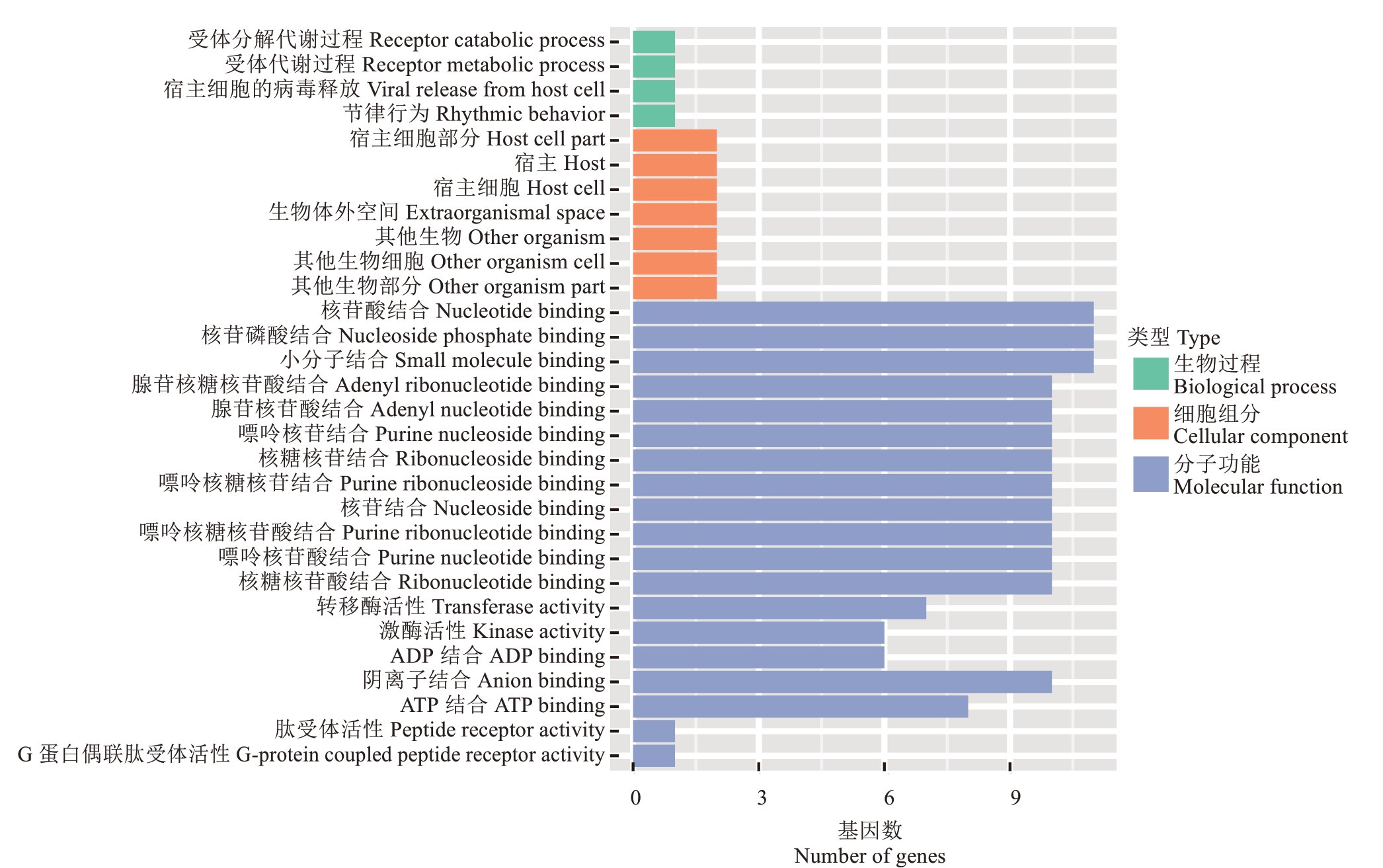
图6 KASP标记所在基因的GO分类注释
Fig. 6 GO classification of putative functions of the genes for KASP makers
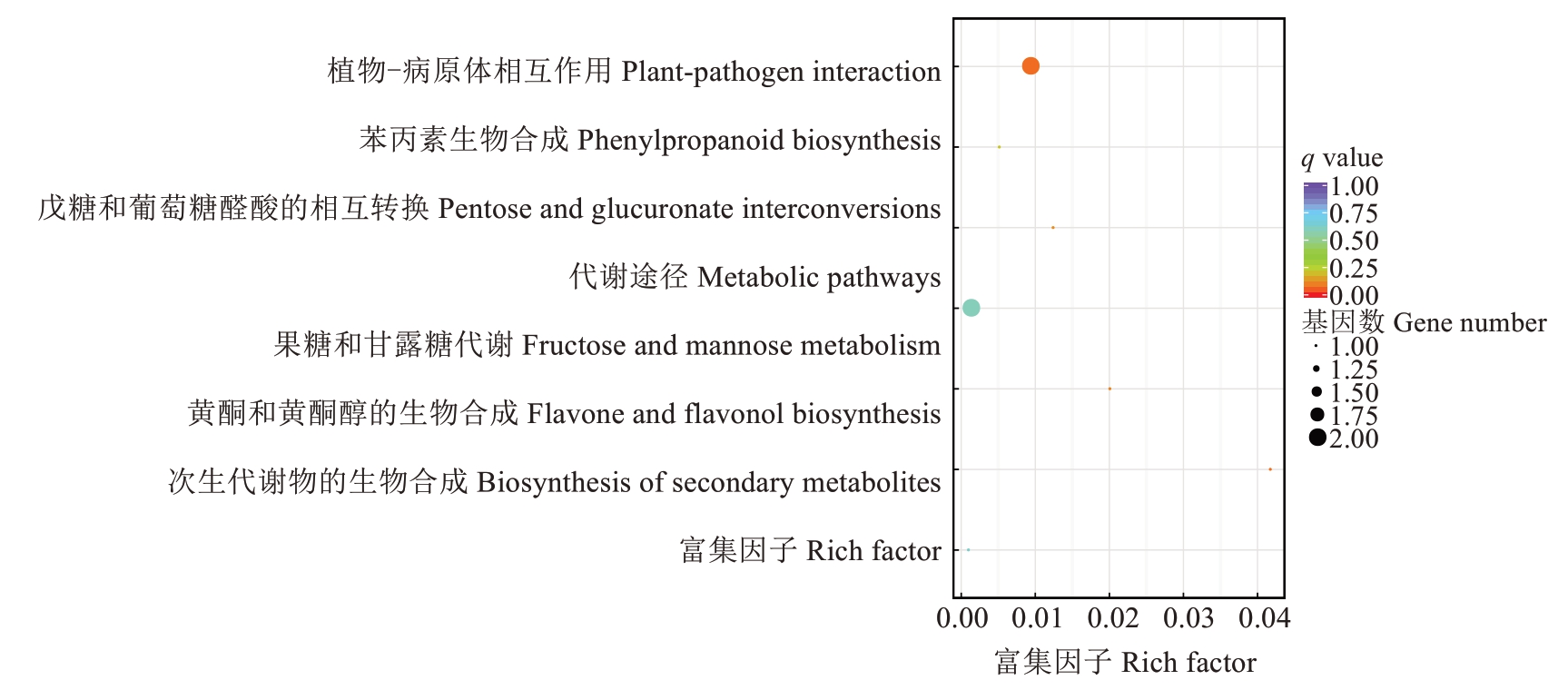
图7 KASP标记所在基因的KEGG富集分析
Fig. 7 KEGG enrichment analysis of the genes for KASP makers
2.7 叶片与果实性状关联分析
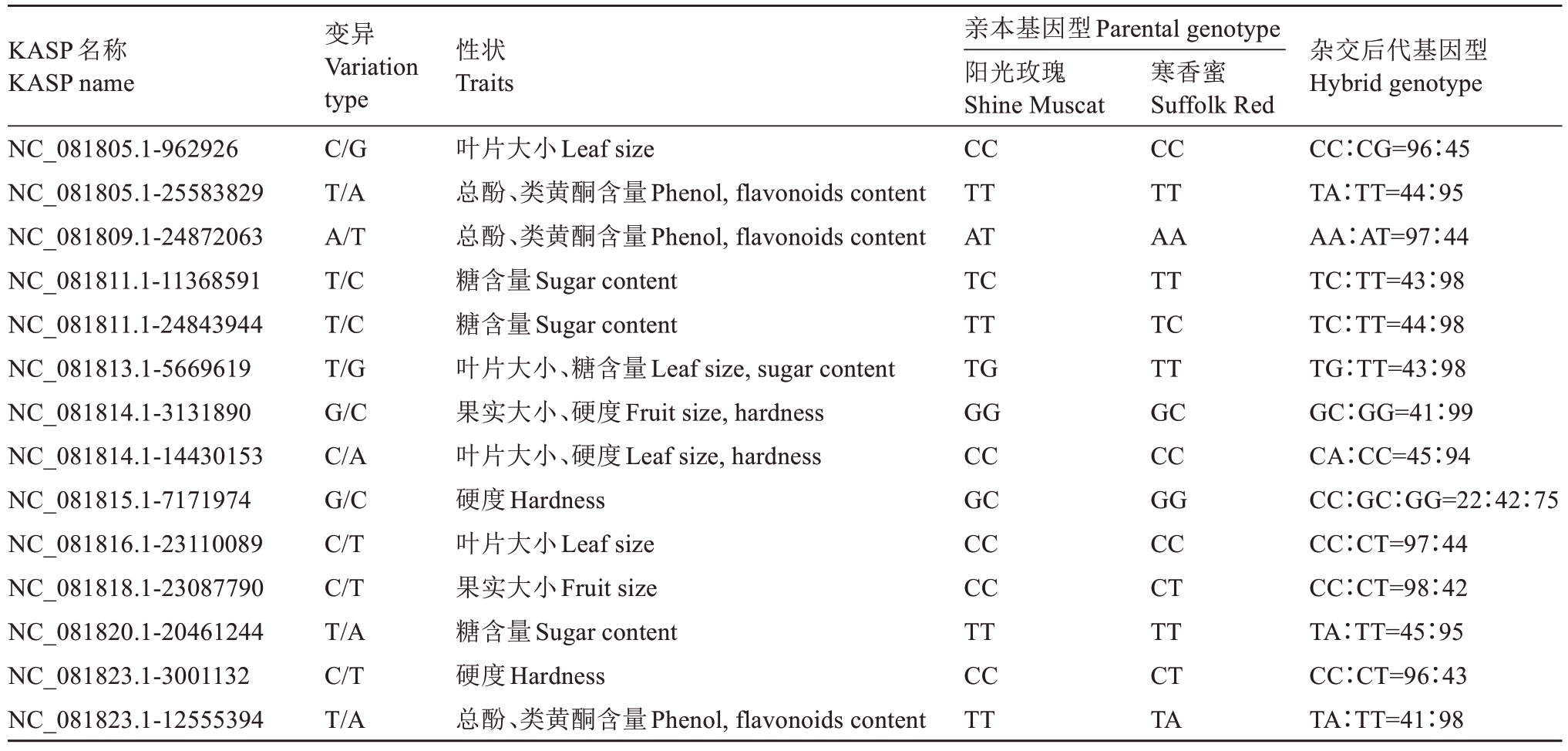
对父母本及150株后代进行性状关联分析,结果表明(表3),阳光玫瑰与寒香蜜在叶面积(532.35 cm2 vs 313.50 cm2)、果实纵径(2.80 cm vs 1.30 cm)、粒质量(8.46 g vs 2.32 g)等性状上存在显著差异,其杂交后代性状分离广泛,叶面积变异系数达40.63%,总酚(30.53%)和粒质量(28.35%)次之,而果糖变异系数最低(9.55%),且叶长、叶宽、粒质量等性状呈正态分布,表明这些性状可能受多基因调控。结合表4筛选的14个KASP标记分析,与叶片大小相关的4个标记,如NC_081805.1-962926,在双亲中均为纯合基因型(CC∶CC),杂交后代中CC∶CG基因型分离比为96∶45,暗示该标记可能与叶面积的显性遗传相关;2个果实大小相关标记,如NC_081818.1-23087790,在双亲中呈现CC∶CT的基因型差异,后代中CC∶CT分离比为98∶42,表明可能与果实纵径的遗传分化有关。
表3 阳光玫瑰×寒香蜜杂交群体叶片表型及果实性状的统计分析
Table 3 Analysis of leaf and fruit traits in hybrid population from Shine Muscat × Suffolk Red
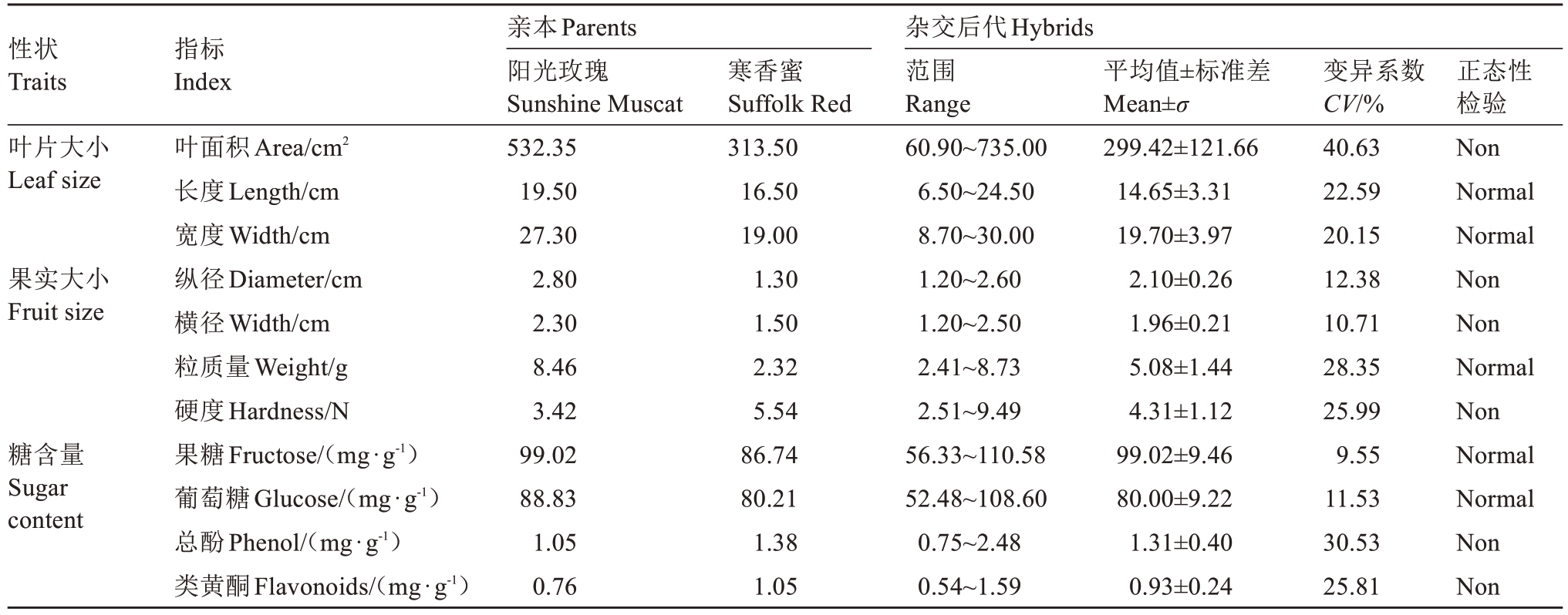
注:Non和Normal表示不同性状和生理指标的正态性检验结果,Non代表非正态分布,Normal代表正态分布(P>0.05)。
Note:Non and Normal represent non-normal distribution and normal distribution for different traits and physiological indices (P>0.05).
性状Traits叶片大小Leaf size果实大小Fruit size糖含量Sugar content指标Index叶面积Area/cm2长度Length/cm宽度Width/cm纵径Diameter/cm横径Width/cm粒质量Weight/g硬度Hardness/N果糖Fructose/(mg·g-1)葡萄糖Glucose/(mg·g-1)总酚Phenol/(mg·g-1)类黄酮Flavonoids/(mg·g-1)亲本Parents阳光玫瑰Sunshine Muscat 532.35 19.50 27.30 2.80 2.30 8.46 3.42 99.02 88.83 1.05 0.76正态性检验Non Normal Normal Non Non Normal Non Normal Normal Non Non寒香蜜Suffolk Red 313.50 16.50 19.00 1.30 1.50 2.32 5.54 86.74 80.21 1.38 1.05杂交后代Hybrids范围Range 60.90~735.00 6.50~24.50 8.70~30.00 1.20~2.60 1.20~2.50 2.41~8.73 2.51~9.49 56.33~110.58 52.48~108.60 0.75~2.48 0.54~1.59平均值±标准差Mean±σ 299.42±121.66 14.65±3.31 19.70±3.97 2.10±0.26 1.96±0.21 5.08±1.44 4.31±1.12 99.02±9.46 80.00±9.22 1.31±0.40 0.93±0.24变异系数CV/%40.63 22.59 20.15 12.38 10.71 28.35 25.99 9.55 11.53 30.53 25.81
表4 14个与叶片及果实性状关联的KASP标记
Table 4 14 KASP markers related to leaf and fruit traits
KASP名称KASP name性状Traits杂交后代基因型Hybrid genotype NC_081805.1-962926 NC_081805.1-25583829 NC_081809.1-24872063 NC_081811.1-11368591 NC_081811.1-24843944 NC_081813.1-5669619 NC_081814.1-3131890 NC_081814.1-14430153 NC_081815.1-7171974 NC_081816.1-23110089 NC_081818.1-23087790 NC_081820.1-20461244 NC_081823.1-3001132 NC_081823.1-12555394变异Variation type C/G T/A A/T T/C T/C T/G G/C C/A G/C C/T C/T T/A C/T T/A叶片大小Leaf size总酚、类黄酮含量Phenol, flavonoids content总酚、类黄酮含量Phenol, flavonoids content糖含量Sugar content糖含量Sugar content叶片大小、糖含量Leaf size, sugar content果实大小、硬度Fruit size, hardness叶片大小、硬度Leaf size, hardness硬度Hardness叶片大小Leaf size果实大小Fruit size糖含量Sugar content硬度Hardness总酚、类黄酮含量Phenol, flavonoids content亲本基因型Parental genotype阳光玫瑰Shine Muscat CC TT AT TC TT TG GG CC GC CC CC TT CC TT寒香蜜Suffolk Red CC TT AA TT TC TT GC CC GG CC CT TT CT TA CC∶CG=96∶45 TA∶TT=44∶95 AA∶AT=97∶44 TC∶TT=43∶98 TC∶TT=44∶98 TG∶TT=43∶98 GC∶GG=41∶99 CA∶CC=45∶94 CC∶GC∶GG=22∶42∶75 CC∶CT=97∶44 CC∶CT=98∶42 TA∶TT=45∶95 CC∶CT=96∶43 TA∶TT=41∶98
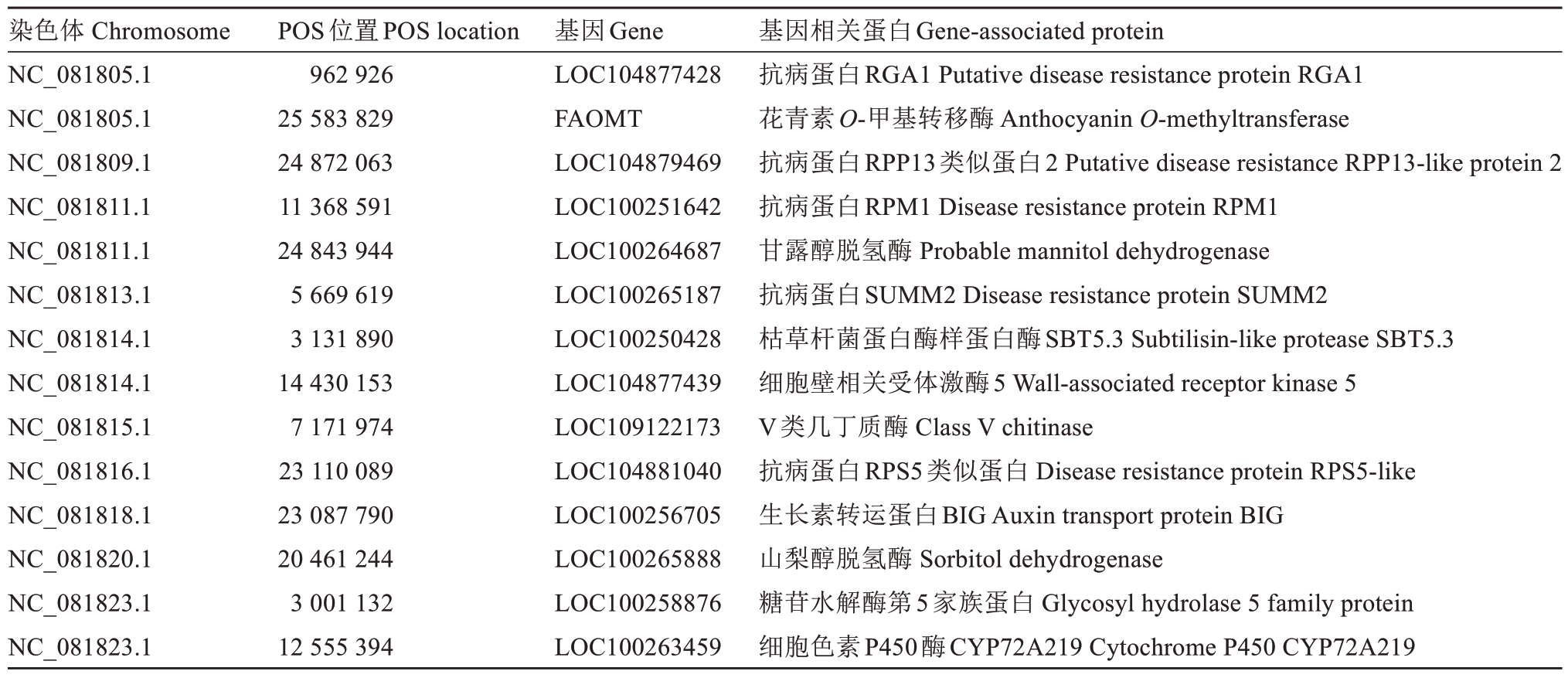
与糖含量相关的4个标记,如NC_081820.1-20461244,在双亲中均为TT纯合型,后代中TA∶TT分离比为45∶95,结合表3中果糖和葡萄糖的正态分布特征与标记所在基因注释结果(表5),推测这些标记可能与山梨醇脱氢酶、甘露醇脱氢酶等糖代谢关键基因关联,参与果糖-葡萄糖的转化调控。3个总酚/类黄酮相关标记,如NC_081805.1-25583829,在后代中TA∶TT分离比为44∶95,其所在基因富集于黄酮和黄酮醇生物合成通路,与表3中总酚的高变异系数(30.53%)相呼应,暗示这些标记可能通过调控花青素、矢车菊素等合成,影响果实酚类物质积累。此外,果实硬度相关标记,如NC_081815.1-7171974的基因型分离与植物-病原体互作通路中的几丁质酶基因关联,可能通过影响细胞壁成分调控果实硬度。综上,表4中14个KASP标记与表3中性状的变异模式、遗传分布高度吻合,为葡萄叶片与果实性状的分子育种提供了可靠的标记工具。
表5 相关标记所在染色体位置对应的基因信息
Table 5 Information about the gene corresponding to the chromosomal location of the markers
染色体 Chromosome NC_081805.1 NC_081805.1 NC_081809.1 NC_081811.1 NC_081811.1 NC_081813.1 NC_081814.1 NC_081814.1 NC_081815.1 NC_081816.1 NC_081818.1 NC_081820.1 NC_081823.1 NC_081823.1 POS位置POS location 962 926 25 583 829 24 872 063 11 368 591 24 843 944 5 669 619 3 131 890 14 430 153 7 171 974 23 110 089 23 087 790 20 461 244 3 001 132 12 555 394基因Gene LOC104877428 FAOMT LOC104879469 LOC100251642 LOC100264687 LOC100265187 LOC100250428 LOC104877439 LOC109122173 LOC104881040 LOC100256705 LOC100265888 LOC100258876 LOC100263459基因相关蛋白Gene-associated protein抗病蛋白RGA1 Putative disease resistance protein RGA1花青素O-甲基转移酶 Anthocyanin O-methyltransferase抗病蛋白RPP13类似蛋白2 Putative disease resistance RPP13-like protein 2抗病蛋白RPM1 Disease resistance protein RPM1甘露醇脱氢酶 Probable mannitol dehydrogenase抗病蛋白SUMM2 Disease resistance protein SUMM2枯草杆菌蛋白酶样蛋白酶SBT5.3 Subtilisin-like protease SBT5.3细胞壁相关受体激酶5 Wall-associated receptor kinase 5 V类几丁质酶 Class V chitinase抗病蛋白RPS5类似蛋白 Disease resistance protein RPS5-like生长素转运蛋白BIG Auxin transport protein BIG山梨醇脱氢酶 Sorbitol dehydrogenase糖苷水解酶第5家族蛋白 Glycosyl hydrolase 5 family protein细胞色素P450酶CYP72A219 Cytochrome P450 CYP72A219
3 讨 论
基于阳光玫瑰和寒香蜜及其150个杂交后代全基因组重测序数据,本研究开发了全基因组KASP标记。通过KEGG富集分析发现,这些标记所关联的基因被显著富集到7个途径中,其中黄酮和黄酮醇的生物合成途径富集最为显著。黄酮与黄酮醇同属植物类黄酮,其生物合成过程主要受两种基因的控制:一种是直接编码类黄酮生物合成相关生物酶的结构基因,另一种是调控这些基因的转录因子,如MYB、bHLH、WD40等[21]。类黄酮作为植物中重要的次生代谢物,不仅具有清除活性氧自由基的抗氧化功能,还广泛参与植物的生长发育及逆境胁迫响应过程,同时也是植物色素的主要来源[22]。本研究筛选出了与黄酮和黄酮醇生物合成途径相关的KASP标记(NC_081805.1-25583829、NC_081823.1-12555394等),结合杂交后代总酚含量变异系数30.53%以及目标性状的基因型分离(TA∶TT=44∶95、TA∶TT=41∶98)情况,表明这些标记所在基因可能通过调控花青素合成,影响果实色泽及酚类物质积累。矢车菊素糖苷在O-甲基转移酶(OMT)催化下甲基化生成芍药花素糖苷,对OMT表达的研究发现,其表达量与花色苷含量呈正相关,且在果实转色前没有表达,转色后表达量上调[23]。据Pan等[24]的研究,常见的花青素包括了矢车菊素、矮牵牛素、芍药花素等,但由于花青素具有不稳定的特点,所以细胞中的花青素通常以糖基化后的花色苷的形式存在。有研究表明花青素是黄酮类多酚水溶性化合物,在果实成熟过程中经苯丙烷代谢途径合成,不仅是果实的主要色素,同时也是植物中重要的营养成分[25-26],例如,苹果中MdGSTF6被MdMYB1激活并参与花青素积累[26],这暗示葡萄中可能存在类似调控机制。
果糖、葡萄糖、蔗糖、山梨醇是水果中常见的几种可溶性糖,其中,果糖占比最大,其次是葡萄糖[27]。果实糖代谢是一个复杂的过程,糖的积累过程由多种酶共同调节,可溶性糖在运输、积累、转化中由多种代谢相关酶共同调节。进入果实的山梨醇会被代谢酶分解,与山梨醇代谢相关的酶主要有山梨醇脱氢酶(SDH)、山梨醇转化酶(SOX),这些酶主要促进山梨醇向葡萄糖和果糖的转化[28]。Berüter等[29]证明了在叶片中合成的山梨醇,通过“源-库”关系进入到果实的细胞质中,经SDH和SOX这两种关键酶不可逆的降解。Berüter等[29]还在苹果中发现糖分积累主要以山梨糖醇和蔗糖的形式输入,但这一机制是否适用于葡萄,还需要进一步验证。本研究筛选到与果糖、葡萄糖相关的KASP标记(NC_081811.1-24843944、NC_081820.1-20461244等),这些标记均与相关的代谢酶有关,NC_081811.1-24843944标记位于山梨醇脱氢酶基因编码区,其T/C变异可能影响酶活性,进而调控山梨醇向果糖的转化。甘露醇脱氢酶(MDH)将甘露醇转化为果糖,山梨醇脱氢酶将山梨醇转化为葡萄糖,催化山梨醇脱氢生成果糖,是调控生物体内山梨醇含量的关键酶之一。MDH是催化甘露醇与果糖之间氧化还原反应的关键酶,由于甘露糖和果糖为同分异构体,在一定条件下,果糖可以经过异构反应转变为葡萄糖和甘露糖[30],表明这些KASP标记所在的基因与控制果糖、葡萄糖类的合成有关。
植物与病原体之间的相互作用是一个复杂的生物学过程,决定了植物体是否会被感染以及是否能抵抗病原体。植物通过受体识别病原体的相关分子模式,触发PTI(模式触发免疫),病原体则通过分泌效应蛋白抑制PTI以促进感染,植物进化出抗病蛋白,可以识别出特定的效应蛋白,激活更强的ETI(效应子触发免疫),但这一过程常常伴随一些负面作用,如局部细胞死亡。本研究筛选出了与植物-病原体相互作用有关的KASP标记(NC_081806.1-20851617、NC_081805.1-962926、NC_081815.1-7171974、NC_081823.1-3001132等),这些标记所对应的基因不仅与相关抗病蛋白、糖基水解酶家族和几丁质酶有关,还与果实的硬度有关。几丁质酶作为一种重要的糖苷酶,在植物抗生物胁迫及干旱、高盐等非生物胁迫过程中发挥重要作用,部分植物的几丁质酶有利于植物与微生物共生体系的建立。有研究表明,几丁质酶通过降解几丁质可以削弱昆虫外骨骼的完整性和稳定性,还能干扰昆虫的生理过程及消化系统,从而增强植物对昆虫的抗性,甚至导致昆虫的死亡[31-32]。干旱会诱导辣椒中几丁质酶相关基因的表达,过表达几丁质酶基因的植株具有更强的抗病性和对环境胁迫的耐受性[33]。糖基水解酶(glycoside hydrolase,GH)是一类催化糖苷键水解的酶,广泛参与植物与病原体的相互作用,既是植物的防御武器,也是病原体的入侵工具。GH5家族是许多活体营养、半活体营养和死体营养真菌和卵菌中最大的糖苷水解酶家族(GH家族)之一。有研究表明,GH12家族蛋白在大豆疫霉菌侵染的过程中,不仅发挥毒力因子的作用,还能够作为激发子使植物产生一系列的免疫反应[34]。不同抗病蛋白对植物抗病性的影响存在差异,植物抗病性增强可以减少病原侵染对叶片造成的损伤,从而维持叶片大小。本研究中与植物-病原体互作相关的标记(如NC_081805.1-962926)同时关联叶片大小,表明抗病通路可能通过维持细胞完整性间接影响叶片发育。生长素的极性运输会影响植物叶片的扩展,生长素不足可能会造成叶片面积减小[35]。此外,已开发的KASP标记所在的基因是否参与叶片大小、果实大小、果实硬度等性状的调控还需进一步深入研究。
4 结 论
通过对阳光玫瑰、寒香蜜及其150株杂交后代的全基因组重测序,共检测到432 926个SNP位点。经深度、完整度及遗传参数过滤,获得74个核心SNP位点,成功开发19个KASP标记。结合叶片与果实性状关联分析,筛选出14个功能标记,其中4个与叶片形态相关,2个关联果实大小,4个涉及果糖/葡萄糖代谢,3个与总酚/类黄酮合成相关。KEGG分析表明,这些标记所在基因(NC_081805.1-25583829、NC_081823.1-12555394等)显著富集于黄酮和黄酮醇生物合成通路(P<0.01),是研究果实色泽与品质调控的分子靶点。本研究开发的KASP标记可用于葡萄育种早期性状筛选,为分子标记辅助育种提供了技术支撑。
[1] FLACHOWSKY H,LE ROUX P M,PEIL A,PATOCCHI A,RICHTER K,HANKE M V. Application of a high-speed breeding technology to apple/(Mɑlus × domesticɑ) based on transgenic early flowering plants and marker-assisted selection[J] . New Phytologist,2011,192(2):364-377.
[2] FLACHOWSKY H,PEIL A,SOPANEN T,ELO A,HANKE V.Overexpression of BpMADS4 from silver birch (Betulɑ pendulɑ Roth.) induces early-flowering in apple /(Mɑlus × domesticɑ Borkh.)[J] . Plant Breeding,2007,126(2):137-145.
[3] 隋建枢,陈天青,罗永露,吴文强,程斌,王伟,何庆才. 75份贵州小麦品种(系)抗病基因的KASP标记检测[J] . 山地农业生物学报,2023,42(3):80-85.SUI Jianshu,CHEN Tianqing,LUO Yonglu,WU Wenqiang,CHENG Bin,WANG Wei,HE Qingcai. KASP marker assays for resistance genes in 75 wheat cultivars (lines) in Guizhou[J] . Journal of Mountain Agriculture and Biology,2023,42(3):80-85.
[4] LI P R,SU T B,WANG H P,ZHAO X Y,WANG W H,YU Y J,ZHANG D S,WEN C L,YU S C,ZHANG F L. Development of a core set of KASP markers for assaying genetic diversity in Brɑssicɑ rɑpɑ subsp. chinensis Makino[J] . Plant Breeding,2019,138(3):309-324.
[5] GREWAL S,HUBBART-EDWARDS S,YANG C Y,DEVI U,BAKER L,HEATH J,ASHLING S,SCHOLEFIELD D,HOWELLS C,YARDE J,ISAAC P,KING I P,KING J. Rapid identification of homozygosity and site of wild relative introgressions in wheat through chromosome-specific KASP genotyping assays[J] . Plant Biotechnology Journal,2020,18(3):743-755.
[6] 赵久然,李春辉,宋伟,王元东,张如养,王继东,王凤格,田红丽,王蕊. 基于SNP芯片揭示中国玉米育种种质的遗传多样性与群体遗传结构[J] . 中国农业科学,2018,51(4):626-634.ZHAO Jiuran,LI Chunhui,SONG Wei,WANG Yuandong,ZHANG Ruyang,WANG Jidong,WANG Fengge,TIAN Hongli,WANG Rui. Genetic diversity and population structure of important Chinese maize breeding germplasm revealed by SNPchips[J] . Scientia Agricultura Sinica,2018,51(4):626-634.
[7] YANG G L,CHEN S P,CHEN L K,SUN K,HUANG C H,ZHOU D H,HUANG Y T,WANG J F,LIU Y Z,WANG H,CHEN Z Q,GUO T. Development of a core SNP arrays based on the KASP method for molecular breeding of rice[J] . Rice,2019,12(1):21.
[8] 王富强,张建,温常龙,樊秀彩,张颖,孙磊,刘崇怀,姜建福.基于KASP标记的葡萄品种鉴定[J] . 中国农业科学,2021,54(13):2830-2846.WANG Fuqiang,ZHANG Jian,WEN Changlong,FAN Xiucai,ZHANG Ying,SUN Lei,LIU Chonghuai,JIANG Jianfu. Identification of grape cultivars based on KASP markers[J] . Scientia Agricultura Sinica,2021,54(13):2830-2846.
[9] NGUYEN N N,KIM M,JUNG J K,SHIM E J,CHUNG S M,PARK Y,LEE G P,SIM S C. Genome-wide SNP discovery and core marker sets for assessment of genetic variations in cultivated pumpkin (Cucurbitɑ spp.)[J] . Horticulture Research,2020,7:121.
[10] 郑文燕,常源升,何平,何晓文,王森,高文胜,李林光,王海波.‘鲁丽’ב红1#’苹果杂交群体全基因组KASP标记开发及验证[J] . 中国农业科学,2023,56(5):935-950.ZHENG Wenyan,CHANG Yuansheng,HE Ping,HE Xiaowen,WANG Sen,GAO Wensheng,LI Linguang,WANG Haibo. Development and validation of KASP markers based on a wholegenome resequencing approach in a hybrid population of ‘Luli’בRed No. 1’[J] . Scientia Agricultura Sinica,2023,56(5):935-950.
[11] CABEZAS J A,IBÁÑEZ J,LIJAVETZKY D,VÉLEZ D,BRAVO G,RODRÍGUEZ V,CARREÑO I,JERMAKOW A M,CARREÑO J,RUIZ-GARCÍA L,THOMAS M R,MARTINEZZAPATER J M. A 48 SNP set for grapevine cultivar identification[J] . BMC Plant Biology,2011,11:153.
[12] WINFIELD M,BURRIDGE A,ORDIDGE M,HARPER H,WILKINSON P,THOROGOOD D,COPAS L,EDWARDS K,BARKER G. Development of a minimal KASP marker panel for distinguishing genotypes in apple collections[J] . PLoS One,2020,15(11):e0242940.
[13] 张小猜,赵政阳,樊红科,党志国,张志敏. 苹果杂种F1代叶片性状分离及早期选择研究[J] . 西北农业学报,2009,18(5):228-231.ZHANG Xiaocai,ZHAO Zhengyang,FAN Hongke,DANG Zhiguo,ZHANG Zhimin. Study on the leaf trait segregation of apple hybrid seedlings and application in pre-selection[J] . Acta Agriculturae Boreali-Occidentalis Sinica,2009,18(5):228-231.
[14] 刘遵春,苗卫东,刘大亮,陈学森. 苹果叶片相关性状的QTL定位及其遗传效应分析[J] . 西北植物学报,2014,34(3):481-487.LIU Zunchun,MIAO Weidong,LIU Daliang,CHEN Xuesen.Identification of quantitative trait loci associated with leaf traits in apple and analysis of their genetic effects[J] . Acta Botanica Boreali-Occidentalia Sinica,2014,34(3):481-487.
[15] TIAN H L,WANG F G,ZHAO J R,YI H M,WANG L,WANG R,YANG Y,SONG W. Development of maizeSNP3072,a highthroughput compatible SNP array,for DNA fingerprinting identification of Chinese maize varieties[J] . Molecular Breeding,2015,35(6):136.
[16] GAO L F,JIA J Z,KONG X Y. A SNP-based molecular barcode for characterization of common wheat[J] . PLoS One,2016,11(3):e0150947.
[17] ZHANG Y C,KUANG M,YANG W H,XU H X,ZHOU D Y,WANG Y Q,FENG X A,SU C,WANG F. Construction of a primary DNA fingerprint database for cotton cultivars[J] . Genetics and Molecular Research,2013,12(2):1897-1906.
[18] 曹建康,姜微波,赵玉梅. 果蔬采后生理生化实验指导[M] . 北京:中国轻工业出版社,2007.CAO Jiankang,JIANG Weibo,ZHAO Yumei. Experimental guidance on postharvest physiology and biochemistry of fruits and vegetables[M] . Beijing:China Light Industry Press,2007.
[19] KOMATSU A,TAKANOKURA Y,MORIGUCHI T,OMURA M,AKIHAMA T. Differential expression of three sucrose-phosphate synthase isoforms during sucrose accumulation in citrus fruits (Citrus unshiu Marc.)[J] . Plant Science,1999,140(2):169-178.
[20] WANG K,LI M Y,HAKONARSON H. ANNOVAR:Functional annotation of genetic variants from high-throughput sequencing data[J] . Nucleic Acids Research,2010,38(16):e164.
[21] XU W J,DUBOS C,LEPINIEC L. Transcriptional control of flavonoid biosynthesis by MYB-bHLH-WDR complexes[J] .Trends in Plant Science,2015,20(3):176-185.
[22] 赖瑞联,吴如健,赖钟雄. 植物类黄酮的分类、药理活性及其生物合成调控研究进展[J] . 东南园艺,2024,12(2):81-99.LAI Ruilian,WU Rujian,LAI Zhongxiong. Research progress on the classification,pharmacological activity,and biosynthesis regulation of plant flavonoid[J] . Southeast Horticulture,2024,12(2):81-99.
[23] 余敏. 猕猴桃花青苷着色[D] . 武汉:中国科学院大学(中国科学院武汉植物园),2020.Yu Min. Coloration of Prunus mume pectinic acid [D] . Wuhan:University of Chinese Academy of Sciences (Wuhan Botanical Garden, Chinese Academy of Sciences),2020.
[24] PAN F G,LIU Y J,LIU J B,WANG E L. Stability of blueberry anthocyanin,anthocyanidin and pyranoanthocyanidin pigments and their inhibitory effects and mechanisms in human cervical cancer HeLa cells[J] . RSC Advances,2019,9(19):10842-10853.
[25] DARYANAVARD H,POSTIGLIONE A E,MÜHLEMANN J K,MUDAY G K. Flavonols modulate plant development,signaling,and stress responses[J] . Current Opinion in Plant Biology,2023,72:102350.
[26] JIANG S H,CHEN M,HE N B,CHEN X L,WANG N,SUN Q G,ZHANG T L,XU H F,FANG H C,WANG Y C,ZHANG Z Y,WU S J,CHEN X S. MdGSTF6,activated by MdMYB1,plays an essential role in anthocyanin accumulation in apple[J] .Horticulture Research,2019,6:40.
[27] 王小红. ‘蜂糖李’果实糖酸组分及其积累规律[D] . 贵阳:贵州大学,2018.WANG Xiaohong. The sugar-acid components of ‘Fengtang plum’ fruit and the regularity of them accumulation[D] . Guiyang:Guizhou University,2018.
[28] 许让伟. 砂梨果实和叶片中糖积累及代谢相关酶活性变化研究[D] . 武汉:华中农业大学,2009.XU Rangwei. Studies on changes of sugar accumulation and related enzymes activities in sand pear fruits and leaves[D] . Wuhan:Huazhong Agricultural University,2009.
[29] BERÜTER J. Carbohydrate metabolism in two apple genotypes that differ in malate accumulation[J] . Journal of Plant Physiology,2004,161(9):1011-1029.
[30] 马钰聪. 花生糖代谢组学分析及子仁可溶性糖快速测定[D] .保定:河北农业大学,2023.MA Yucong. Metabolomic analysis of sugar and rapid determination of kernel soluble sugar in peanut[D] . Baoding:Hebei Agricultural University,2023.
[31] RODGERS F H,GENDRIN M,WYER C A S,CHRISTOPHIDES G K. Microbiota-induced peritrophic matrix regulates midgut homeostasis and prevents systemic infection of malaria vector mosquitoes[J] . PLoS Pathogens,2017,13(5):e1006391.
[32] 张辉红,张崇星. 蚊虫肠道共生菌功能的研究进展[J] . 热带病与寄生虫学,2024,22(1):61-64.ZHANG Huihong,ZHANG Chongxing. Research progress on the function of intestinal commensal bacteria in mosquitoes[J] .Journal of Tropical Diseases and Parasitology,2024,22(1):61-64.
[33] 巩凯玲,陈双慧,纪晓晨,林怡容,张荃. 植物几丁质酶的研究进展[J] . 分子植物育种,2019,17(20):6840-6849.GONG Kailing,CHEN Shuanghui,JI Xiaochen,LIN Yirong,ZHANG Quan. The research progress of plant chitinases[J] . Molecular Plant Breeding,2019,17(20):6840-6849.
[34] MA Z C,SONG T Q,ZHU L,YE W W,WANG Y,SHAO Y Y,DONG S M,ZHANG Z G,DOU D L,ZHENG X B,TYLER B M,WANG Y C. A Phytophthorɑ sojɑe glycoside hydrolase 12 protein is a major virulence factor during soybean infection and is recognized as a PAMP[J] . The Plant Cell,2015,27(7):2057-2072.
[35] 孙媛媛,谢欢,艾星梅,蒙重迪,万敏. 外源生长素调控睡莲叶片生长和延缓衰老的生理效应[J] . 西南林业大学学报(自然科学),2025,45(3):56-64.SUN Yuanyuan,XIE Huan,AI Xingmei,MENG Chongdi,WAN Min. Physiological effects of exogenous auxin on regulating the leaf growth and delaying senescence of water lily[J] .Journal of Southwest Forestry University (Natural Sciences),2025,45(3):56-64.