君迁子(Diospyros lotus L.)属柿科柿属,原产亚洲西部。其根系发达,抗寒力较强,且寿命长久,是中国柿树的主要砧木[1-2]。同时,其基因组相对较小,二倍体中所含等位基因位点相对较少,有利于靶基因敲除,并与栽培柿(D. kaki)有类似的生理代谢途径,可作为柿属植物遗传转化体系建立和功能基因分析的研究材料。日本从20 世纪80 年代开展了柿属植物组织培养研究,之后包括中国在内的许多国家相继对柿组培技术进行探索并取得较大进展[3]。1980 年,Ishida 等[4]获得平核无胚培养试管苗,之后分别以日本甜柿茎尖[5]、平核无休眠芽[6]、次郎叶片[7]为外植体获得组培苗;1993 年,西村早生组培苗生根后移栽大田获得成功[8],这些研究为柿属植物分子育种提供技术支撑。尽管以君迁子为材料进行组培研究已有成功报道[9-16],但仍存在外植体成活率低、组培苗褐化率高、增殖系数较小、生根困难等问题[3],君迁子胚培养体系尚不成熟。而杂交育种作为果树创造新种质的重要手段,其后代常规播种育苗存在种子萌发率低、出苗不整齐、易受病虫害危害及育种周期长等问题,严重阻碍育种工作开展,这更凸显了胚培养在打破种子休眠、克服早期胚败育、加速育种进程等方面的重要价值[17]。鉴于此,选取君迁子作为试验材料,开展胚培养成苗体系的相关研究。设计并实施了多组对比试验,探究了胚发育时期、培养基类型、蔗糖浓度、植物生长调节剂配比、生根条件等因素对君迁子胚培养的影响,构建了稳定高效的胚培养成苗体系,为深入开展君迁子分子生物学研究和杂交育种提供理论和技术支撑。
1 材料和方法
1.1 试验材料
试验材料来自河南科技学院柿属植物种质资源圃。选择生长健壮、花朵数量适中、结实率高、结实稳定的成龄雌株(只开雌花)xx-sc-01 为母本;花量大、花粉萌发率高、与雌株花期相遇的雄株(只开雄花)xy-24 为父本,人工授粉。分别于授粉后45、55、65、75 d采摘果实,带回实验室进行种胚培养。
1.2 试验设计
基本培养基为MS、1/2 MS、(1/2N)MS;蔗糖浓度为30、50、70 g·L-1;IBA浓度为0.04、0.08、0.12 mg·L-1;6-BA 浓度为0.20、0.40、0.60 mg·L-1。培养基pH 值为5.7~5.8,加入聚乙烯吡咯烷酮(PVP)600 mg·L-1防止褐化。高压灭菌锅灭菌20 min。每个处理10瓶,每瓶接种3个幼胚。
胚取样时期:采摘授粉后45、55、65、75 d 的果实,剥取幼胚后分别接种在(1/2N)MS+0.04 mg·L-1 IBA+0.20 mg·L-1 6-BA+50 g·L-1 蔗糖+7 g·L-1 琼脂+600 mg·L-1 PVP 培养基上,每个处理接种30瓶,每瓶接种3个幼胚。
胚培养苗诱导生根:(1)接种后暗处理3 d;(2)培养基添加3 g·L-1活性炭;(3)培养基添加1%墨汁;(4)对照。4种处理均接种在(1/2N)MS+0.08 mg·L-1 IBA+0.20 mg·L-1 6-BA+50 g·L-1蔗糖+7 g·L-1琼脂+600 mg·L-1 PVP 培养基上。在添加活性炭处理时,琼脂浓度调整为9 g·L-1,其他物质比例不变。每个处理接种30 瓶,每瓶接种3 个幼胚。生根后的材料经过断根处理后,接种在(1/2N)MS+0.05 mg·L-1 IBA+0.40 mg·L-1 6-BA+30 g·L-1蔗糖+7 g·L-1琼脂+600 mg·L-1 PVP培养基上。
1.3 试验方法
采摘授粉45、55、65、75 d后的君迁子幼果,先用流水冲洗表面不少于4 h,然后置于烧杯中并在超净工作台上进行消毒。消毒具体步骤如下:用75%乙醇浸洗消毒30 s,在浸泡过程中不断摇晃使果面充分消毒,倒掉废液,用无菌水冲洗3 次;用0.1%升汞(HgCl2)消毒5 min,其间不断摇晃,回收废液,无菌水冲洗3 次。在超净工作台内,将消毒后的幼果剥取幼胚后接种于不同处理培养基上。
培养环境:温度25 ℃,光照时间16 h/d,光照度2000 lx。
接种5 周后统计君迁子胚培养苗的苗高、苗质量、主根长、侧根数、侧根长。炼苗移栽1 周后,统计移栽成活率。
移栽成活率/%=移栽成活苗数/移栽总苗数×100;
无侧根苗率/%=无侧根苗数/接种幼胚总数×100。
1.4 数据处理与分析
使用Excel 2010进行数据统计,利用SPSS 23软件进行数据分析,采用Duncan’s 新复极差法进行差异显著性分析(P<0.05)。每个处理均设置3 次重复。
2 结果与分析
2.1 不同取样时期对胚培养苗生长势的影响
由表1 可知,在君迁子胚的发育进程中,胚成苗率与胚的成熟程度之间存在着紧密关系。随着胚逐渐发育成熟,胚成苗率呈现出稳步上升的态势,并且由此培育出的幼苗在生长发育方面展现出良好状态。这些幼苗的叶片颜色浓郁翠绿,植株生长态势强健,展现出旺盛的生命力。接种授粉后45 d 的幼胚,移栽成活率为62.00%;接种授粉后55 d 的幼胚,移栽成活率提升至74.20%;而接种授粉后65 d 的幼胚表现最为突出,移栽成活率高达90.6%。表明胚发育成熟度对移栽成活率以及幼苗整体生长质量具有显著影响。
表1 不同取样时期对胚培养苗生长势的影响
Table 1 Effect of different sampling periods on growth of embryo cultured seedlings
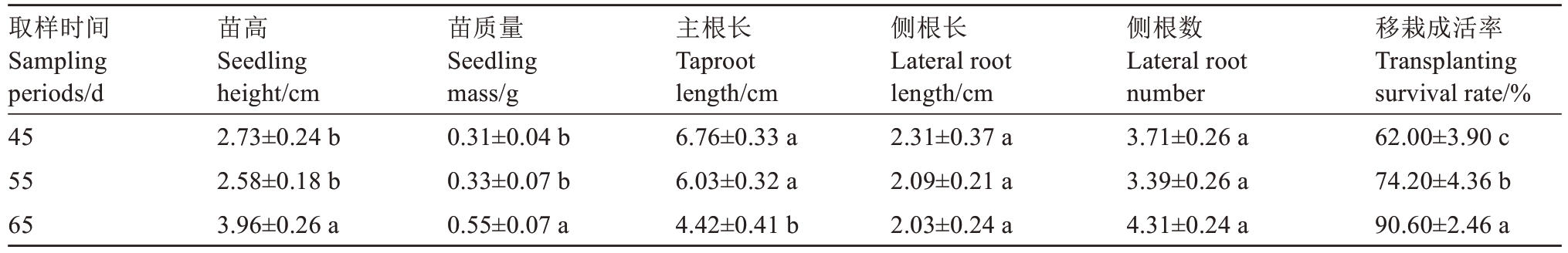
注:同列不同小写字母代表差异显著(P<0.05)。下同。
Note:Different small letters in the same column represent significant differences (P<0.05). The same below.
取样时间Sampling periods/d 45 55 65移栽成活率Transplanting survival rate/%62.00±3.90 c 74.20±4.36 b 90.60±2.46 a苗高Seedling height/cm 2.73±0.24 b 2.58±0.18 b 3.96±0.26 a苗质量Seedling mass/g 0.31±0.04 b 0.33±0.07 b 0.55±0.07 a主根长Taproot length/cm 6.76±0.33 a 6.03±0.32 a 4.42±0.41 b侧根长Lateral root length/cm 2.31±0.37 a 2.09±0.21 a 2.03±0.24 a侧根数Lateral root number 3.71±0.26 a 3.39±0.26 a 4.31±0.24 a
2.2 不同基本培养基类型对胚培养苗生长势及移栽成活率的影响
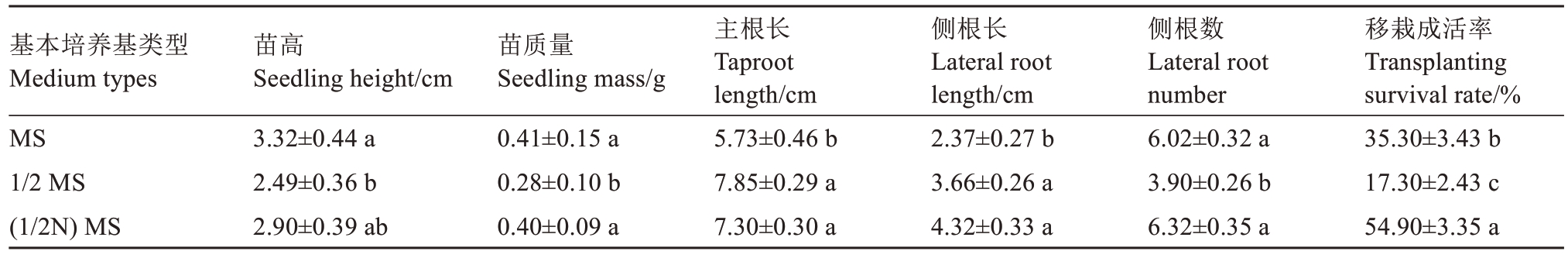
由表2可知,将君迁子幼胚接种于(1/2N)MS培养基,各项生长指标表现较为优异。其中,幼苗高度均值可达2.90 cm,苗质量均值为0.40 g,侧根平均长度为4.32 cm,侧根平均数量为6.32 条,且移栽成活率在3种基本培养基处理中最高,达到了54.90%。
表2 不同基本培养基类型对胚培养苗生长势及移栽成活率的影响
Table 2 Effect of different minimal medium types on growth and transplanting survival rate of embryo cultured seedlings
基本培养基类型Medium types MS 1/2 MS(1/2N) MS苗高Seedling height/cm 3.32±0.44 a 2.49±0.36 b 2.90±0.39 ab苗质量Seedling mass/g 0.41±0.15 a 0.28±0.10 b 0.40±0.09 a主根长Taproot length/cm 5.73±0.46 b 7.85±0.29 a 7.30±0.30 a侧根长Lateral root length/cm 2.37±0.27 b 3.66±0.26 a 4.32±0.33 a侧根数Lateral root number 6.02±0.32 a 3.90±0.26 b 6.32±0.35 a移栽成活率Transplanting survival rate/%35.30±3.43 b 17.30±2.43 c 54.90±3.35 a
当幼胚接种于1/2 MS 培养基时,胚培养苗质量仅为0.28 g,侧根平均数量仅为3.90 条,移栽成活率也仅为17.30%,与(1/2N)MS 培养基培养的胚培养苗差异显著。
当幼胚接种于MS培养基时,胚培养苗主根平均长度仅为5.73 cm,侧根平均长度仅为2.37 cm,移栽成活率为35.30%,这与(1/2N)MS 培养基培养的胚培养苗差异显著。以上结果表明,不同的培养基类型对君迁子胚培养苗的生长态势具有影响,(1/2N)MS 培养基在促进君迁子胚培养苗的生长及提高移栽成活率方面表现更为突出,适宜作为君迁子胚培养的基本培养基。
2.3 不同蔗糖浓度对胚培养苗生长势及移栽成活率的影响
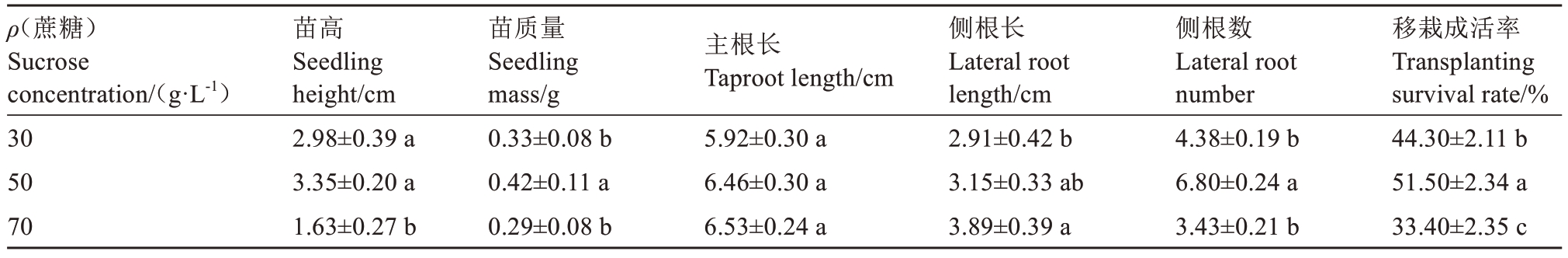
由表3 可知,蔗糖浓度对君迁子胚培养苗的生长发育影响显著。当培养基中蔗糖浓度为50 g·L-1时,君迁子胚培养苗呈现出良好的生长态势,苗高达到3.35 cm,苗质量为0.42 g,侧根数量为6.80 条,移栽成活率为51.50%。
表3 不同蔗糖浓度对胚培养苗生长势及移栽成活率的影响
Table 3 Effect of different sucrose concentration on growth and transplanting survival rate of embryo cultured seedlings
ρ(蔗糖)Sucrose concentration/(g·L-1)30 50 70苗高Seedling height/cm 2.98±0.39 a 3.35±0.20 a 1.63±0.27 b苗质量Seedling mass/g 0.33±0.08 b 0.42±0.11 a 0.29±0.08 b主根长Taproot length/cm 5.92±0.30 a 6.46±0.30 a 6.53±0.24 a侧根长Lateral root length/cm 2.91±0.42 b 3.15±0.33 ab 3.89±0.39 a侧根数Lateral root number 4.38±0.19 b 6.80±0.24 a 3.43±0.21 b移栽成活率Transplanting survival rate/%44.30±2.11 b 51.50±2.34 a 33.40±2.35 c
当蔗糖浓度提升至70 g·L-1时,组培苗的生长受到明显抑制,苗高仅为1.63 cm,苗质量仅为0.29 g,侧根数量仅为3.43 条,移栽成活率也降至33.40%。该浓度下的胚培养苗在各项生长指标上,与蔗糖浓度为50 g·L-1的胚培养苗存在显著差异。而当蔗糖浓度降低至30 g·L-1时,胚培养苗的生长同样受到影响。苗质量为0.33 g,主根长为5.92 cm,侧根长为2.91 cm,侧根数量为4.38条,移栽成活率为44.30%。此浓度下的胚培养苗与蔗糖浓度为50 g·L-1的胚培养苗相比,各项生长指标差异显著。
综合结果表明,50 g·L-1的蔗糖浓度最有利于君迁子幼胚的生长发育,是君迁子胚培养过程中适宜的蔗糖浓度。
2.4 不同植物生长调节剂配比对胚培养苗生长势的影响
植物生长调节剂的不同组合,在君迁子幼胚的生长发育过程中起着重要的作用。由表4 可知,当幼胚接种于T3组合培养基时,呈现出良好的生长表现。君迁子幼胚成苗后的生长势良好,平均苗质量达到0.42 g,主根长为8.81 cm,侧根长为6.45 cm,且接种后的所有幼胚均能顺利产生侧根,移栽成活率最高,达到62.70%,显著优于其他处理组培养基。
表4 不同植物生长调节剂配比对君迁子胚培养苗生长势及移栽成活率的影响
Table 4 Effects of different plant growth regulators ratio on growth and transplanting survival rate of embryo cultured seedlings
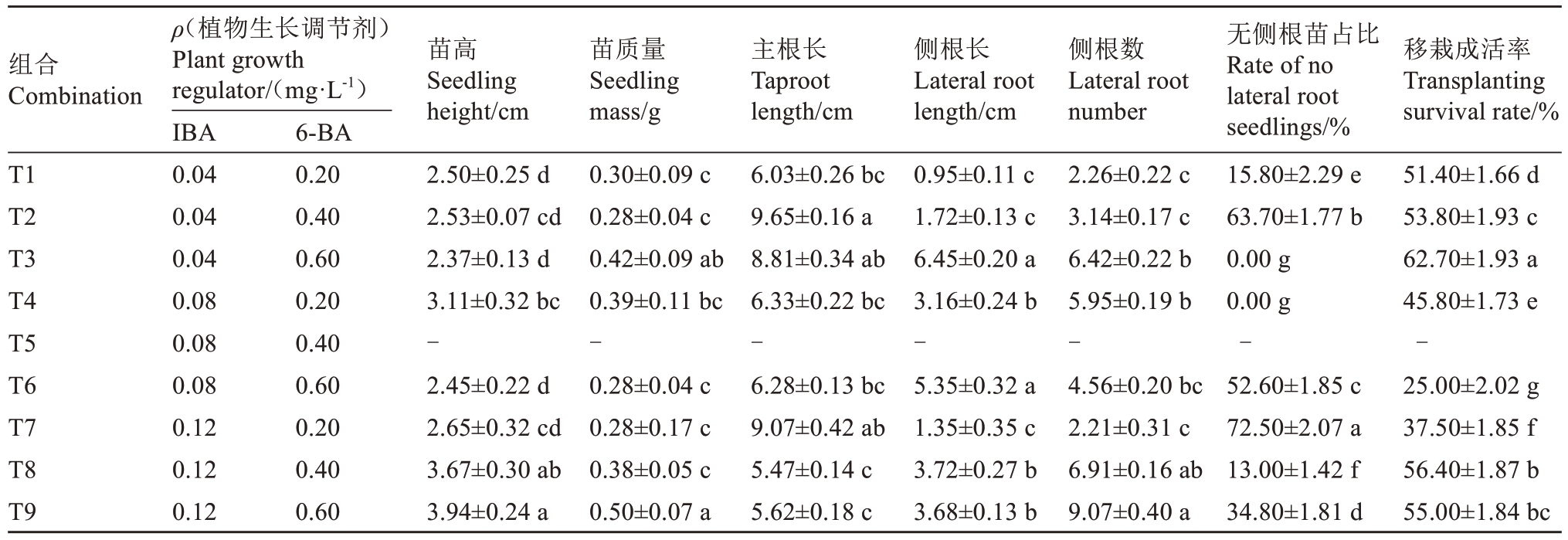
注:“-”表示该组试验材料污染死亡,未获得有效数据。
Note:“-” Indicates that the experimental materials of this group were contaminated or died, so no valid data was obtained.
组合Combination苗高Seedling height/cm苗质量Seedling mass/g主根长Taproot length/cm侧根长Lateral root length/cm侧根数Lateral root number移栽成活率Transplanting survival rate/%T1 T2 T3 T4 T5 T6 T7 T8 T9 ρ(植物生长调节剂)Plant growth regulator/(mg·L-1)IBA 0.04 0.04 0.04 0.08 0.08 0.08 0.12 0.12 0.12 6-BA 0.20 0.40 0.60 0.20 0.40 0.60 0.20 0.40 0.60 51.40±1.66 d 53.80±1.93 c 62.70±1.93 a 45.80±1.73 e-25.00±2.02 g 37.50±1.85 f 56.40±1.87 b 55.00±1.84 bc 2.50±0.25 d 2.53±0.07 cd 2.37±0.13 d 3.11±0.32 bc-2.45±0.22 d 2.65±0.32 cd 3.67±0.30 ab 3.94±0.24 a 0.30±0.09 c 0.28±0.04 c 0.42±0.09 ab 0.39±0.11 bc-0.28±0.04 c 0.28±0.17 c 0.38±0.05 c 0.50±0.07 a 6.03±0.26 bc 9.65±0.16 a 8.81±0.34 ab 6.33±0.22 bc-6.28±0.13 bc 9.07±0.42 ab 5.47±0.14 c 5.62±0.18 c 0.95±0.11 c 1.72±0.13 c 6.45±0.20 a 3.16±0.24 b-5.35±0.32 a 1.35±0.35 c 3.72±0.27 b 3.68±0.13 b 2.26±0.22 c 3.14±0.17 c 6.42±0.22 b 5.95±0.19 b-4.56±0.20 bc 2.21±0.31 c 6.91±0.16 ab 9.07±0.40 a无侧根苗占比Rate of no lateral root seedlings/%15.80±2.29 e 63.70±1.77 b 0.00 g 0.00 g-52.60±1.85 c 72.50±2.07 a 13.00±1.42 f 34.80±1.81 d
接种于T9 组合培养基的幼胚,苗质量(0.50 g)与T3组合培养基相比差异并不显著。然而,在苗高(3.94 cm)、主根长度(5.62 cm)、侧根长度(3.68 cm)、侧根数量(9.07 条)、接种后无侧根苗的比例(34.80%)以及移栽成活率(55.00%)等指标上,T9组合培养基与T3组合培养基存在显著差异。
接种于T8 组合培养基的幼胚,侧根数量(6.91条)与T3 组合培养基相比差异不显著。在苗高(3.67 cm)、主根长(5.47 cm)、侧根长(3.72 cm)、侧根数量(6.91 条)、移栽成活率(56.40%)以及接种后无侧根苗比例(13.00%)等指标上,与T3组合培养基存在显著差异。
接种于T4 组合培养基的幼胚,移栽成活率较低,仅为45.80%。接种于T5 组合培养基上的幼胚,未出现萌发迹象;接种于T7 组合培养基的幼胚,虽能萌发,但产生的无侧根苗比例极高,达到72.50%。综合分析表明,不同植物生长调节剂的配比,对君迁子胚培养苗的生长势如苗高、苗质量、根的生长发育以及移栽成活率等具有重要的影响,筛选适宜的植物生长调节剂组合,对君迁子胚培养技术体系的优化很重要。
2.5 断根对君迁子胚培养苗生长势的影响
在君迁子幼胚的生长发育进程中,部分组培苗出现了特殊现象,即仅生成一条主根,却未产生侧根,这类组培苗被定义为无侧根苗(图1-A~B)。为研究断根处理对君迁子组培苗根系生长的影响,将试验过程中出现的无侧根苗挑选出来,对其实施断根处理,随后接种至生根培养基中进行培养观察。断根处理对无侧根苗的根系发育起到了显著的促进作用(图1-C~D)。说明断根处理能够打破无侧根苗的生长局限,促进侧根的生长发育,为君迁子组培苗根系的优化提供了可行的技术手段,在君迁子胚培养成苗体系中具有重要的作用。

图1 断根对君迁子胚培养中出现的无侧根苗的影响
Fig. 1 Effects of root cutting on lateral root seedlings in embryo culture
2.6 不同诱导生根处理对君迁子胚培养苗生长势的影响
不同诱导生根方式对君迁子胚培养苗的生长发育具有不同影响(图2)。由表5 可知,在培养基中添加活性炭,不仅无法促进君迁子组培苗侧根的产生,还会导致植株生长迟缓,所培育的组培苗均未长出侧根。
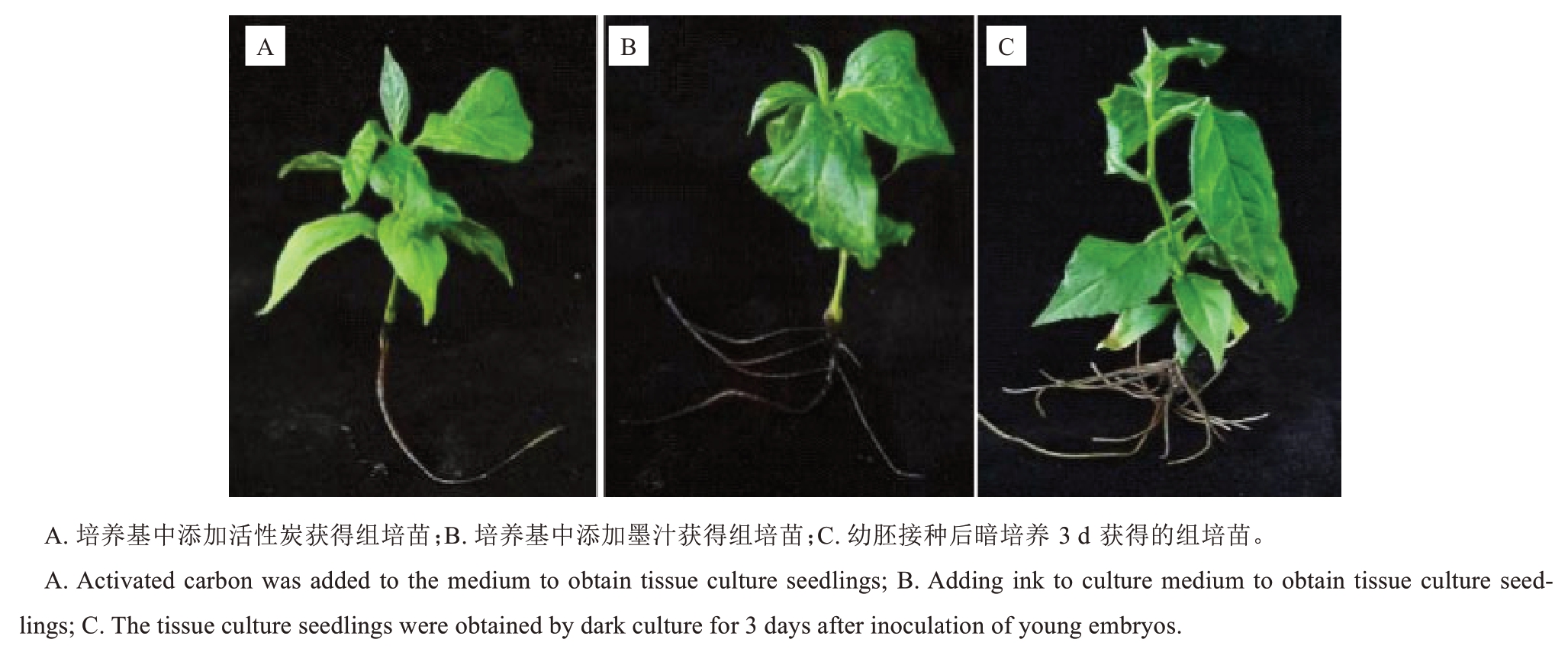
图2 不同诱导生根处理对君迁子胚培养苗生长势的影响
Fig. 2 Effects of different induced rooting treatments on the growth of seedlings cultured from date plum embryos
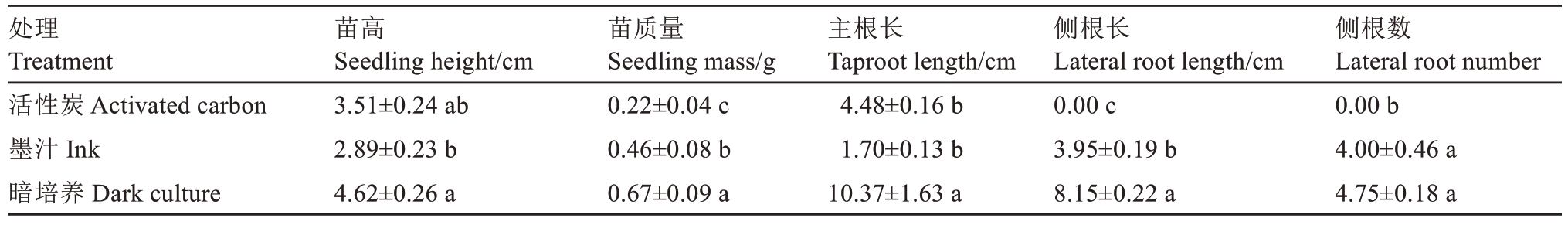
表5 不同诱导生根方式对君迁子胚培养苗生长势的影响
Table 5 Effects of different rooting induction methods on growth of embryo culture seedlings
处理Treatment活性炭 Activated carbon墨汁 Ink暗培养 Dark culture苗高Seedling height/cm 3.51±0.24 ab 2.89±0.23 b 4.62±0.26 a苗质量Seedling mass/g 0.22±0.04 c 0.46±0.08 b 0.67±0.09 a主根长Taproot length/cm 4.48±0.16 b 1.70±0.13 b 10.37±1.63 a侧根长Lateral root length/cm 0.00 c 3.95±0.19 b 8.15±0.22 a侧根数Lateral root number 0.00 b 4.00±0.46 a 4.75±0.18 a
在培养基中添加墨汁以及接种后进行3 d 暗培养,这两种处理方式均能对君迁子幼胚的生根起到促进作用。其中,添加墨汁处理的组培苗,侧根平均数量为4.00 条;而接种后暗培养3 d 处理的组培苗,侧根平均数量达到4.75条。添加墨汁处理虽能促进生根,但此处理的幼胚成苗的叶片出现卷曲现象,苗高仅为2.89 cm,苗质量为0.46 g,植株较为矮小,生长发育速度缓慢。综合结果表明,君迁子幼胚接种后暗培养3 d 的处理方式,在促进生根方面效果最佳,能够使胚培养苗获得更为良好的生长发育状态。
2.7 驯化移栽
在植物组织培养过程中,驯化移栽是实现组培苗从实验室环境向自然环境过渡的关键环节,对提高组培苗的成活率和后续生长发育质量至关重要。笔者总结了君迁子组培苗的驯化移栽操作流程(图3),具有可操作性和实用性,具体步骤如下:

图3 君迁子组培苗的炼苗移栽
Fig. 3 Refinement and transplanting of tissue cultured seedlings of date plum
(1)驯化初期,在第1 天小心解开封口绳,以轻柔的动作揭开部分封口膜,使组培苗逐渐适应外界环境的气体交换,这一过程有助于避免环境变化过于剧烈对组培苗造成冲击。随后,在接下来的3~4 d内,逐步扩大封口膜的揭开面积,直至第4、第5天完全揭开封口膜,让组培苗在组培室内经历4~5 d 的炼苗过程。
(2)完成组培室内炼苗后,将组培瓶移至室外阴凉处,继续炼苗1~2 d。
(3)移栽时,使用经过消毒处理的镊子,小心地将组培苗从培养瓶中拔出,尽量避免损伤根系。移栽基质选用泥炭土、蛭石和珍珠岩,按体积比3∶1∶1混合配制而成。该基质具有良好的透气性和保水性。基质的湿度以手握成团、落地散开为宜。这种湿度条件既有利于保持根系的水分,又能确保根系获得充足的氧气,为组培苗的生长提供适宜环境。
(4)移栽完成后,立即浇一次透水,使基质与组培苗根系充分接触,为根系提供水分和养分。在后续的养护过程中,每隔1~2 d 浇一次水,保持基质湿润,但需注意避免积水,以防止根系腐烂。通过这样的驯化移栽操作,能够有效提高君迁子组培苗的移栽成活率,促进其健康生长,为苗木的规模化培育奠定坚实基础。
3 讨 论
胚龄是影响君迁子胚培养成功的核心因素,其与胚成苗率及幼苗生长质量呈显著正相关[18]。朱际君等[19]研究发现胚龄越小越难培养成功;Chaparro等[20]在蜜桃的胚培养研究中发现,花后68 d接种时,幼胚萌发率达70%,而在花后30~53 d接种萌发率为2%~3%;扈惠灵等[21]揭示了磨盘柿杂种败育的细胞学机制,认为可以利用胚挽救的技术手段,分别在授粉后30~40 d 及60~70 d 进行胚离体培养以获得F1代杂种;徐莉清等[22]研究结果表明,完全甜柿次郎幼胚的最佳培养时期是授粉后50~60 d。本研究结果表明,授粉后65 d 的幼胚移栽成活率高达90.60%,显著优于45 d(62.00%)和55 d(74.20%)的处理(P<0.05)。这与朱际君等[19]的结论一致,也与Chaparro等[20]在蜜桃、徐莉清等[22]在次郎柿中的研究结果吻合。需特别注意的是,过早取胚(如45 d)会因胚未成熟而导致成苗率低,过晚取胚(如75 d)则因胚乳硬化增加操作难度并损伤幼胚。综合效率与成活率,确定授粉后50~60 d 为最佳取胚期,此时胚乳未硬化,既保证操作便捷性,又能获得较高成苗率。
目前,在所有木本植物的组织培养中,最常用的培养基类型为MS 培养基。但在多数柿属植物组织培养的研究中表明,氮素浓度过高不利于芽的启动与增殖培养,在组培中使用最多的是1/2 MS 培养基和(1/2N)MS 培养基[17]。谷晓峰等[23]研究表明,罗田甜柿胚培养时的最适培养基为(1/2N)MS培养基,而扈惠灵等[24]认为,适当提高MS培养基中N的浓度可促进磨盘柿胚挽救苗的茁壮生长。笔者发现(1/2N)MS 培养基表现显著优于MS 和1/2MS。其幼苗移栽成活率达54.90%,侧根数量达6.32 条,均显著高于MS(35.30%,6.02 条)和1/2MS(17.30%,3.90 条)(P<0.05)。这一结果与谷晓峰等[23]在罗田甜柿中的研究一致,印证了降低氮素浓度对柿属植物胚培养具有促进作用。高氮浓度可能抑制芽的启动与增殖,而(1/2N)MS 通过优化氮素水平,为胚萌发和幼苗生长提供了更适宜的矿质环境,对木本植物尤其是柿属的组培具有重要的参考价值。
植物生长调节剂配比是影响根系发育的关键变量[25]。本研究结果表明,(1/2N)MS+0.04 mg·L-1 IBA+0.60 mg·L-1 6-BA 组合表现最优,移栽成活率达62.70%。与之对比,T9 组合(0.12 mg·L-1 IBA+0.60 mg·L-1 6-BA)虽侧根数量达9.07 条,但主根短(5.62 cm)、无侧根苗率高(34.80%),表明高浓度IBA 可能导致根系畸形;T7 组合(0.12 mg·L-1 IBA+0.20 mg·L-1 6-BA)无侧根苗率高达72.50%,进一步表明IBA 浓度过高会严重抑制侧根形成。由此可见,低浓度IBA(0.04 mg·L-1)与较高浓度6-BA(0.60 mg·L-1)的协同作用,是促进根系均衡发育的关键。
断根处理有效促进了侧根的发育,这一现象符合植物创伤修复理论,即切断主根顶端优势后,刺激了侧根原基的激活与生长。该技术不仅解决了组培苗根系畸形问题,还通过增加根系吸收面积,提升了幼苗对水分和养分的吸收能力,为后续移栽成活奠定了坚实基础,是优化根系结构的关键技术环节。
生根困难是制约柿属植物组培发展的关键因素,受品种、培养条件以及继代次数的影响[26]。蒋振莹[27]研究发现在(1/2N)MS+1.0 mg·L-1 IBA 培养基中添加0.5 mg·L-1 6-BA,暗培养3 d,君迁子组培苗生根率达到93.51%,平均根数达到5.06 条;扈惠灵等[28]研究表明培养基中添加墨汁和活性炭能促进柿组培苗生根,且通过断根处理能将磨盘柿组培苗中的畸形苗转变成正常的组培苗。本试验结果表明,暗培养3 d 表现出显著优势,侧根数量达4.75 条,显著高于墨汁处理(4.00 条)和活性炭处理(0 条)(P<0.05)。活性炭处理不仅未能促进生根,还导致植株矮小(苗高3.51 cm)、无侧根,可能与其吸附生长物质有关;墨汁处理虽能生根,但叶片卷曲(苗高2.89 cm),推测与墨汁中不明成分的毒性相关。暗培养通过模拟自然萌发初期的遮光环境,可能激活了根系发育相关基因的表达,从而促进侧根原基的形成,为柿属植物组培中难以生根的问题提供了有效解决方案。
驯化移栽流程的优化是组培苗商业化应用的关键。笔者采用“逐步透气-室外炼苗-基质优化”的三步法:组培室内4~5 d 逐步揭膜炼苗,使幼苗适应湿度梯度变化;室外阴凉处1~2 d炼苗,增强抗逆性;移栽基质采用泥炭土、蛭石、珍珠岩体积比3∶1∶1,其持水孔隙与通气孔隙比例协调,既避免积水烂根,又保证氧气供应。该流程显著提升了移栽成活率,结合断根处理和暗培养技术,形成了从离体培养到田间定植的完整技术链,为君迁子的规模化育苗提供了可复制的操作范式。
尽管建立了稳定的胚培养体系,但仍存在优化空间:以(1/2N)MS+0.04 mg·L-1 IBA+0.60 mg·L-1 6-BA 为基础,(1/2N)MS 培养基的矿质元素配比可进一步微调,如探索钙、镁离子浓度对根系木质化的影响;探索植物生长调节剂组合更优配比;断根处理的最佳时机(如主根长度阈值)和再生机制的深入研究;驯化移栽中光照度、湿度等环境因子的精准调控模型的构建。未来研究可围绕上述方向展开,进一步提升体系的稳定性与效率,推动君迁子在分子育种和砧木改良中的广泛应用。
4 结 论
笔者确立了君迁子胚培养成苗的核心技术体系:取胚最佳时期为授粉后55~65 d,此阶段胚乳未硬化,可保障成苗质量与操作效率。优选(1/2N)MS培养基,添加0.04 mg·L-1 IBA、0.60 mg·L-1 6-BA 及50 g·L-1蔗糖,显著提升胚萌发率,促进幼苗健壮生长与主侧根均衡发育。幼胚接种后暗培养3 d,结合断根处理,可高效诱导侧根形成,根系质量显著优化。移栽环节采用泥炭土、蛭石、珍珠岩体积比3∶1∶1 的基质,通过渐进式的炼苗流程,大幅提高移栽成活率。该体系解决了君迁子胚培养中外植体成活率低、生根困难等问题,为君迁子杂交胚挽救及规模化育苗提供了技术方案,对柿属植物遗传改良具有重要应用价值。
[1] 杨婷婷,于泽群,夏乐晗,杨勇,王仁梓. 君迁子(Diospyros lotus)种质资源形态学性状的聚类分析[J]. 果树学报,2014,31(4):566-573.YANG Tingting,YU Zequn,XIA Lehan,YANG Yong,WANG Renzi. Cluster analysis based on morphological traits of date plum (Diospyros lotus) germplasm resources[J]. Journal of Fruit Science,2014,31(4):566-573.
[2] 张晓娜,周瑞金,毛树林,张传来,扈惠灵. 三种花色君迁子的花粉粒形态及花粉生活力鉴定[J]. 河南科技学院学报(自然科学版),2021,49(2):1-5.ZHANG Xiaona,ZHOU Ruijin,MAO Shulin,ZHANG Chuanlai,HU Huiling. Identification of pollen morphology and viability of three staminate flower colors in Diospyros lotus L.[J]. Journal of Henan Institute of Science and Technology (Natural Science Edition),2021,49(2):1-5.
[3] 罗正荣,张青林,徐莉清,郭大勇. 柿的遗传多样性及育种研究进展[J]. 落叶果树,2021,53(3):1-5.LUO Zhengrong,ZHANG Qinglin,XU Liqing,GUO Dayong.Advances in genetic diversity and breeding of persimmon[J].Deciduous Fruits,2021,53(3):1-5.
[4] ISHIDA M,INAB A,SOBAJIMA Y. In vitro culture of young embryos of Hiratanenashi persimmon[J]. Scientific Reports of the Kyoto Prefectural University, Agriculture,1980,32:20-24.
[5] TAO R,SUGIURA A. Micropropagation of Japanese persimmon (Diospyros kaki L.)[M]//BAJAJ Y P S. Biotechnology in Agriculture and Forestry,High-Tech and Micropropagation II.Berlin,Heidelberg:Springer,1992:424-440.
[6] SUGIURA A,TAO R,MURAYAMA H,TOMANA T. In vitro propagation of Japanese persimmon[J]. HortScience,1986,21(5):1205-1207.
[7] TAO R,SUGIURA A. Adventitious bud formation from callus cultures of Japanese persimmon[J]. HortScience,1992,27(3):259-261.
[8] TETSUMURA T,YUKINAGA H,TAO R. Early field performance of micropropagated Japanese persimmon trees[J]. Hort-Science,1998,33(4):751-753.
[9] 艾鹏飞,罗正荣. 柿和君迁子试管苗茎尖玻璃化法超低温保存及再生植株遗传稳定性研究[J]. 中国农业科学,2004,37(12):2023-2027.AI Pengfei,LUO Zhengrong. Cryopreservation of in vitro shoottips of persimmon and date plum by vitrification and genetic stability of regenerated plantlets[J]. Scientia Agricultura Sinica,2004,37(12):2023-2027.
[10] 谢启鑫,黄美连,吴晓萍,庄东红. 君迁子叶片培养再生植株的研究[J]. 中国农业科学,2008,41(2):607-612.XIE Qixin,HUANG Meilian,WU Xiaoping,ZHUANG Donghong. Plant regeneration from leaves of date plum (Diospyros lotus L.)[J]. Scientia Agricultura Sinica,2008,41(2):607-612.
[11] 李晶,罗玉洁,张青林,罗正荣,刘继红. 君迁子休眠芽及叶片离体培养体系优化及植株再生[J]. 华中农业大学学报,2016,35(4):14-19.LI Jing,LUO Yujie,ZHANG Qinglin,LUO Zhengrong,LIU Jihong. In vitro culture system optimization and regeneration of date plum (Diospyros lotus Linn.) dormant buds and leaves[J].Journal of Huazhong Agricultural University,2016,35(4):14-19.
[12] 周瑞金,张晓娜,扈惠灵,李桂荣,宋如慧. 无核君迁子离体叶片的植株再生[J]. 北方园艺,2016(22):104-106.ZHOU Ruijin,ZHANG Xiaona,HU Huiling,LI Guirong,SONG Ruhui. Plant regeneration from leaves of seedless date plum (Diospyros lotus L.)[J]. Northern Horticulture,2016(22):104-106.
[13] LI X H,JIANG Z Y,SHEN Y Y,LI F H,YU X Y,QU S C. In vitro regeneration and Agrobacterium tumefaciens-mediated genetic transformation of Diospyros lotus L.[J]. Scientia Horticulturae,2018,236:229-237.
[14] 魏文豪,杨雅婷,白亚娟,魏一杰,杨文龙,周瑞金. 君迁子茎段启动培养研究[J]. 现代园艺,2020(23):27-28.WEI Wenhao,YANG Yating,BAI Yajuan,WEI Yijie,YANG Wenlong,ZHOU Ruijin. Research on the start culture of Diospyros lotus stem segment[J]. Xiandai Horticulture,2020(23):27-28.
[15] 吕中一,刘庆华,范芝蕊,申小霞,关长飞,杨勇. 君迁子组培苗生根移栽体系优化[J]. 北方园艺,2024(3):33-40.LÜ Zhongyi,LIU Qinghua,FAN Zhirui,SHEN Xiaoxia,GUAN Changfei,YANG Yong. Optimization of rooting and transplanting system of Diospyros lotus L. tissue cultured seedlings[J].Northern Horticulture,2024(3):33-40.
[16] 吕中一,闻家乐,刘泽远,张馨予,胡碧春,范芝蕊,关长飞,杨勇. 君迁子组培体系的建立及优化[J]. 西北农林科技大学学报(自然科学版),2024,52(5):102-109.LÜ Zhongyi,WEN Jiale,LIU Zeyuan,ZHANG Xinyu,HU Bichun,FAN Zhirui,GUAN Changfei,YANG Yong. Establishment and optimization of a tissue culture and rapid propagation system of Diospyros lotus L.[J]. Journal of Northwest A & F University (Natural Science Edition),2024,52(5):102-109.
[17] 王永清,杜奎,杨志武,陶炼,杨芩,范建新,邓仁菊. 果树远缘杂交育种研究进展[J]. 果树学报,2012,29(3):440-446.WANG Yongqing,DU Kui,YANG Zhiwu,TAO Lian,YANG Qin,FAN Jianxin,DENG Renju. Advances in the studies of distant hybridization in fruit crops[J]. Journal of Fruit Science,2012,29(3):440-446.
[18] 刘用生,胡霓云,路广明. 早熟桃胚珠离体培养研究[J]. 西北农业大学学报,1991,19(3):37-43.LIU Yongsheng,HU Niyun,LU Guangming. Research on ovule culture in vitro of early-maturing peach[J]. Journal of Northwest Agricultural University,1991,19(3):37-43.
[19] 朱际君,吴鹤鸣,汪祖华. 桃早熟品种种胚培养技术研究[J].江苏农业科学,1983,11(9):33-35.ZHU Jijun,WU Heming,WANG Zuhua. Study on embryo culture technology of early-maturing peach varieties[J]. Jiangsu Agricultural Sciences,1983,11(9):33-35.
[20] CHAPARRO J X,SHERMAN W B. Culture date and germination procedure affects success of nectarine ovule and embryo culture[J]. Fruit Varieties Journal,1994,48(3):173-175.
[21] 扈惠灵,李壮,曹永庆,冷平. 磨盘柿败育杂种胚胎发育的细胞学特征[J]. 果树学报,2007,24(5):630-633.HU Huiling,LI Zhuang,CAO Yongqing,LENG Ping. Cytological research on abnormal hybrid seeds in parthenocarpic Mopanshi persimmon cultivar[J]. Journal of Fruit Science,2007,24(5):630-633.
[22] 徐莉清,张青林,罗正荣. 幼胚发育阶段对次郎柿胚抢救效果的影响[J]. 果树学报,2008,25(1):45-48.XU Liqing,ZHANG Qinglin,LUO Zhengrong. Effect of embryo development stage on embryo rescue for Jirou persimmon culitivar[J]. Journal of Fruit Science,2008,25(1):45-48.
[23] 谷晓峰,唐仙英,罗正荣. 罗田甜柿幼胚培养条件的研究[J].果树学报,2001,18(2):80-83.GU Xiaofeng,TANG Xianying,LUO Zhengrong. A study on culture conditions of immature embryo in Luotiantianshi persimmon variety[J]. Journal of Fruit Science,2001,18(2):80-83.
[24] 扈惠灵,张慧,李宝,冷平. 磨盘柿的合子胚挽救培养[J]. 园艺学报,2005,32(6):1077-1079.HU Huiling,ZHANG Hui,LI Bao,LENG Ping. In vitro rescue culture of zygotic embryo of ‘Mopanshi’ persimmon[J]. Acta Horticulturae Sinica,2005,32(6):1077-1079.
[25] 吕中一,关长飞,李家艳,丁瑜,范芝蕊,杨勇. 柿属植物组织培养技术研究进展[J]. 北方园艺,2023(12):129-137.LÜ Zhongyi,GUAN Changfei,LI Jiayan,DING Yu,FAN Zhirui,YANG Yong. Research progress on tissue culture of Diospyros[J]. Northern Horticulture,2023(12):129-137.
[26] 檀苏红,邓少宁,程梦叶,刘博威,张驰,李双,朱陈宇,耿晶晶,王文江. 柿砧木优系L938 离体快繁技术建立[J]. 果树学报,2024,41(9):1875-1884.TAN Suhong,DENG Shaoning,CHENG Mengye,LIU Bowei,ZHANG Chi,LI Shuang,ZHU Chenyu,GENG Jingjing,WANG Wenjiang. Establishment of in vitro rapid propagation technology for an elite persimmon rootstock line,L938[J]. Journal of Fruit Science,2024,41(9):1875-1884.
[27] 蒋振莹. 君迁子组培快繁及叶片再生体系研究[D]. 南京:南京农业大学,2015.JIANG Zhenying. Study on tissue culture and plant regeneration of persimmon (Diospyros lotus L.)[D]. Nanjing:Nanjing Agricultural University,2015.
[28] 扈惠灵,曹永庆,卫永乐,任杰,冷平. 磨盘柿杂种胚挽救中的生根壮苗培养[J]. 华北农学报,2007,22(5):117-119.HU Huiling,CAO Yongqing,WEI Yongle,REN Jie,LENG Ping. Rooting and hardening-off culture of Mopanshi persimmon hybrid zygotic embryo[J]. Acta Agriculturae Boreali-Sinica,2007,22(5):117-119.