果实的成熟调控是园艺植物研究的核心课题。果实成熟涉及复杂的生理、生化和结构转变,如色泽、质地、风味、香气和营养成分的变化,这一过程受多种因素的共同调控,包括植物激素、环境条件(如温度和光照)以及遗传背景[1]。对于跃变型果实,乙烯通常被视为关键的成熟激素,而在非跃变型果实的成熟中,ABA 则展现出更为关键的调控作用[2]。果实大小是果实品质的重要指标之一,与多种因素有关,主要由细胞分裂和细胞膨大决定,也与植物自身的碳水化合物含量、内源激素含量、光照、水分和温度等外界环境条件有关[3]。
荔枝(Litchi chinensis Sonn.)原产于中国云南[4],全国荔枝种植面积为52.7 万hm2,2023 年产量达到329 万t[5],作为热带和亚热带地区的重要经济果树,对当地农民增收和乡村振兴具有显著贡献。果实大小是决定荔枝鲜果销售价格的关键因素,但在栽培过程中,优质品种的果实大小往往参差不齐。在采收时,果农对荔枝果实进行分级包装,果个大者价格优势明显。以仙进奉为例,果实大于28 g 可以按粒果进行包装销售,价格是普通大小果(<23 g)的3倍以上。关于如何提高荔枝优质果比例的研究报道较少。疏果虽能提高果实大小,但会降低产量[6]。人工疏果劳动成本高,效率低[7]。化学疏果虽然效率高,但存在安全隐患和不稳定性[8]。优化栽培措施如施肥、灌溉和修剪技术虽能增加果实大小,但效果有限[9]。此外,市场上优质品种多为晚熟品种,集中上市加大了市场供给压力[10]。若能实现早熟,提早上市,既能显著提升荔枝的经济价值,又能缓解销售压力。
3,5,6-TPA 是一种生长素类植物生长调节剂,在柑橘上,花后82 d 喷施15 mg·L-1的3,5,6-TPA 能够在不增加果实脱落的情况下,使采收期的单果质量比对照显著增加9.5%[11]。在甜橙上,花后8~11 周喷施3,5,6-TPA同样能够提高果实大小,改善果实品质[12]。在樱桃上,果实直径为13 mm 时喷施10 mg·L-1的3,5,6-TPA 可以显著促进果实膨大,大果实的产量增加了60%以上[13]。葡萄柚在果实直径大于22 mm 时喷施20 mg·L-1的3,5,6-TPA,果实单果质量比对照提高4.9%[14]。
以上研究表明,在果树上应用3,5,6-TPA对果实大小和成熟的调控具有积极作用,但是3,5,6-TPA调控果实生长发育的生理机制仍然未知。此外,国内还未见在荔枝生产上使用3,5,6-TPA 的研究报道。基于此,笔者以优质晚熟荔枝仙进奉为材料,探究3,5,6-TPA 对果实生长发育的调控,并分析其潜在原因,以期为3,5,6-TPA在荔枝上的高效利用提供理论依据和指导。
1 材料和方法
1.1 材料与试验设计
试验地位于广州市增城区郭仔农业有限公司荔枝园(113°41′ E,23°11′ N),年平均气温22.1 ℃,年平均降水量2 039.5 mm,试验材料为高接换种的16年生的晚熟优质荔枝品种仙进奉,砧木为妃子笑。
2022 年5 月9 日选择树势相对一致的6 株仙进奉作为供试材料,其中3 株在花后5 周(小果约1 g)整树喷施40 mg·L-1 3,5,6-TPA[15],另外3 株喷施清水为对照(CK),单株重复,喷至叶面滴水为止,每株树喷施用量为8 L。每个处理随机选择15 个枝进行挂牌,统计初始坐果数,此后每周统计落果数,每个处理随机各选20 个果挂牌测量横径和纵径。从处理开始至果实成熟时为止,每隔1 周采样1 次,每次取果实30 个,分开果皮、果肉、种子,放入液氮罐中速冻并带回实验室,-80 ℃冰箱保存备用,最后采收果实,测定果实品质。
1.2 测定指标及方法
1.2.1 果实动态发育分析 果实横径和纵径测量:从处理到采收期间,每隔1 周观察果实发育情况,并测量果实横径和纵径,参考李芳等[16]的方法测定,采用游标卡尺测定果实的横径(垂直于缝合线的最大距离)和纵径(从果蒂到果顶的距离),若在观测中有标记果实脱落或发育不正常的果实,则在同一穗上选择大小相近的正常果实代替。果形指数为果实纵径与横径的比值。
1.2.2 落果的动态分析 自喷施3,5,6-TPA 起统计初始坐果数,此后每隔1 周统计1 次落果数,直至最后采收。若存在裂果,则统计后再摘除,记录并统计分析坐果动态变化。累计落果率(cumulative abscission rate,CAR)计算公式如下:CAR/%=(X0-Xt)/X0×100。式中,X0为处理当天坐果量,Xt为t时的坐果量。
1.2.3 果实品质测定 (1)单果质量:果实成熟后采摘,使用电子天平称取每个挂牌果实质量。
(2)果实分级:随机采摘200 个果实称质量,根据果质量大小进行分级,分级标准参考T/GDNB 158—2023《增城主栽优质荔枝果品等级规格》团体标准,分为特级果(>30 g)、一级果(>23~30 g)、二级果(20~23 g)、等外果(<20 g)。
(3)可食率:称取每个果实单果质量、果皮质量和种子质量。可食率/%=(单果质量-果皮质量-种子质量)/单果质量×100。
(4)可溶性固形物(TSS)含量:每个处理3 个重复,每个重复取10个果,去果皮取果肉榨汁,用纱布过滤后使用糖度计进行测定,直接记录读数。
(5)可滴定酸(TA)含量:参考龙淑珍等[17]的方法,吸取2 mL 新鲜果汁于25 mL 三角瓶中,加入2滴1%酚酞作为指示剂,用0.1 mol·L-1 NaOH 溶液滴定,最后以苹果酸表示果实中主要可滴定酸含量。每个处理共3个重复,每个重复测定3次。按如下公式进行换算:
式中,C 为NaOH 溶液的浓度(mol·L-1); W 为样品体积(mL);V 为滴定时消耗NaOH 溶液的体积(mL),K为换算系数(0.067)。
(6)固酸比:可溶性固形物含量/可滴定酸含量。
(7)果皮色泽值:参照王利群等[18]的方法,摘取15 个果实,果皮色泽参数采用日本生产的Minolta CR-400型全自动测色色差仪,沿果面赤道一周均匀取4 个点,用色差仪测得L、a 和b 的数值后取平均值。a值表示红绿色度,b值表示黄蓝色度,L值表示色泽亮度。
1.2.4 叶片光合特性的测定 在每株树树冠的外部同一方位选择高度一致的8 枚老熟程度相同的叶片,挂牌标记,采用CIRAS-3 便携式光合仪(PP system,USA)于处理前和处理后的1、4、7、10、13、16、19、22 d 上午09:00—11:00 测量叶片的净光合速率(Pn),直到光合损伤恢复为止。
1.2.5 糖含量的测定 糖含量的测定参照胡志群等[19]的方法并略作改进。准确称取荔枝假种皮1 g于研钵中,微波炉杀酶40 s,加入2 mL 超纯水研磨成匀浆后转入10 mL 刻度试管中,反复清洗3~4 次,定容至10 mL,取2 mL 于离心管13 000 r·min-1离心10 min,上清液过 Sep-Pak®1cc(100 mg)C18 Cartridges(Waters)后于棕色样品瓶中待测。
使用 Angilent 1200 HPLC system(Agilent technologies,Waldbronn,Germany),对样品中的不同糖组分及含量进行检测,每个样品3次技术重复。
1.2.6 糖代谢相关酶的提取与活性测定 参照王惠聪等[20]的提取方法并略作改进。取果肉冻样粉末0.5 g,加入2 mL 预冷的提取缓冲液,缓冲液包含100 mmol·L-1 Hepes-NaOH(pH 7.5)、5 mmol·L-1 MgCl2、1 mmol·L-1 EDTA、2.5 mmol·L-1 DTT、0.5%Triton-100、1% BSA、5% PVPP 和10%甘油,冰浴下匀浆后转入2 mL离心管,13 000 r·min-1离心10 min,取1 mL 上清液加入到PD10(SephadexTM G-25 M,GE Healthcare)柱中脱盐,用2 mL 平衡液(包含25 mmol·L-1 Hepes-KOH(pH 7.5)、5 mmol·L-1 MgCl2、1 mmol·L-1 EDTA、30%甘油)冲洗,用2 mL冻存管收集冲洗液作为酶提取液。以上操作均在4 ℃下进行。
中性转化酶(NI):参考Lowell 等[21]的方法并进行改进。中性转化酶反应体系1 mL 包含1%蔗糖,100 mmol·L-1 Hepes-NaOH(pH 7.5),5 mmol·L-1 MgCl2,1 mmol·L-1 EDTA 和0.2 mL 酶提液,34 ℃水浴1 h后,沸水浴5 min终止反应,加入1.5 mL 3,5-二硝基水杨酸(DNS)测定还原糖含量;另取0.2 mL 经沸水浴10 min 的酶提液作为对照。测定在540 nm的吸光值,用两者OD 值的差计算还原糖合成速率,以分析纯葡萄糖作为标样制定DNS的标准曲线。
酸性转化酶(AI):反应体系1 mL 包含1%蔗糖,100 mmol·L-1 醋酸-磷酸钾缓冲液(pH 5.5)和0.2 mL 酶提取液,34 ℃下反应1 h后沸水浴5 min终止反应,其余操作同中性转化酶。
蔗糖合成酶(SS):参照胡志群等[19]的方法并加以改进,取0.1 mL酶液加入0.1 mL的反应液,反应液包括5 mmol·L-1 UDP,100 mmol·L-1蔗糖,5 mmol·L-1 NaF,在34 ℃下反应1 h 后,加入0.2 mL 30% KOH,转入沸水浴10 min 以终止反应,冷却至室温,加入0.8 mL纯水,其余操作同中性转化酶。
蔗糖磷酸合成酶(SPS)活性:参照赵智中等[22]的方法并略加修改,取0.1 mL 酶液加入0.1 mL 的反应液,反应液包括10 mmol·L-1 UDPG、5 mmol·L-1 6-磷酸果糖、15 mmol·L-1 6-磷酸葡萄糖、15 mmol·L-1 MgCl2、1 mmol·L-1 EDTA、1 mmol·L-1 硼酸缓冲液(pH=8.0)在34 ℃下反应1 h 后,加入0.2 mL 30%KOH,转入沸水浴10 min 以终止反应,冷却至室温,混匀后加入3.5 mL 蒽酮溶液(0.15 g 蒽酮溶于100 mL 81%硫酸),在40 ℃下反应20 min 后冷却。另取0.1 mL 经沸水浴10 min 的酶提液作为对照。其余操作同上。测定在620 nm 的吸光值,用两者OD 值的差计算蔗糖的合成速率,以分析纯蔗糖为标样制作标准曲线。
1.2.7 IAA 和ABA 含量测定 参照徐婧等[23]的方法测定果实中IAA 和ABA 含量,取样品0.5 g,使用超高效液相色谱-三重四级杆质谱联用仪(Waters Xevo UPLC-TOD-MS)分析提取的样品。
1.3 数据分析
采用SPSS 22 软件进行数据差异显著性分析,采用Origin 2022绘图。
2 结果与分析
2.1 3,5,6-TPA 对仙进奉荔枝果实生长发育和品质的影响
2.1.1 对果实发育动态和落果的影响 在花后5 周喷施40 mg·L-1的3,5,6-TPA 荔枝果实横径和纵径的动态变化情况如图1 所示,喷施前果实横径、纵径分别为11、18 mm,处理后的3~7 周,处理的纵横径均显著大于对照。果实采收时,处理的果实纵径达到了39.0 mm,果实横径达到了36.1 mm,比对照分别增加了7.4%、8.7%。果实成熟时,对照果实的果形指数为1.09,处理的果形指数为1.08,无明显差异。
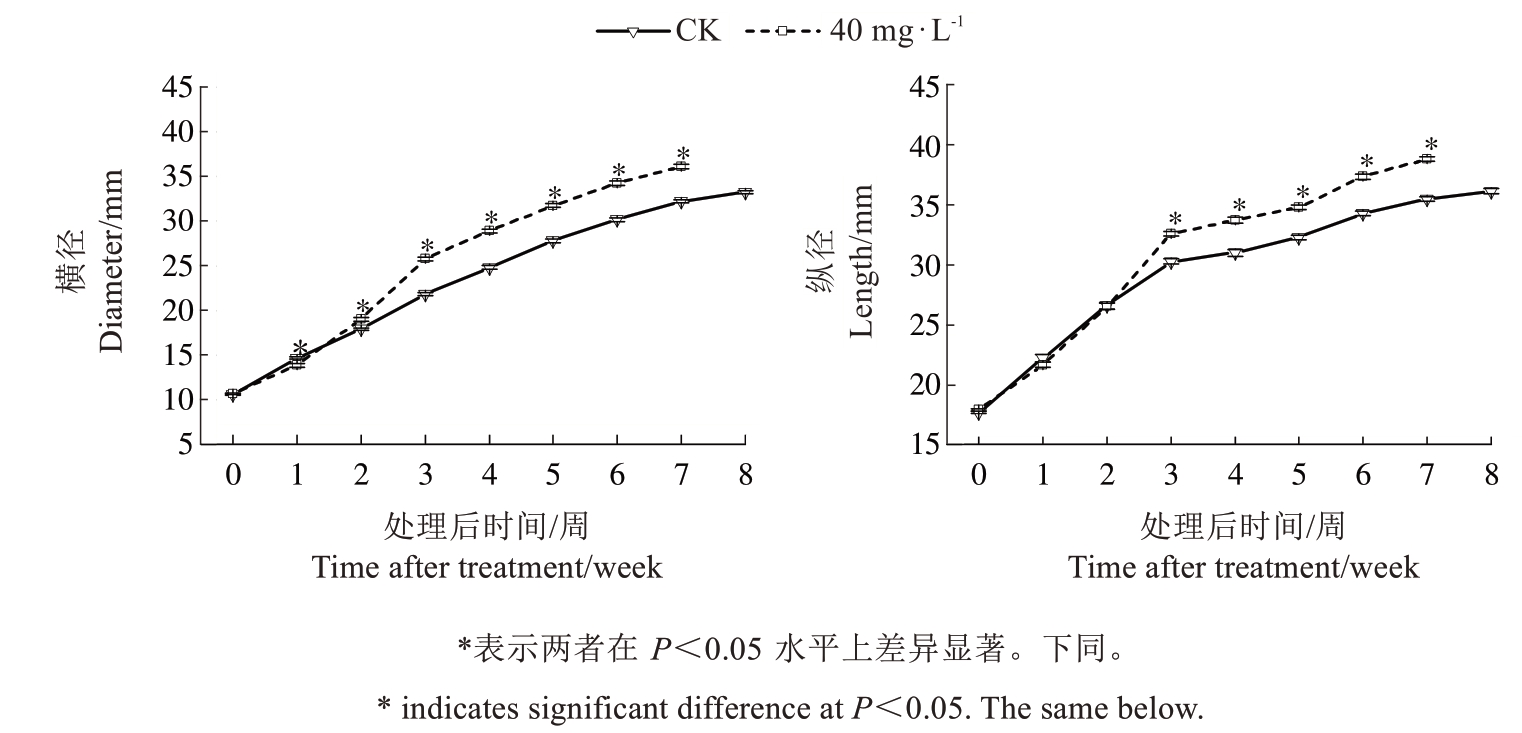
图1 花后5 周喷施3,5,6-TPA 对仙进奉果实横径和纵径发育的影响Fig. 1 Effects of 3,5,6-TPA application at 5 weeks after flowering on the transverse and longitudinal diameter development of Xianjinfeng fruit
在花后5 周喷施40 mg·L-1的3,5,6-TPA 对仙进奉荔枝落果的影响如图2 所示,在处理后第1 周,处理和对照的累计落果率无显著差异,处理后第2~3周,对照的累计落果率高于处理,尤其是在第2周达到显著水平。这里需要特别指出的是,尽管处理前3 周的累计落果率低于对照组,但果穗上部分果实的发育出现果实停止生长和果皮变黄现象(图3),这些发育受阻的果实从3 周开始陆续脱落,因此导致经过3,5,6-TPA 处理的仙进奉荔枝累计落果率从第4 周开始直至采收,均高于对照,达到了一定的疏果效果。以上结果说明,花后5 周喷施40 mg·L-1 3,5,6-TPA,会造成部分幼果的发育障碍,致使果实前期落果少,后期落果多,具有一定的疏果作用。
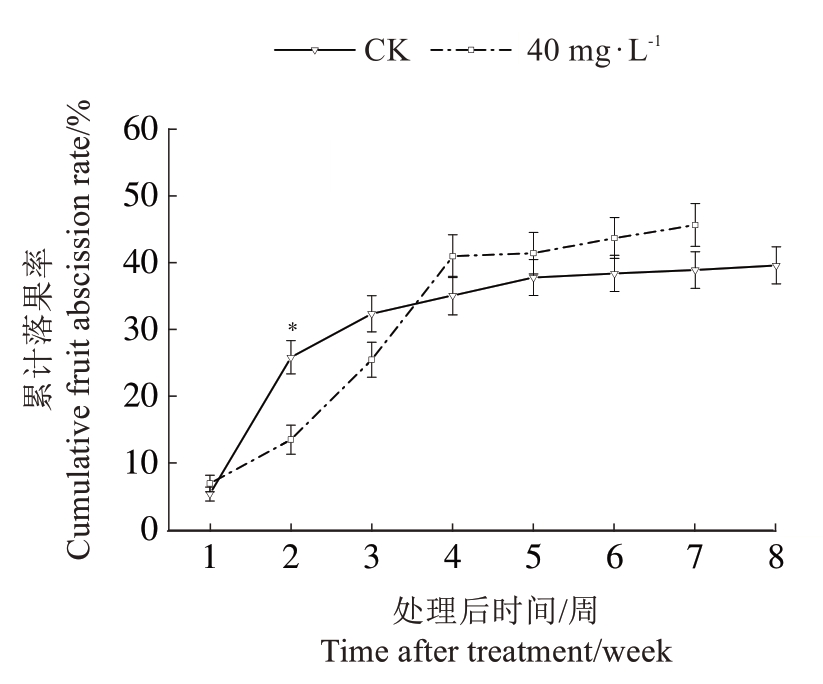
图2 花后5 周喷施3,5,6-TPA 对仙进奉果实落果的影响
Fig. 2 Effects of 3,5,6-TPA application at 5 weeks after flowering on fruit abscission of Xianjinfeng
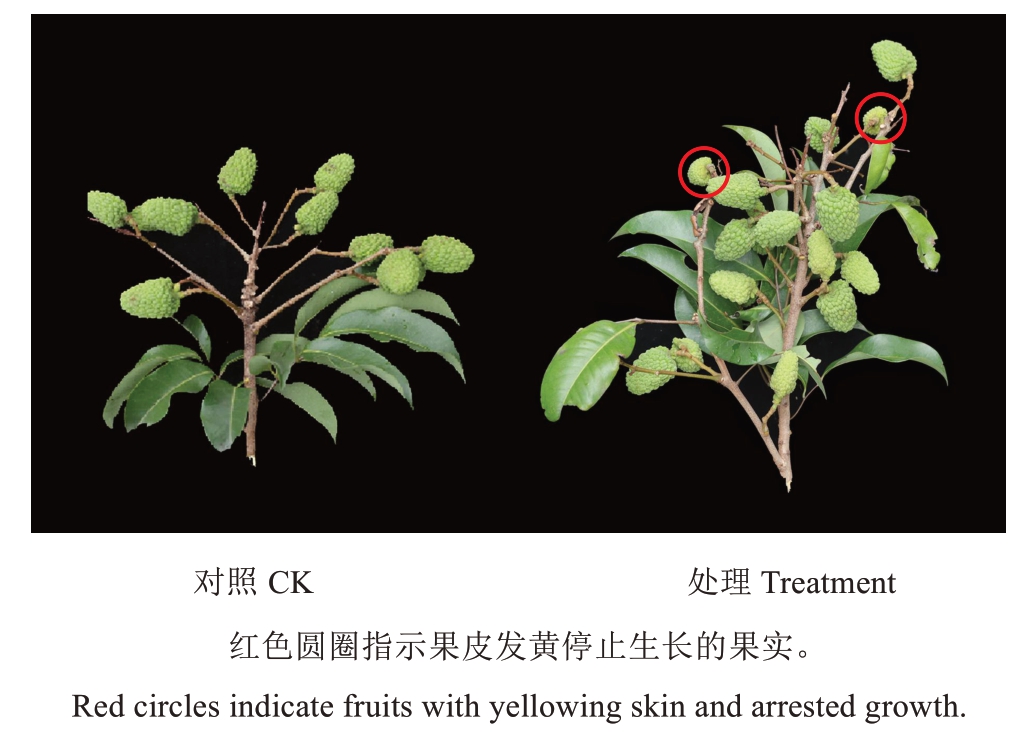
图3 3,5,6-TPA 处理后第2 周对仙进奉果实的影响Fig. 3 Effects of 3,5,6-TPA treatment in the second week on Xianjinfeng fruit
如图4 所示,喷施3,5,6-TPA 促进果皮提前着色,可以促进果实提早一周成熟;在单果质量方面,处理的平均单果质量达到了25.0 g,而对照仅为22.9 g,处理比对照显著提高了9.2%(表1)。
表1 花后5 周喷施3,5,6-TPA 对仙进奉果实成熟期和单果质量的影响
Table 1 Effects of 3,5,6-TPA application at 5 weeks after flowering on the maturity date and single fruit mass of Xianjinfeng

注:同列不同小写字母表示两者差异显著(P<0.05)。下同。
Note:Different small letters in the same column indicate significant difference at P<0.05. The same below.
处理Treatment CK 40 mg·L-1 3,5,6-TPA单果质量Single fruit mass/g 22.90 b 25.00 a成熟日期Maturation date 7月4日Jul. 4 6月27日Jun. 27
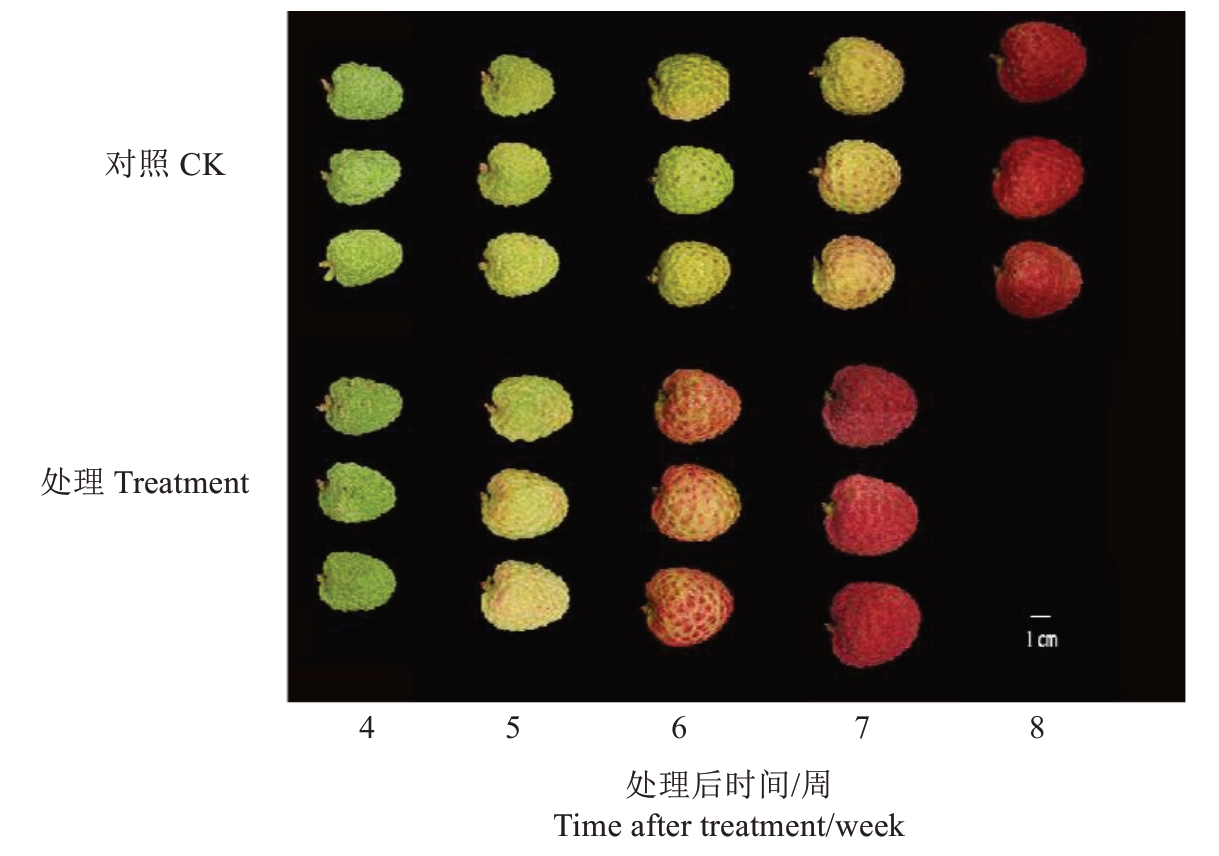
图4 3,5,6-TPA 处理对仙进奉果实成熟进程的影响
Fig. 4 Effects of 3,5,6-TPA treatment on the maturation process of Xianjinfeng fruit
依据《增城主栽优质荔枝果品等级规格》仙进奉果实大小分级标准,分为特级果(>30 g)、一级果(>23~30 g)、二级果(20~23 g)、等外果(<20 g)四个级别。如图5所示,处理和对照都没有特级果,3,5,6-TPA处理的一级果比率为64.6%,而对照仅为27.2%,处理比对照显著提高了37.4个百分点。对照的等外果比率为24.5%,而处理只有10.7%,处理比对照显著降低了13.8 个百分点。说明3,5,6-TPA 处理可以显著提高一级果的比率和降低等外果的比率。
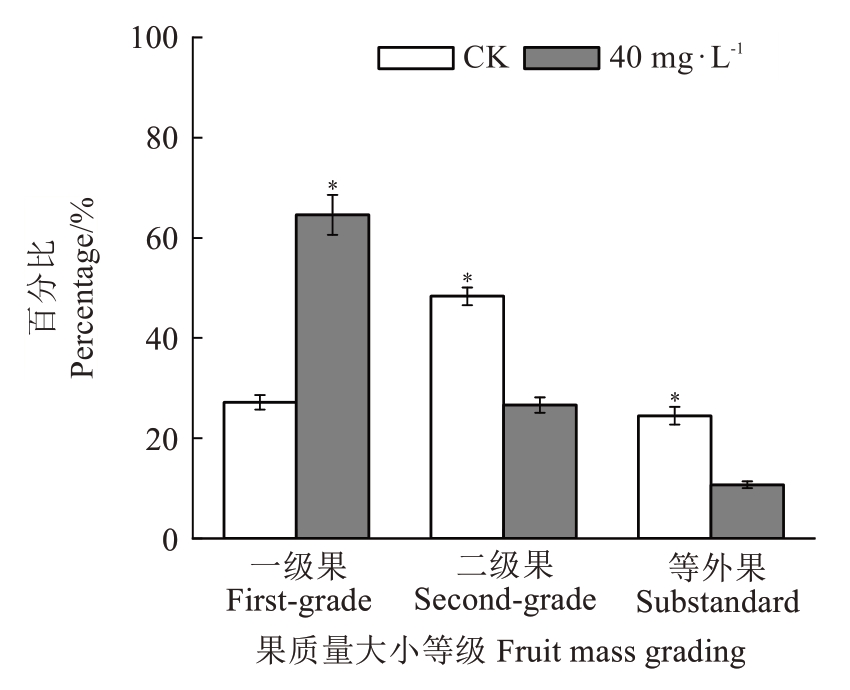
图5 花后5 周喷施3,5,6-TPA 对仙进奉单果质量分布频率的影响
Fig. 5 Effects of 3,5,6-TPA application at 5 weeks after
flowering on the frequency distribution of single fruit mass in Xianjinfeng
2.1.2 对果实品质影响 荔枝的可溶性固形物含量、可滴定酸含量、固酸比、可食率、焦核率等是评判荔枝品质的重要指标,在花后5 周喷施3,5,6-TPA 对荔枝果实内在品质的影响如表2 所示,所测指标均没有显著差异。
表2 花后5 周喷施3,5,6-TPA 对仙进奉果实品质的影响
Table 2 Effects of 3,5,6-TPA application at 5 weeks after flowering on the fruit quality of Xianjinfeng
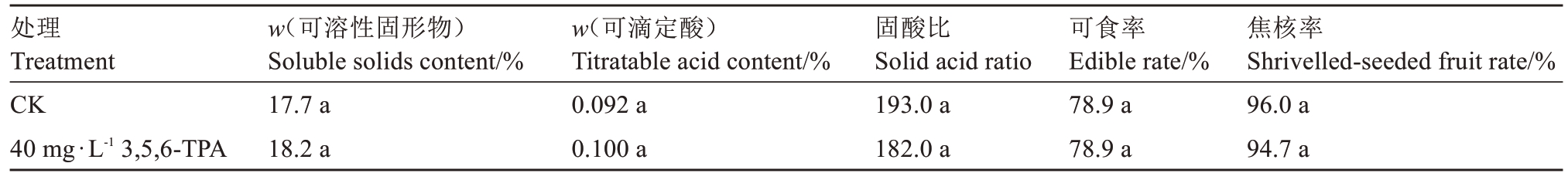
处理Treatment CK 40 mg·L-1 3,5,6-TPA w(可溶性固形物)Soluble solids content/%17.7 a 18.2 a w(可滴定酸)Titratable acid content/%0.092 a 0.100 a固酸比Solid acid ratio 193.0 a 182.0 a可食率Edible rate/%78.9 a 78.9 a焦核率Shrivelled-seeded fruit rate/%96.0 a 94.7 a
2.1.3 对果实着色的影响 花后5 周喷施3,5,6-TPA 对仙进奉果实处理后第5 周到采收期的色泽变化如图6 所示。在处理后的第5 周,处理与对照的a值不存在显著差异,在处理后的第6~7 周经过处理的果皮a 值显著高于对照。到最后采收期,对照的果皮a 值为28.3,与处理的29.0 无显著差异。以上数据说明处理的果皮颜色比对照更早转变红色,到采收期无显著差异。处理的b 值从处理后的第5 周到采收期呈现下降的趋势,而对照的b 值在处理后第5~6周呈上升趋势,在处理后第6周到采收期呈下降趋势。在处理后的第6~7周,对照的果皮b色度值显著高于处理。到最后采收期,处理与对照的果皮b 值无显著差异。处理的果皮L 值呈一直下降的趋势,直到采收期,而对照的果皮L 值在处理后第5~6周呈上升趋势,从处理后第6 周到采收期呈下降趋势。与对照相比,在处理后第7 周,处理的果皮L 值显著高于对照。在采收期,处理与对照的果皮L 值分别为34.9、34.2,二者无显著差异。以上数据说明处理的果皮亮度比对照的果皮亮度更早的下降,即果皮颜色变深更早,到采收期无显著差异。
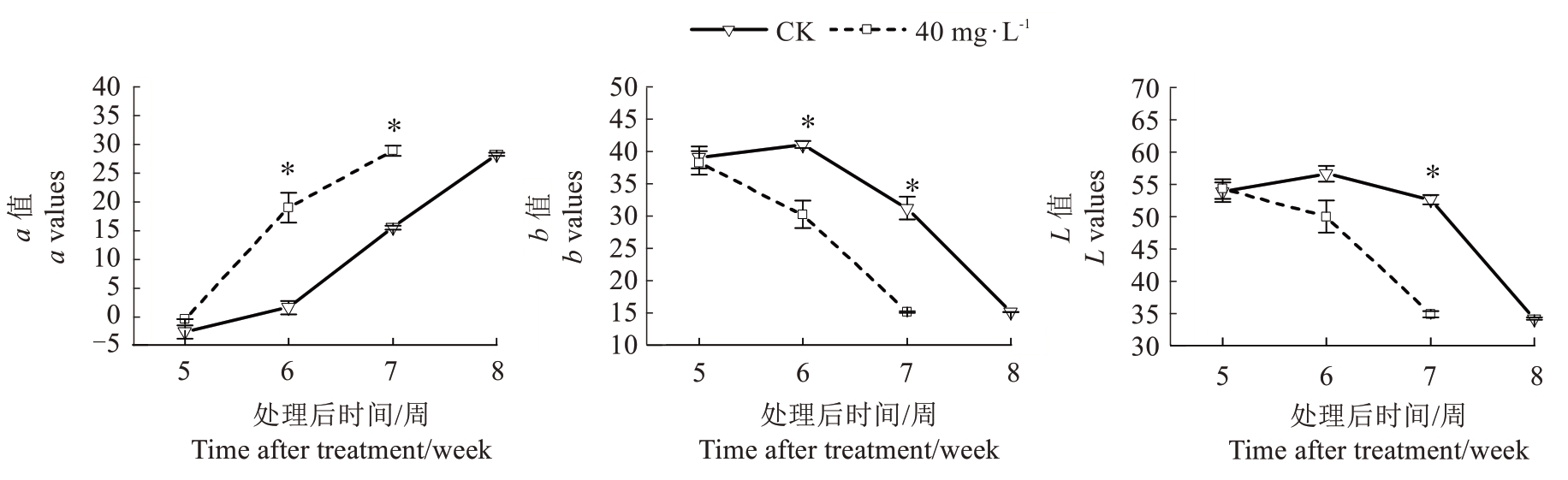
图6 3,5,6-TPA 对仙进奉成熟过程中果皮色泽的影响
Fig. 6 Effects of 3,5,6-TPA on the fruit skin color during the maturation process of Xianjinfeng
综上所述,在仙进奉荔枝花后5周喷施40 mg·L-1的3,5,6-TPA 可以显著提高采收前2 周内果皮的色度值a,并同时显著降低色度值b 和L,使仙进奉果实提早1周转色和成熟。
2.2 3,5,6-TPA 促进荔枝果实增大和成熟的原因分析
2.2.1 对叶片光合作用的影响 如图7 所示,在喷施3,5,6-TPA 后1 d,仙进奉荔枝叶片净光合速率显著低于对照,且持续7 d 左右,然后处理的净光合速率会略高于对照,到最后保持大致相同。以上数据说明喷施3,5,6-TPA 后能暂时诱导荔枝叶片的光合作用损伤。
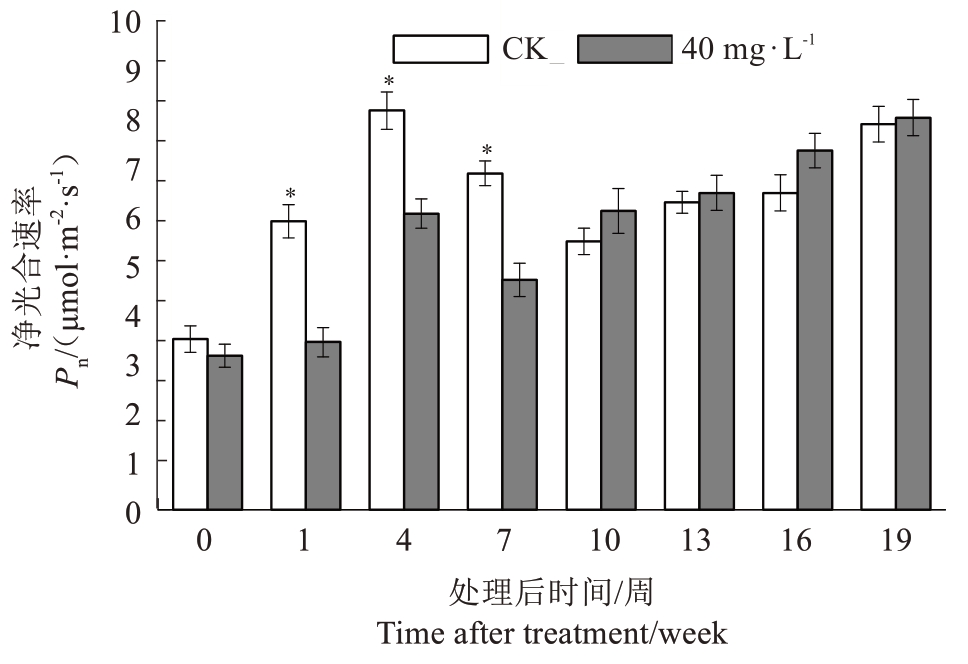
图7 花后5 周喷施3,5,6-TPA 对仙进奉叶片净光合速率的影响
Fig. 7 Effects of 3,5,6-TPA application at 5 weeks after flowering on the net photosynthetic rate of leaves in Xianjinfeng
2.2.2 对果实发育过程中糖分含量和相关代谢酶活性的影响 为了分析喷施3,5,6-TPA 对仙进奉荔枝果实糖分含量的影响,测定了喷施3,5,6-TPA 后不同时期的糖组分变化,结果如图8-A 所示,在处理后第2~3 周,处理的蔗糖含量迅速上升,且上升幅度明显大于对照,到第3 周,处理的蔗糖含量达到最高,为85.1 mg·g-1,对照的蔗糖含量为55.2 mg·g-1,两者的差值最大。从第3 周开始,处理的蔗糖含量开始下降,到最后采收时含量为51.1 mg·g-1,而对照的蔗糖含量则在第4 周达到最高值,为75.5 mg·g-1,从第4周开始下降,到最后采收时的含量为44.9 mg·g-1。果糖含量从处理到最后采收时均呈上升趋势(图8-B),处理后第3周具有显著差异,处理比对照显著提高了57.3%。到最后采收时处理与对照没有显著差异,分别为39.6 mg·g-1和42.5 mg·g-1。葡萄糖含量大致呈先上升后下降再上升的变化趋势(图8-C),3,5,6-TPA 处理后1 周对照的葡萄糖含量显著高于处理。对照在前2周快速积累葡萄糖,于第2周达到最大积累量(44.9 mg·g-1),与处理无显著差异。处理后第3周,处理的葡萄糖含量最高,达到59.3 mg·g-1,比对照显著提高了109.5%,其他时期,处理和对照的葡萄糖含量差异不显著。处理和对照总糖含量的变化趋势存在差异(图8-D),在处理后第1 周,处理和对照的总糖含量分别为43.3、48.9 mg·g-1,对照的总糖含量略高于处理,但不具有显著差异。随着果实发育,总糖含量迅速积累,在处理后第3周,处理和对照总糖含量差值最大,对照的果实假种皮的总糖含量为95.7 mg·g-1,而处理的总糖含量达到163.7 mg·g-1,处理比对照显著提高了71.1%。其他时期对照和处理的总糖含量差异不显著。
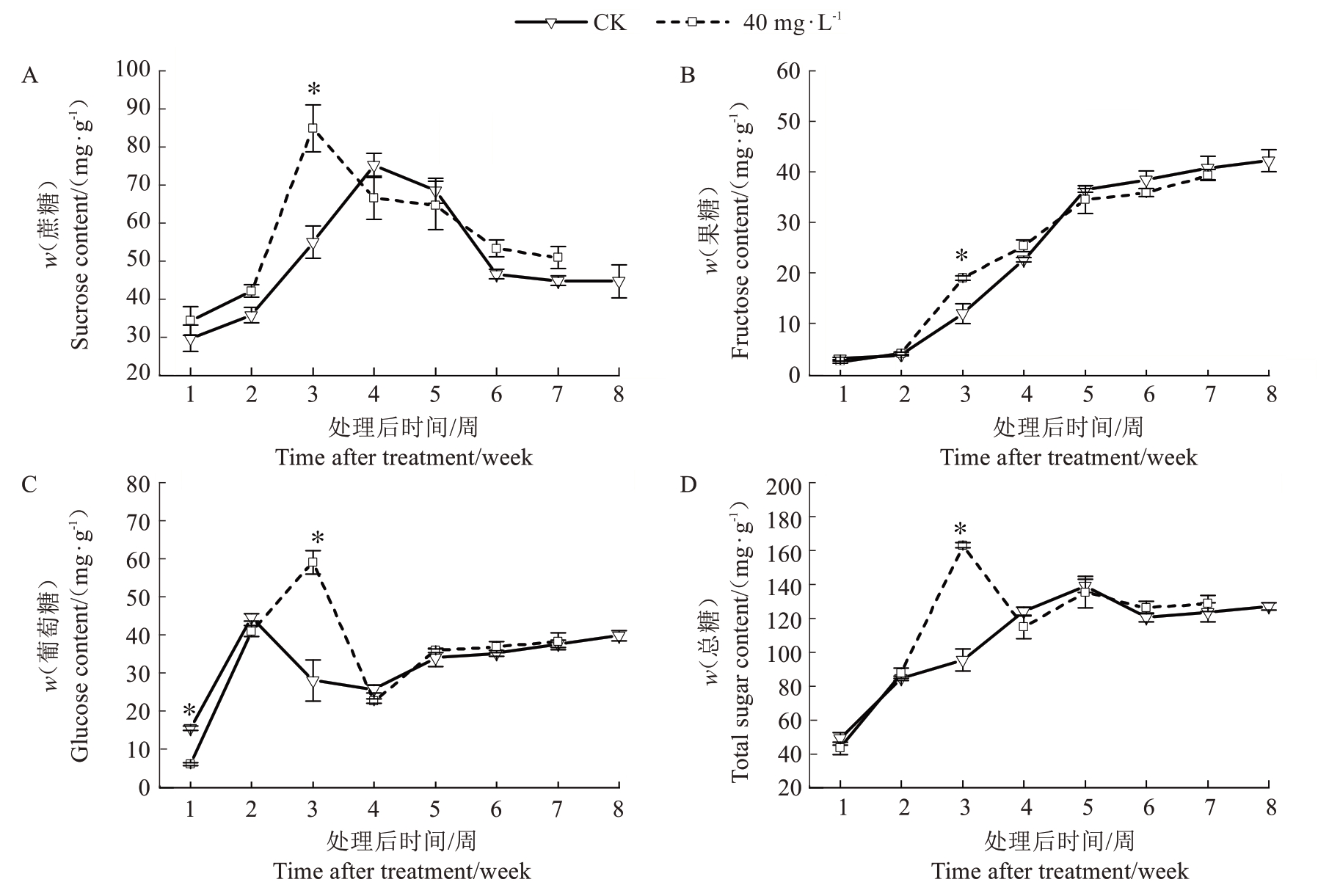
图8 花后5 周喷施3,5,6-TPA 对仙进奉假种皮糖组分含量的影响
Fig. 8 Effects of 3,5,6-TPA application at 5 weeks after flowering on the sugar composition content in the aril of Xianjinfeng
荔枝果实发育过程中假种皮蔗糖代谢关键酶包括酸性转化酶(AI)、中性转化酶(NI)、蔗糖合成酶(SS)和蔗糖磷酸合成酶(SPS)。如图9-A 所示,荔枝假种皮的AI 活性均呈先上升后下降再上升的趋势,喷施3,5,6-TPA 的荔枝假种皮的AI 活性在前3 周呈上升趋势,到第3 周最高,达到2.8 mg·g-1·h-1,且此时处理与对照的酶活性差异最大,处理比对照显著提高22.3%,在第3~4 周处理的AI 活性迅速下降,到第4 周,对照AI 活性显著高于处理,其他时期对照与处理均未有显著差异。
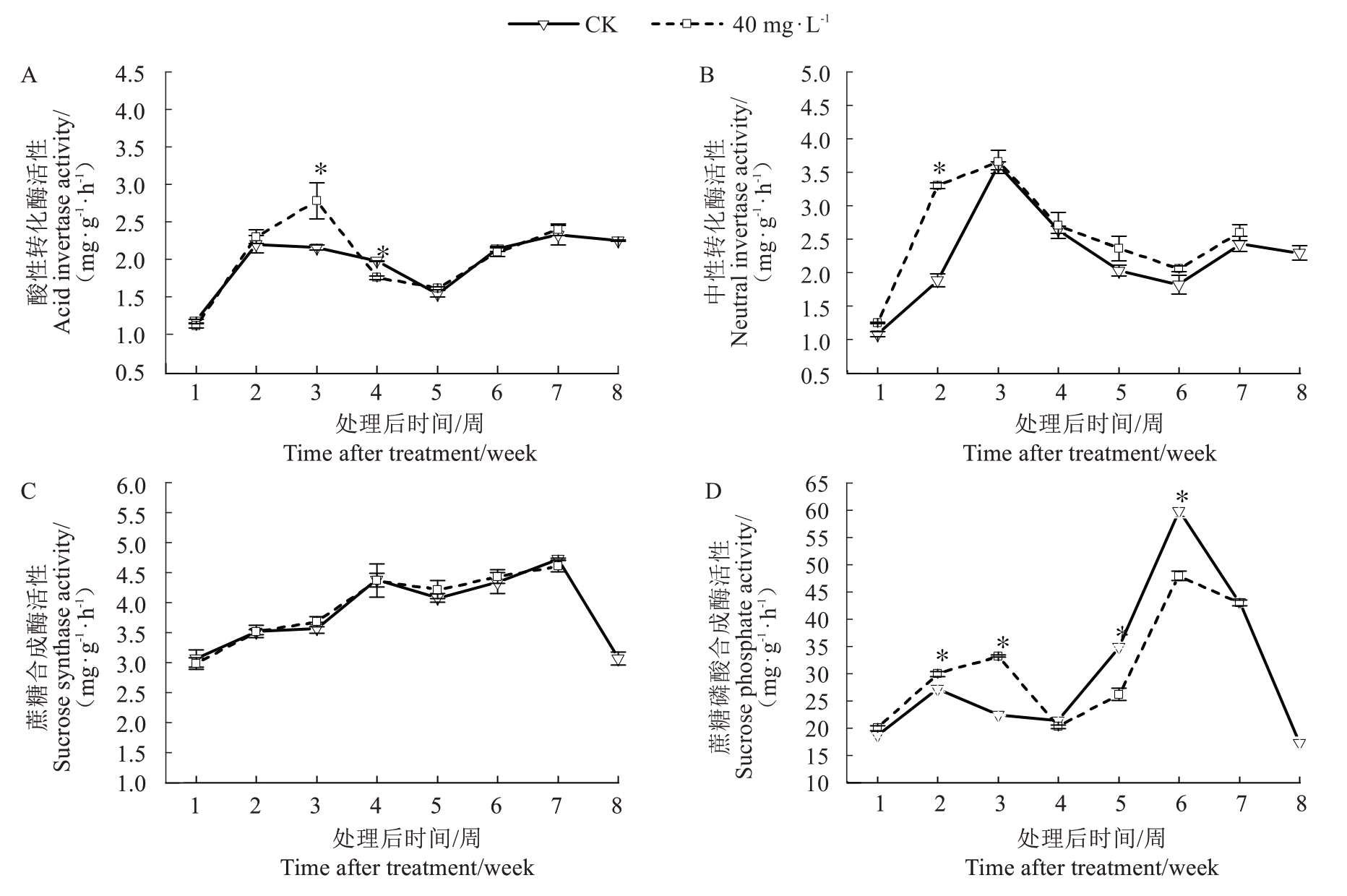
图9 花后5 周喷施3,5,6-TPA 对仙进奉假种皮中酸性转化酶(A)、中性转化酶(B)、蔗糖合成酶(C)和蔗糖磷酸合成酶(D)活性的变化
Fig. 9 Effects of 3,5,6-TPA application at 5 weeks after flowering on the activities of acid invertase (A), neutral invertase (B),sucrose synthase (C), and sucrose phosphate synthase (D) in the aril of Xianjinfeng
如图9-B 所示,从喷施3,5,6-TPA 开始到果实采收,NI活性呈先上升后下降再上升的趋势,在假种皮发育的早期,NI活性较低,随着果实的发育,NI活性升高,在处理后第3 周开始下降,随后在第6 周又开始上升。比较处理与对照的NI活性,处理第2周,酶活性差异最大,具有显著差异,经过处理的NI活性为3.3 mg·g-1·h-1,而对照的NI活性仅为1.8 mg·g-1·h-1,其他时期的NI活性均未有显著差异。
如图9-C 所示,SS 活性随着果实发育大致呈先上升后下降再上升的趋势,且处理与对照的SS活性在所测的时期均未发现显著差异。在对照的最后一个时期,SS 活性迅速下降,这可能与果实“退糖”,或者高温天气的影响有关。
如图9-D 所示,SPS 活性整体呈现先上升后下降再上升再下降的趋势,经过3,5,6-TPA处理的仙进奉假种皮SPS 活性在前3 周呈现上升趋势,随后下降,从第4周开始又急速上升,在第6周又开始下降,对照的SPS 活性在前两周呈现上升趋势,随后的趋势同处理一致。前3 周处理的SPS 活性均高于对照,且在第3 周差异最大,分别为33.3 mg·g-1·h-1和22.5 mg·g-1·h-1,在第4~6 周对照的SPS 活性呈上升趋势且高于处理,对照的SPS 活性在5~6 周显著高于处理。
2.2.3 3,5,6-TPA 对仙进奉荔枝果实各组织中IAA含量的影响 仙进奉荔枝果皮、假种皮和种子中IAA 含量的测定结果如图10 所示。随着果实发育和成熟,仙进奉荔枝果皮和假种皮内源IAA 含量大致呈先上升后下降的趋势,图10-A 表明,在处理后0~3 周,处理与对照的仙进奉果皮中IAA 含量均比较低,从第3 周开始,随着果实发育,IAA 含量迅速增加;与对照相比,处理后第2~4 周,经过处理的果皮IAA 含量增长速度高于对照且从第3 周开始具有显著差异,在第4周,两者差异最大,处理的果皮IAA含量为294.9 ng·g-1,而对照的果皮IAA 含量为91.7 ng·g-1,处理比对照显著提高221.6 %。处理的果皮IAA 含量从第4 周开始下降,而对照的果皮IAA 含量则在第5 周开始下降。仙进奉荔枝假种皮IAA 含量变化如图10-B所示,在处理后前3周,处理与对照没有显著差异,从第3 周开始,经过处理的荔枝假种皮IAA 含量增加速度高于对照,在第3~5 周,处理的荔枝假种皮IAA 含量高于对照且比对照提前1 周下降。如图10-C 所示,处理的种子中IAA 含量呈降-升-降-升-降的变化趋势,在处理后第2~5 周,处理的种子IAA 含量高于对照,且比对照提前1 周开始下降,直至采收。
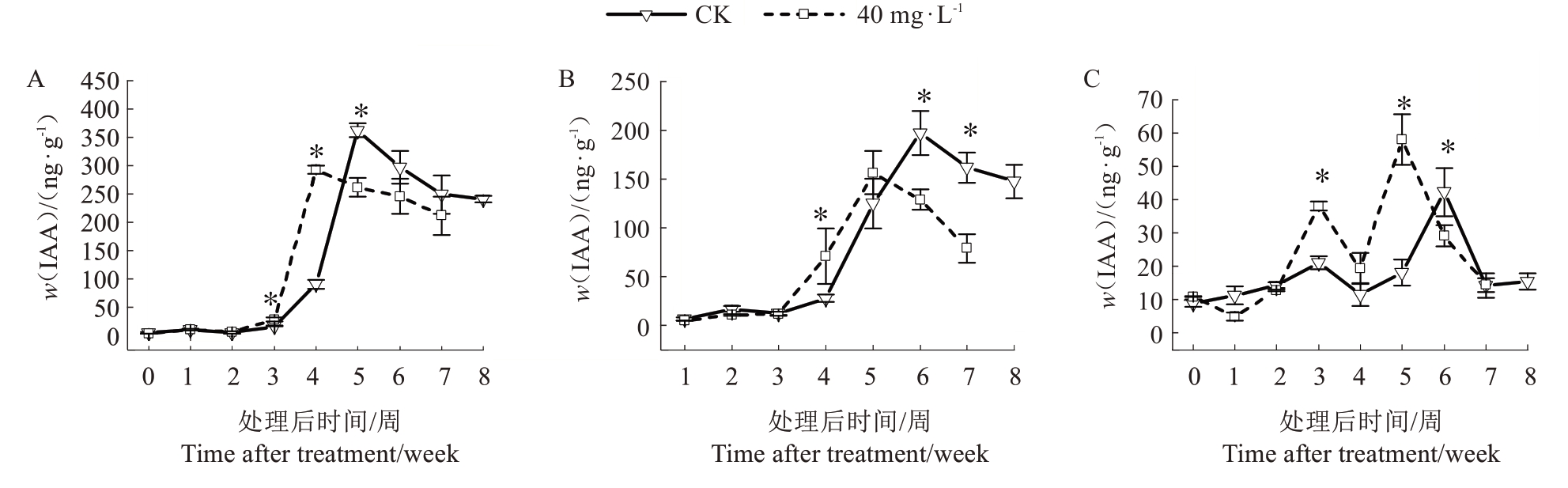
图10 花后5 周喷施3,5,6-TPA 对仙进奉果皮(A)、假种皮(B)、种子(C)中IAA 含量的影响
Fig. 10 Effects of 3,5,6-TPA application at 5 weeks after flowering on the IAA content in the peel (A), aril (B) and seed(C) of Xianjinfeng
2.2.4 3,5,6-TPA 对仙进奉荔枝果实各组织中ABA含量的影响 荔枝是一种非跃变型水果,前人研究发现,调控非跃变型果实的关键激素,更倾向于认为是脱落酸(ABA)。荔枝果实成熟过程中,两个主要的生理变化,脱色(叶绿素的降解)和色素沉着(花青素的合成)在视觉上是明显的。采用超高效液相色谱-三重四级杆质谱联用仪测定了喷药后荔枝各组织中ABA 含量,结果如图11 所示,处理与对照中果实成熟发育过程中ABA 含量积累趋势大致相同。在果皮中(图11-A),ABA 含量呈先下降后上升的趋势,在喷后第3 周,两者差异最大,处理比对照显著提高278.1%;由于发育早期果实太小,假种皮难采集,只能从喷后1 周开始采集。在假种皮中(图11-B),ABA 含量呈先升高后轻微下降的趋势,在处理后第1 周和第3 周,处理显著高于对照。在种子中(图11-C),处理的ABA 含量在喷药后1~6 周显著高于对照。在各个组织中,处理的果实ABA 含量高于对照,且部分时期具有显著差异,由此推断,ABA 引起了仙进奉果实发育期的转变,调控了荔枝果实的发育成熟进程。
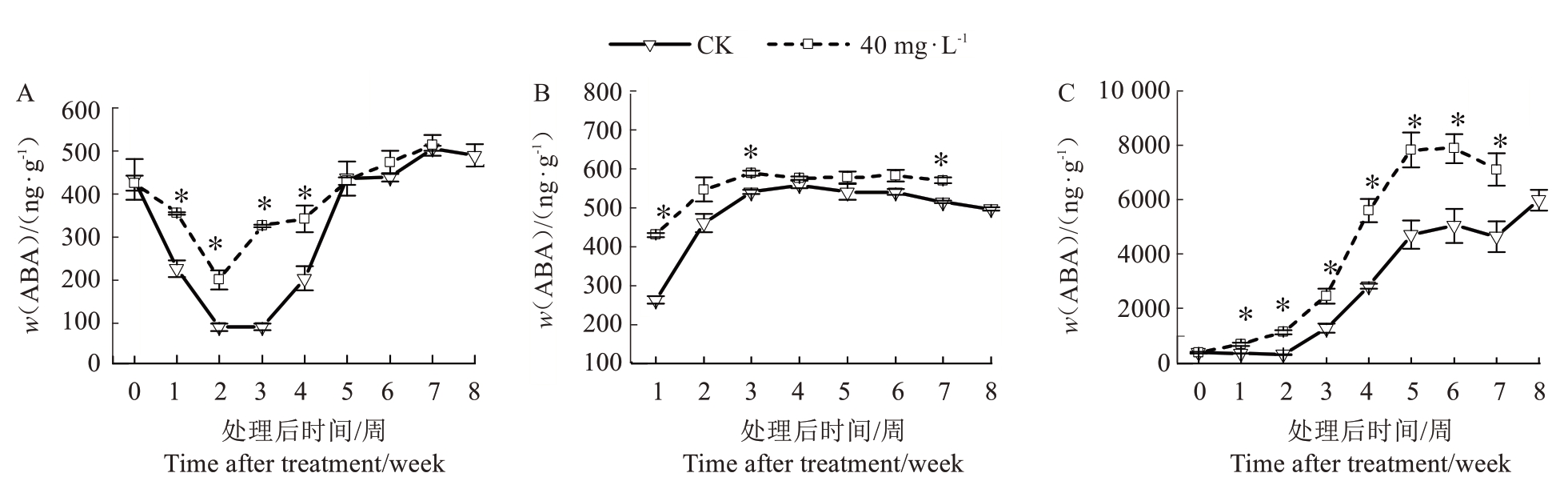
图11 花后5 周喷施3,5,6-TPA 对仙进奉果实发育成熟过程中果皮(A)、假种皮(B)、种子(C)中ABA 含量的影响
Fig. 11 Effects of 3,5,6-TPA application at 5 weeks after flowering on the ABA content in the pericarp (A), aril (B) and seed(C) during the fruit development and maturation process of Xianjinfeng
3 讨 论
3.1 3,5,6-TPA增大果实的原因分析
果实大小是影响果实商品价值的关键因素之一,通过优化标准栽培措施,如施肥、灌溉和修剪,果实大小的增加是有限的[24]。在农业生产中,生长素可用于诱导果实增大和减少采前落果[25]。在荔枝中,常用NAA、2,4-D 来促进果实增大[26-27]。但是,2,4-D 可能危害健康,它可能被禁止在果园中使用。3,5,6-TPA 是一种人工合成的生长素类植物生长调节剂,在李子[8]、樱桃[28]上喷施3,5,6-TPA 可以显著提高采收时果实大小。笔者也获得了相似的研究结果,喷施3,5,6-TPA 能在不减少果实数量的情况下显著提高仙进奉果实单果质量和优果率,说明3,5,6-TPA促进木本果树果实增大存在普遍性。
根据光合作用产物的输出与输入特性,植物组织和器官可分为源和库。植物的生长发育依赖于光合产物在不同组织间的协调运输与分配[29]。研究表明,3,5,6-TPA 促进果实生长可能是通过增强库强度,促进光合产物向果实转运,以及增加碳水化合物的积累[30]。笔者在本研究中测定了喷施3,5,6-TPA后荔枝叶片光合作用的变化,发现处理初期(前7 d)净光合速率受到抑制,随后逐渐恢复。这一初期的光合速率下降减少了光合产物的产生,尽管前3 周的累计落果率低于对照组,但果穗上的小果发育已受胁迫,出现黄化和萎缩现象。这可能是处理影响了荔枝叶片的源功能,使后期果实脱落。同时,光合产物的重新分配可能使得未脱落的果实获得更多碳水化合物,从而促进果实发育。
果实的库强度是决定光合产物向其运输的关键因素,而库活力,即果实糖代谢酶活性,是影响库强度的重要指标[31]。碳水化合物代谢对果实最终大小的控制至关重要[32]。蔗糖通常通过韧皮部直接运输或转化为六碳糖后进入果实,其进入速率依赖于源与库之间的浓度梯度[19]。转化酶,包括酸性和中性转化酶,主要维持源库间的蔗糖浓度梯度,对光合产物的运输至关重要。液泡中的可溶性酸性转化酶参与调节己糖与蔗糖的比例,改变细胞渗透压,增强细胞壁的可塑性,促进细胞伸长[33]。蔗糖磷酸合成酶在蔗糖生物合成中起关键作用,尤其在脐橙果实膨大期糖积累中发挥重要作用[34]。蔗糖合成酶通过可逆反应调节细胞内外的浓度梯度[35]。笔者发现,3,5,6-TPA 处理后,荔枝假种皮中的转化酶活性在处理前3周高于对照,蔗糖磷酸合成酶活性在处理后4周也高于对照,而蔗糖合成酶活性无显著差异。3,5,6-TPA 处理增强了果实对碳水化合物的吸收能力,通过测定假种皮中的糖组分,发现处理后第3 周,蔗糖、果糖和总糖含量显著增加。这表明3,5,6-TPA可能通过改变假种皮中相关代谢酶活性,增大源库间的浓度梯度,加速蔗糖向果实的卸载,提高前期假种皮中的蔗糖和果糖含量,同时提高总糖含量,为果实发育提供更多能源和碳源,促进果实增大。此外,细胞内溶质浓度的增加,有助于细胞吸收更多水分,进一步促进果实膨大。
植物生长素已经被证实可以促进果实持续膨大[36],果实的膨大主要由细胞的增殖和扩大所决定,果实所需的生长素大多是果实内部自己提供的,生长素调控果实的生长发育主要是参与协调细胞的分裂、扩增和分化[37]。同时内源IAA 含量的提高,也可以导致细胞壁的松弛,降低细胞膨压,从而降低细胞水势,促进果实细胞扩张,吸收更多水分,增加碳水化合物含量,促进果实发育,最终影响果实大小[27]。在本研究中,对喷施3,5,6-TPA 后荔枝果实中各组织内源IAA 含量进行测定,结果表明,3,5,6-TPA 可以在处理后3~4 周显著提高果实各组织中IAA 含量,由此推测3,5,6-TPA 促进荔枝果实增大的原因也可能与其促进荔枝果实中内源IAA合成有关。
3.2 3,5,6-TPA促进果实成熟的原因分析
激素在调控果实成熟方面一直是研究的焦点。研究发现,生长素具有调节果实成熟的作用,是控制果实成熟的因素之一[38]。生长素水平的下降与肉质水果成熟的开始有关,并且可能是成熟相关过程发生的必要条件[39]。笔者在本研究中发现,处理的荔枝果皮和假种皮内源IAA 含量比对照要提前1 周下降。因此推断,果实中IAA 含量的提前下降可能有助于果实成熟。
ABA 在非呼吸跃变型果实的成熟过程中起主导作用[40-42]。在草莓中,ABA 能促进果实着色、软化和乙烯释放,加速成熟[43];在葡萄中,ABA 能上调与成熟相关的基因表达,提高花色苷含量,促进果实成熟[44]。在荔枝中,ABA 也被报道能促进叶绿素分解和花色苷合成,加速果实成熟[45]。本研究显示,喷施3,5,6-TPA 可以提高果实各组织中内源 ABA 含量,由此推断3,5,6-TPA 促进果实成熟也可能与其提高了果实内源ABA含量有关。
综上所述,3,5,6-TPA 促进荔枝果实增大的潜在原因可能包括以下几点:首先,3,5,6-TPA 短暂抑制了荔枝叶片的光合作用,导致部分果实在早期发育阶段生长受阻,甚至在后期自然脱落,从而起到了类似疏果的效果,优化了果实的负载量;其次,该处理显著提高了果实发育前期果皮、假种皮和种子中的内源生长素(IAA)含量,这可能促进了细胞的伸长和分裂,进而推动果实的膨大;此外,3,5,6-TPA 还增强了果实中细胞壁转化酶、酸性转化酶、中性转化酶以及蔗糖磷酸合成酶活性,这些酶活性的提升有助于促进糖分的合成与积累,进一步推动果实的生长和发育。3,5,6-TPA 促使果实成熟提前的潜在原因可能涉及以下两个方面:一方面,3,5,6-TPA 处理提高了果实发育期间果皮、假种皮和种子中的内源ABA 含量,ABA 是调控果实成熟的关键激素之一,其含量的增加可能加速了果实的成熟进程;另一方面,该处理促进了果实成熟期间果皮和假种皮中内源IAA 含量的提前下降,IAA 含量的降低可能解除了对果实成熟的抑制作用,从而促使果实提前进入成熟阶段。
4 结 论
花后5 周喷施40 mg·L-1的3,5,6-TPA 可以在对仙进奉荔枝的内在品质无显著影响的情况下,短暂抑制荔枝叶片净光合速率,改变假种皮中相关代谢酶活性,调控果实中各组织内源IAA 和ABA 含量,从而增加荔枝的果实大小和提高优质果率,促进果实提前成熟,有效提高荔枝产业的经济效益,但其分子机制仍需进一步研究。
[1] KLEE H J,GIOVANNONI J J. Genetics and control of tomato fruit ripening and quality attributes[J]. Annual Review of Genetics,2011,45:41-59.
[2] JIA H F,WANG Y H,SUN M Z,LI B B,HAN Y,ZHAO Y X,LI X L,DING N,LI C,JI W L,JIA W S. Sucrose functions as a signal involved in the regulation of strawberry fruit development and ripening[J]. New Phytologist,2013,198(2):453-465.
[3] HARADA T,KURAHASHI W,YANAI M,WAKASA Y,SATOH T. Involvement of cell proliferation and cell enlargement in increasing the fruit size of Malus species[J]. Scientia Horticulturae,2005,105(4):447-456.
[4] HU G B,FENG J T,XIANG X,WANG J B,SALOJÄRVI J,LIU C M,WU Z X,ZHANG J S,LIANG X M,JIANG Z D,LIU W,OU L X,LI J W,FAN G Y,MAI Y X,CHEN C J,ZHANG X T,ZHENG J K,ZHANG Y Q,PENG H X,YAO L X,WAI C M,LUO X P,FU J X,TANG H B,LAN T Y,LAI B,SUN J H,WEI Y Z,LI H L,CHEN J Z,HUANG X M,YAN Q,LIU X,MCHALE L K,ROLLING W,GUYOT R,SANKOFF D,ZHENG C F,ALBERT V A,MING R,CHEN H B,XIA R,LI J G. Two divergent haplotypes from a highly heterozygous lychee genome suggest independent domestication events for early and late-maturing cultivars[J]. Nature Genetics,2022,54(1):73-83.
[5] 陈厚彬,苏钻贤,杨胜男. 2023 年全国荔枝生产调查与形势分析[J]. 中国热带农业,2023(3):13-22.CHEN Houbin,SU Zuanxian,YANG Shengnan. Investigation and analysis of the litchi production in China in 2023[J]. China Tropical Agriculture,2023(3):13-22.
[6] 孔志强,张猛,秋卓君. 疏蕾、疏花、疏果对费约果品质的影响[J]. 中国南方果树,2021,50(3):87-90.KONG Zhiqiang,ZHANG Meng,QIU Zhuojun. Effects of flower bud thinning,flower thinning,and fruit thinning on the quality of Feijoa fruit[J]. South China Fruits,2021,50(3):87-90.
[7] 王功银,田贞环,方秉高,杨帮贵,覃伟. 椪柑多轮疏果技术及其经济效益[J]. 中国南方果树,2013,42(4):110.WANG Gongyin,TIAN Zhenhuan,FANG Binggao,YANG Banggui,QIN Wei. Multiple thinning techniques for ponkan mandarins and their economic benefits[J]. South China Fruits,2013,42(4):110.
[8] STERN R A,FLAISHMAN M,BEN-ARIE R. Effect of synthetic auxins on fruit size of five cultivars of Japanese plum (Prunus salicina Lindl.)[J]. Scientia Horticulturae,2007,112(3):304-309.
[9] CRONJE R B,MOSTERT P G. Evaluation of maxim® (3,5,6-tpa) for increase in yield,fruit size and retention in litchi,cv.HLH Mauritius,in South Africa[J]. Acta Horticulturae,2010,863:425-432.
[10] 齐文娥,陈厚彬,李伟文,张浩军. 中国荔枝产业发展现状、趋势与建议[J]. 广东农业科学,2016,43(6):173-179.QI Wen’e,CHEN Houbin,LI Weiwen,ZHANG Haojun. Development situation,trend and suggestions of Chinese litchi industry[J]. Guangdong Agricultural Sciences,2016,43(6):173-179.
[11] AGUSTÍ M,ZARAGOZA S,IGLESIAS D J,ALMELA V,PRIMO-MILLO E,TALÓN M. The synthetic auxin 3,5,6-TPA stimulates carbohydrate accumulation and growth in citrus fruit[J].Plant Growth Regulation,2002,36(2):141-147.
[12] YILDIRM B,YEŞİLOĞLU T,KAMILOĞLU M U,İNCESU M. Effects of 3,5,6-trichloro-2-pyridyloxyacetic acid on fruit size and yield of Valencia oranges (Citrus sinensis Osb.)[J]. Journal of Food Agriculture and Environment,2011,9(1):275-279.
[13] STERN R A,FLAISHMAN M,APPLEBAUM S,BEN-ARIE R. Effect of synthetic auxins on fruit development of ‘Bing’cherry (Prunus avium L.)[J]. Scientia Horticulturae,2007,114(4):275-280.
[14] YESILOGLU T,KOÇ S,ÇIMEN B. The usage of auxins with various cultural techniques to increase fruit size in Star Ruby grapefruit[J]. Fresenius Environmental Bulletin,2017,26(10):5717-5722.
[15] 邓嘉辉. 隔年交替结果技术和3,5,6-TPA 在‘仙进奉’荔枝上的应用研究[D]. 广州:华南农业大学,2021.DENG Jiahui. The application of alternate bearing technology and 3,5,6-TPA on ‘Xianjinfeng’ litchi[D]. Guangzhou:South China Agricultural University,2021.
[16] 李芳,刘耀婷,王祥和,李焕苓,王果,王家保. 两个荔枝品种的果实生长发育动态观察[J]. 热带农业科学,2021,41(10):27-33.LI Fang,LIU Yaoting,WANG Xianghe,LI Huanling,WANG Guo,WANG Jiabao. Dynamic analysis of fruit growth and development of two litchi varieties[J]. Chinese Journal of Tropical Agriculture,2021,41(10):27-33.
[17] 龙淑珍,何永群. 荔枝可滴定酸与维生素C 的测定及其相关性[J]. 广西农业科学,2002(4):188-189.LONG Shuzhen,HE Yongqun. Determination of titratable acids and vitamin C in lychee and their correlation[J]. Guangxi Agricultural Sciences,2002(4):188-189.
[18] 王利群,戴雄泽. 色差计在辣椒果实色泽变化检测中的应用[J].辣椒杂志,2009,7(3):23-26.WANG Liqun,DAI Xiongze. Application of colorimeter for testing its color change during the development of hot pepper (Capsicum annuum L.) fruit[J]. Journal of China Capsicum,2009,7(3):23-26.
[19] 胡志群,王惠聪,胡桂兵. 高效液相色谱测定荔枝果肉中的糖、酸和维生素C[J]. 果树学报,2005,22(5):582-585.HU Zhiqun,WANG Huicong,HU Guibing. Measurement of sugars,organic acids and vitamin C in litchi fruit by high performance liquid chromatography[J]. Journal of Fruit Science,2005,22(5):582-585.
[20] 王惠聪,黄辉白,黄旭明. 荔枝果实的糖积累与相关酶活性[J].园艺学报,2003,30(1):1-5.WANG Huicong,HUANG Huibai,HUANG Xuming. Sugar accumulation and related enzyme activities in the litchi fruit of‘Nuomici’ and ‘Feizixiao’[J]. Acta Horticulturae Sinica,2003,30(1):1-5.
[21] LOWELL C A,TOMLINSON P T,KOCH K E. Sucrose-metabolizing enzymes in transport tissues and adjacent sink structures in developing citrus fruit[J]. Plant Physiology,1989,90(4):1394-1402.
[22] 赵智中,张上隆,徐昌杰,陈昆松,刘拴桃. 蔗糖代谢相关酶在温州蜜柑果实糖积累中的作用[J]. 园艺学报,2001,28(2):112-118.ZHAO Zhizhong,ZHANG Shanglong,XU Changjie,CHEN Kunsong,LIU Shuantao. Roles of sucrose- metabolizing enzymes in accumulation of sugars in Satsuma mandarin fruit[J].Acta Horticulturae Sinica,2001,28(2):112-118.
[23] 徐婧,王丹,陈庆欣,张艳青,王俊,赵明磊,李建国. 超高效液相色谱-三重四级杆质谱联用法同时定量荔枝果实组织中IAA 和ABA[J]. 中国南方果树,2022,51(1):59-66.XU Jing,WANG Dan,CHEN Qingxin,ZHANG Yanqing,WANG Jun,ZHAO Minglei,LI Jianguo. Simultaneous quantification of indole-3-aceticacid and abscisic acid in litchi fruit tissues by ultra-high performance liquid chromatography-tandem mass spectrometry[J]. South China Fruits,2022,51(1):59-66.
[24] CRONJE R B,MOSTERT P G. Evaluation of maxim® (3,5,6-TPA) for increase in yield,fruit size and retention in litchi,cv.HLH Mauritius,in South Africa[C]. The Third International Symposium on Longan, Lychee,and other Fruit Trees in Sapindaceae Family. Guangdong,China:International Society for Horticultural Science,2008.
[25] GUELFAT-REICH S,BEN-ARIE R. Maturation and ripening of‘Canino’ apricot as affected by combined sprays of succinic acid 2,2-dimethylhydrazide (SADH) and 2,4,5-trichlorophenoxypropionic acid (2,4,5-TP)[J]. Journal of the American Society for Horticultural Science,1975,100(5):517-519.
[26] STERN R A,STERN D,MILLER H,XU H F,GAZIT S. The effect of the synthetic auxins 2,4,5-TP and 3,5,6-TPA on yield and fruit size of young ‘Feizixiao’ and ‘Heiye’ litchi trees in Guangxi province,China[J]. Acta Horticulturae,2001(558):285-288.
[27] 李建国,黄旭明,黄辉白. NAA 增大荔枝果实及原因分析[J].华南农业大学学报(自然科学版),2004,25(2):10-12.LI Jianguo,HUANG Xuming,HUANG Huibai. NAA sprays increased litchi fruit size and its roles[J]. Journal of South China Agricultural University (Natural Science Edition),2004,25(2):10-12.
[28] ZEMAN S,CMELIK Z,JEMRIĆ T. Size and weight of sweet cherry (Prunus avium L. ‘Regina’) fruit treated with 3,5,6-TPA and GA3[J]. Agriculturae Conspectus Scientificus,2012,77(1):45-47.
[29] 李卫东. 桃库源关系中源叶光合作用及其碳水化合物代谢的研究[D]. 北京:中国农业大学,2005.LI Weidong. Photosynthesis and carbohydrate metabolism in source leaves in response to sink-source manipulations in peach[Prunus persica (L.) Batsch.][D]. Beijing:China Agricultural University,2005.
[30] ORTOLÀ A G,MONERRI C,GUARDIOLA J L. Fruitlet age and inflorescence characteristics affect the thinning and the increase in fruitlet growth rate induced by auxin applications in citrus[J]. Acta Horticulturae,1998(463):501-508.
[31] 沙建川,贾志航,张鑫,吴晓娴,葛顺峰,姜远茂. 外源脱落酸对富士苹果果实膨大后期光合产物向果实运输的影响[J]. 应用生态学报,2019,30(6):1854-1860.SHA Jianchuan,JIA Zhihang,ZHANG Xin,WU Xiaoxian,GE Shunfeng,JIANG Yuanmao. Effects of exogenous ABA on translocation of photosynthate to fruit of Fuji apple during late stage of fruit rapid-swelling[J]. Chinese Journal of Applied Ecology,2019,30(6):1854-1860.
[32] COWAN A K,CRIPPS R F,RICHINGS E W,TAYLOR N J.Fruit size:Towards an understanding of the metabolic control of fruit growth using avocado as a model system[J]. Physiologia Plantarum,2001,111(2):127-136.
[33] 许让伟. 砂梨果实和叶片中糖积累及代谢相关酶活性变化研究[D]. 武汉:华中农业大学,2009.XU Rangwei. Studies on changes of sugar accumulation and related enzymes activities in sand pear fruits and leaves[D]. Wuhan:Huazhong Agricultural University,2009.
[34] 陈俊伟,张良诚,张上隆. 果实中的糖分积累机理[J]. 植物生理学通讯,2000,36(6):497-503.CHEN Junwei,ZHANG Liangcheng,ZHANG Shanglong. Sugar accumulation mechanism in fruits[J]. Plant Physiology Communications,2000,36(6):497-503.
[35] LI M J,FENG F J,CHENG L L. Expression patterns of genes involved in sugar metabolism and accumulation during apple fruit development[J]. PLoS One,2012,7(3):e33055.
[36] WOODWARD A W,BARTEL B. Auxin:Regulation,action,and interaction[J]. Annals of Botany,2005,95(5):707-735.
[37] OZGA J A,VAN HUIZEN R,REINECKE D M. Hormone and seed-specific regulation of pea fruit growth[J]. Plant Physiology,2002,128(4):1379-1389.
[38] MCATEE P,KARIM S,SCHAFFER R,DAVID K. A dynamic interplay between phytohormones is required for fruit development,maturation,and ripening[J]. Frontiers in Plant Science,2013,4:79.
[39] IRELAND H S,YAO J L,TOMES S,SUTHERLAND P W,NIEUWENHUIZEN N,GUNASEELAN K,WINZ R A,DAVID K M,SCHAFFER R J. Apple SEPALLATA1/2-like genes control fruit flesh development and ripening[J]. The Plant Journal,2013,73(6):1044-1056.
[40] SUN L,ZHANG M,REN J,QI J X,ZHANG G J,LENG P. Reciprocity between abscisic acid and ethylene at the onset of berry ripening and after harvest[J]. BMC Plant Biology,2010,10:257.
[41] 胡冰. ABA 调控荔枝果皮叶绿素降解和花色苷生物合成的分子机理研究[D]. 广州:华南农业大学,2018.HU Bing. Study on the molecular mechanism of ABA in regulating chlorophyll degradation and anthocyanin biosynthesis in pericarp of Litchi chinensis[D]. Guangzhou:South China Agricultural University,2018.
[42] 李翠,侯柄竹. 脱落酸调控果实成熟的分子及信号转导机制研究进展[J]. 果树学报,2023,40(5):988-999.LI Cui,HOU Bingzhu. Molecular mechanism of abscisic acid in regulating fruit ripening[J]. Journal of Fruit Science,2023,40(5):988-999.
[43] JIANG Y M,JOYCE D C. ABA effects on ethylene production,PAL activity,anthocyanin and phenolic contents of strawberry fruit[J]. Plant Growth Regulation,2003,39(2):171-174.
[44] KOYAMA K,SADAMATSU K,GOTO-YAMAMOTO N. Abscisic acid stimulated ripening and gene expression in berry skins of the Cabernet Sauvignon grape[J]. Functional & Integrative Genomics,2010,10(3):367-381.
[45] HU B,LAI B,WANG D,LI J Q,CHEN L H,QIN Y Q,WANG H C,QIN Y H,HU G B,ZHAO J T. Three LcABFs are involved in the regulation of chlorophyll degradation and anthocyanin biosynthesis during fruit ripening in Litchi chinensis[J].Plant & Cell Physiology,2019,60(2):448-461.