猕猴桃隶属猕猴桃科(Actinidiaceae)猕猴桃属(Actinidia Lindl),是我国重要的木质藤本果树[1]。因其果实风味独特、富含维生素C 而深受消费者喜爱,素有“维C之王”的称号[2]。我国猕猴桃产业经历40 余年的发展,已成为世界上猕猴桃产量和种植面积最大的国家[3],截至2024年,猕猴桃栽培面积和年产量已达30 万hm2和434.6 万t,在我国县域经济发展、农民脱贫致富、乡村经济振兴中发挥了重要作用[4]。猕猴桃细菌性溃疡病由丁香假单胞杆菌猕猴桃致病变种(Pseudomonas syringae pv. actinidiae,Psa)引起,是全球猕猴桃产业的毁灭性病害。在我国陕西、贵州等主产区病株率高达30%,严重威胁猕猴桃产业的可持续发展[5]。我国拥有丰富的猕猴桃种质资源,挖掘抗性优异的种质资源,揭示抗性形成的内在机制,培育创制抗病品种,是解决溃疡病发生的重要途径[6]。
植物在生长和繁殖过程中经常遭受各种生物和非生物因素的干扰,其体内的代谢物不断变化,因此代谢物的变化承载着代谢水平、基因表达和蛋白质功能方面的丰富信息[7]。近年来,代谢组学作为一种重要的生物技术方法已在植物科学研究中得到广泛应用[8-10],不仅能够客观准确地评价不同样品间的均一性,还能筛选不同样品间的成分差异,同时对未知样本进行归属判别,在定向育种、品种鉴定和品质评价等方面发挥重要作用[11]。通过研究代谢所产生的差异代谢物,揭示其参与的生命活动机制,已成为研究植物抗病机制的重要手段。通过代谢组分析比对不同抗性品种在病原菌侵染下各种差异代谢物的含量变化,筛选与抗性相关的代谢物,同时结合遗传学揭示植物与病菌之间的分子互作机制。番茄抗感品种响应斑萎病侵染过程主要涉及94 种差异代谢物,其中大部分属于类黄酮,表明类黄酮合成途径可能与番茄植株的斑萎病抗病机制密切相关[12]。在十字花科植物中,Li 等[13]发现感病萝卜品种比抗病品种含有更多的差异代谢物,进一步通过体外抗菌试验,证实喷施5 mg·L-1的人参皂苷 Rg1 及6-姜酚可有效降低发病率和病情指数,且能促进幼苗生长。Xiao 等[14]在茄子抗青枯病品种的代谢组中鉴定到63 种差异代谢物,进一步分析证实植物激素在对抗青枯病过程中发挥重要作用。Reymick 等[15]通过代谢组学分析,发现茉莉酸(JA)生物合成和信号转导及苯丙烷类生物合成基因参与了柠檬醛诱导柑橘果实抗青霉病的过程。Liu 等[16]在抗感甜橙品种中鉴定到13 种对柑橘溃疡病菌具有显著抑制作用的代谢产物,其中瑞香素和七叶亭抑菌效果超过60%。由此证实代谢组技术已广泛应用于植物抗病机制研究。
鉴于此,笔者以国家猕猴桃资源圃多年构建及保存的山梨及中华猕猴桃杂交群体为材料,基于高效液相色谱-串联质谱法(LCMS/MS),通过非靶向代谢组学技术对溃疡病不同感染时间的抗病种质E2545 和感病种质E674 进行代谢物定性定量分析,筛选与抗性相关的差异代谢物,并解析差异代谢物参与植物抗病的代谢途径,旨在阐明猕猴桃种质的溃疡病抗病机制,以期为研发新型生防药剂奠定理论基础。
1 材料和方法
1.1 材料
山梨猕猴桃与中华猕猴桃种间杂交种质均保存于中国科学院武汉植物园国家猕猴桃种质资源圃(武汉)中,均为2 倍体,树龄6 a(年),树势生长良好。分别于2022 年和2023 年对山梨与中华猕猴桃杂交种质群体进行离体枝条接种,以评价群体抗性[17]。综合两年的枝条鉴定结果,筛选出抗病种质E2545 和感病种质E674 作为本研究材料,接种Psa病菌后,两者枝条病斑长度分别为(4.99±0.65) mm和(10.45±0.22) mm。
供试菌株M228 为猕猴桃溃疡病病原菌丁香假单胞菌猕猴桃致病变种Pseudomonas syringae pv.actinidiae(Psa),由西北农林科技大学果树病害病原生物学及综合防治研究团队提供[18],保存于中国科学院武汉植物园植物种质创新与特色农业重点实验室。
1.2 方法
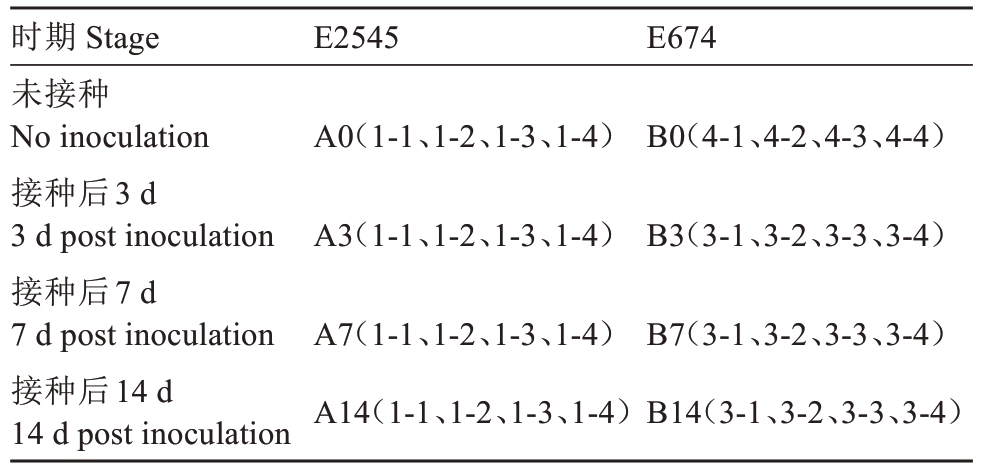
1.2.1 代谢组材料采集 2024 年11 月落叶后,采集当年生猕猴桃健康枝条,选取直径约为0.8 cm 且长势一致的枝条,截成12~14 cm 的短枝后,尽快用石蜡密封枝条两端,防止水分流失。参照朱佳慧等[19]的方法活化病菌,配置OD600=1.0 的菌悬液(浓度为109 CFU·mL-1)。使用打孔器在枝条上制造3 mm宽、深至木质部的伤口,接种菌液,以无菌水处理作为阴性对照。代谢组样本取样时间为未接种、接种后3 d、7 d、14 d四个时间点,取样部位参照秦红艳[20]的方法,剪取以病菌接种点为中心的上下各1 cm 处的枝条木质化组织0.3 g。每个时间点设置4 次重复,共32 个样品(表1)。代谢组检测由青岛百谱生物科技有限公司完成。
表1 代谢组检测样品
Table 1 Metabolome detected samples
时期 Stage未接种No inoculation接种后3 d 3 d post inoculation接种后7 d 7 d post inoculation接种后14 d 14 d post inoculation E2545 E674 A0(1-1、1-2、1-3、1-4)B0(4-1、4-2、4-3、4-4)A3(1-1、1-2、1-3、1-4)B3(3-1、3-2、3-3、3-4)A7(1-1、1-2、1-3、1-4)A14(1-1、1-2、1-3、1-4)B7(3-1、3-2、3-3、3-4)B14(3-1、3-2、3-3、3-4)
1.2.2 代谢物提取 参考Wang 等[21]的操作方法提取代谢物:称取50 mg猕猴桃枝条样本,加入1000 µL内标提取液(甲醇、乙腈、水体积比为2∶2∶1),混匀后加入钢珠研磨10 min,冰水浴超声处理10 min,20 ℃静置1 h。4 ℃、12 000 r·min-1离心15 min,取500 µL上清液于真空浓缩器中干燥。在干燥后的代谢物中加入160 μL 提取液(乙腈、水体积比为1∶1)复溶,涡旋30 s,冰水浴超声10 min,4 ℃、12 000 r·min-1离心15 min,取上清液待测。
1.2.3 仪器设备 液质联用系统由沃特世Acquity IClass PLUS 超高效液相串联沃特世Xevo G2XS QTof高分辨质谱仪组成,所使用色谱柱为购自沃特世的Acquity UPLC HSS T3 色谱柱(1.8 μm,2.1 m×100 mm)。质谱条件:在采集软件(MassLynx V4.2,Waters)控制下的MSe模式进行一级、二级质谱数据采集。在每个数据采集循环中,同时对低碰撞能量及高碰撞能量进行双通道数据采集。低碰撞能量为2 V,高碰撞能量区间为10~40 V,质谱图扫描频率为每0.2 s一张。ESI离子源参数如下:毛细管电压2000 V(正离子模式)或1500 V(负离子模式);锥孔电压30 V;离子源温度150 ℃;脱溶剂气温度500 ℃;反吹气流速50 L·h-1;脱溶剂气流速800 L·h-1。
1.2.4 数据统计 利用MassLynx V4.2 采集代谢物原始数据,运用Progenesis QI 软件对数据进行峰提取、峰对齐等处理。基于百迈克生物科技有限公司构建数据库BMK (biomarker database),根据二级谱信息进行物质定性分析,利用三重四级杆质谱的多反应监测模式进行定量分析。差异代谢物筛选阈值为变量权重值(variable importance in projection,VIP)≥1、P-value<0.05、差异倍数(fold change,FC),经log2转化,log2|FC|≥1。
2 结果与分析
2.1 QC样本质控结果
为保证色谱质谱分析的可靠性,每个样品中取等体积混匀作为 QC样本(quality control,QC),考察QC 样本间的相关性。根据代谢物的相对定量值计算 QC 样本间的皮尔逊相关系数(r)。相关系数越接近1,QC 样本间相关性越高,表明整个检测过程仪器稳定性越好,数据质量越高。
本试验QC 样本相关性如图1 所示,QC 样本在正离子模式下相关性分布在0.988 4~0.996 4 之间,负离子模式下相关性分布在0.994 1~0.997 7 之间,均表现出高相关性,证实本研究数据质量可靠。
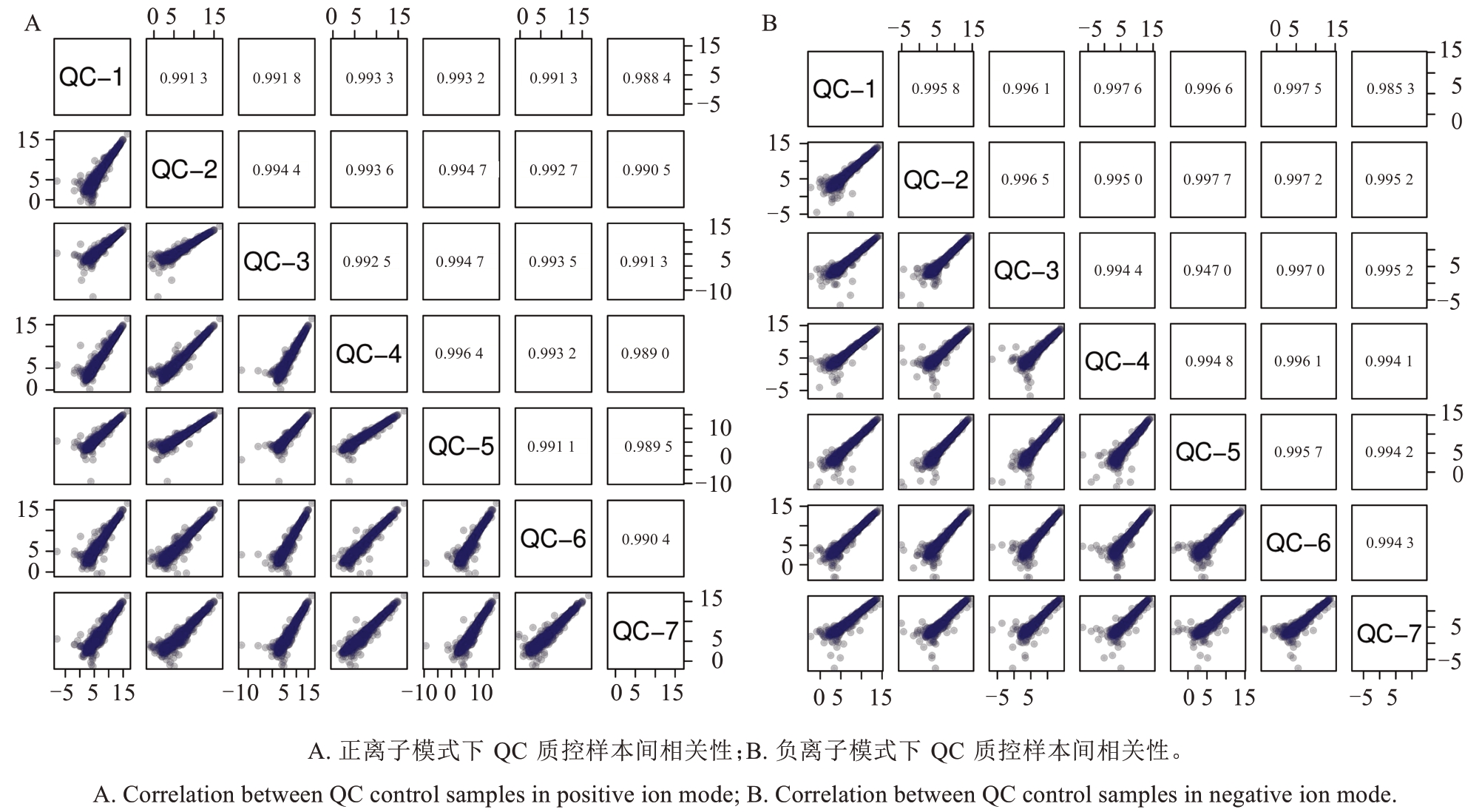
图1 QC 质控样本间相关性
Fig. 1 Correlation between QC control samples
2.2 样本间PCA和OPLS-DA结果
PCA 主成分分析是一种无监督模式识别的多维数据统计分析方法,反映代谢组数据的原始情况。PCA 分析结果以散点图形式展示各代谢组之间的分离趋势,以此表明各样品组间代谢物的差异。本研究PCA 结果如图2 所示,2 个主成分的累计贡献率达39.4%,当PC1=23.6%、PC2=15.8%时,8组样品间的分离趋势较为明显,反映出样品间代谢组数据存在差异,且重复样本聚在一起,表明重复样本间的相似性较高,可用于后续分析。进一步分析发现,除B14 组外,抗病组和感病组样本分离明显,表明抗病种质和感病种质的代谢群存在显著差异,与预期结果一致。此外,未接种抗病种质样本A0大部分分布在PC1 左半部分,接种后抗病种质A 组样本均分布在PC1 右半部分;与未接种感病种质样本B0 相比,接种后感病种质B 组样本在PC1 上向右发生偏移。由此表明,在溃疡病病原菌侵染下,猕猴桃抗感种质中的代谢物均发生了变化。
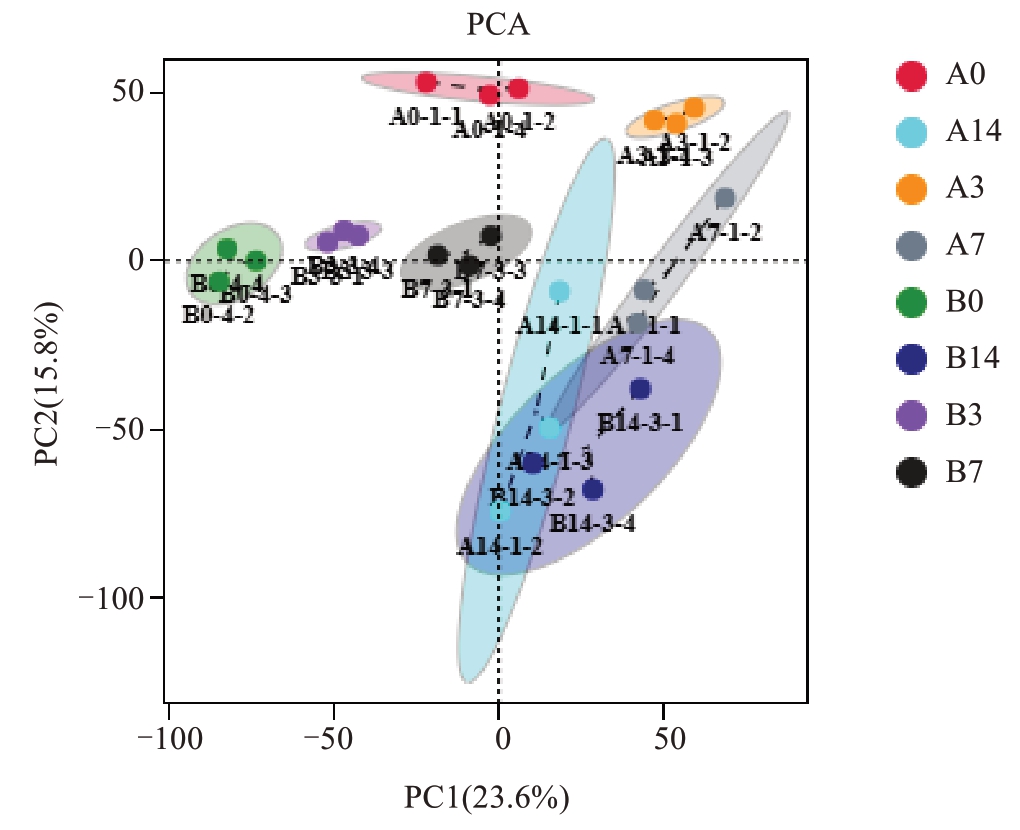
图2 样本PCA 主成分分析
Fig. 2 Sample PCA principal component analysis
由于代谢组数据检测的代谢物种类较多,且很多代谢物具有多重共线性趋势,因此对于一些相关性较小的差异变量,需要使用偏最小二乘判别分析(orthogonal projections to latent structures- discriminant analysis,OPLS-DA)进行判断。OPLS-DA 预测模型评价参数中的R2Y 和Q2Y 越接近于1,表示模型越稳定可靠。因此,可用此模型筛选差异代谢物。Q2Y>0.5 时认为是有效的模型,Q2Y>0.9 时为出色的模型。
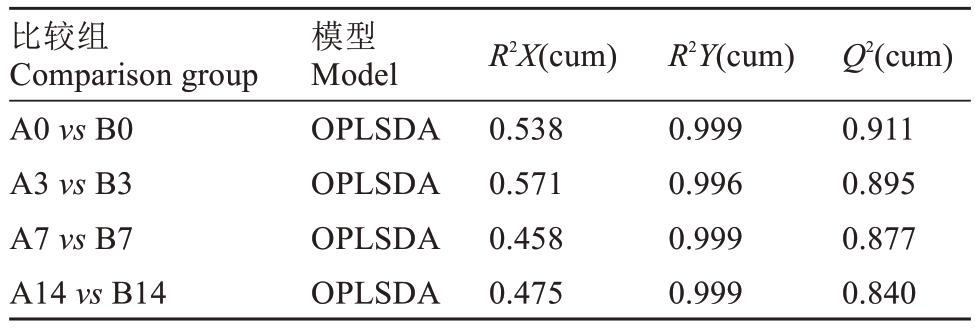
由表2 可知,不同组间OPLS-DA 相关模型的R2Y(cum)和Q2(cum)范围分别为0.996~0.999 和0.840~0.911 之间,R2Y、Q2值均大于0.5,表明该模型稳定可靠。猕猴桃溃疡病侵染抗感种质第3 天、7天、14 天后的代谢组数据(处理组和对照组之间)存在统计学显著差异。
表2 OPLS-DA 模型参数
Table 2 Statistics of OPLSDA analysis
比较组Comparison group A0 vs B0 A3 vs B3 A7 vs B7 A14 vs B14模型Model OPLSDA OPLSDA OPLSDA OPLSDA R2X(cum)0.538 0.571 0.458 0.475 R2Y(cum)0.999 0.996 0.999 0.999 Q2(cum)0.911 0.895 0.877 0.840
2.3 不同接种时间抗感种质间差异代谢物
设置不同分组,对抗病(A)、感病(B)材料不同时期样本进行差异代谢物分析(图3)。通过非靶向代谢组学分析方法共检测到代谢物5886 种,进一步对代谢物进行分类,结果显示这些代谢物主要为有机氧化合物(organic oxygen compounds)、异戊烯醇脂类(prenol lipids)、苯和取代衍生物(benzene and substituted derivatives)、脂肪酰基(fatty Acyls)、羧酸及其衍生物 (carboxylic acids and derivatives)、黄酮类化合物(flavonoids)、酚类化合物(phenols)、类固醇及其衍生物(steroids and their derivatives)、香豆素及其衍生物(coumarins and their derivatives)等。相较于感病种质,在抗病种质接种前(A0 vs B0)共鉴定到2179 种差异代谢物(其中971 种上调,1208种下调);接种后3 d(A3 vs B3)鉴定到1715 种差异代谢物(其中500 种上调,1215 种下调);接种后7 d(A7 vs B7)鉴定到1518 种差异代谢物(其中679 种上调,839 种下调);接种后14 d(A14 vs B14)鉴定到1345种差异代谢物(其中614种上调,731种下调)。
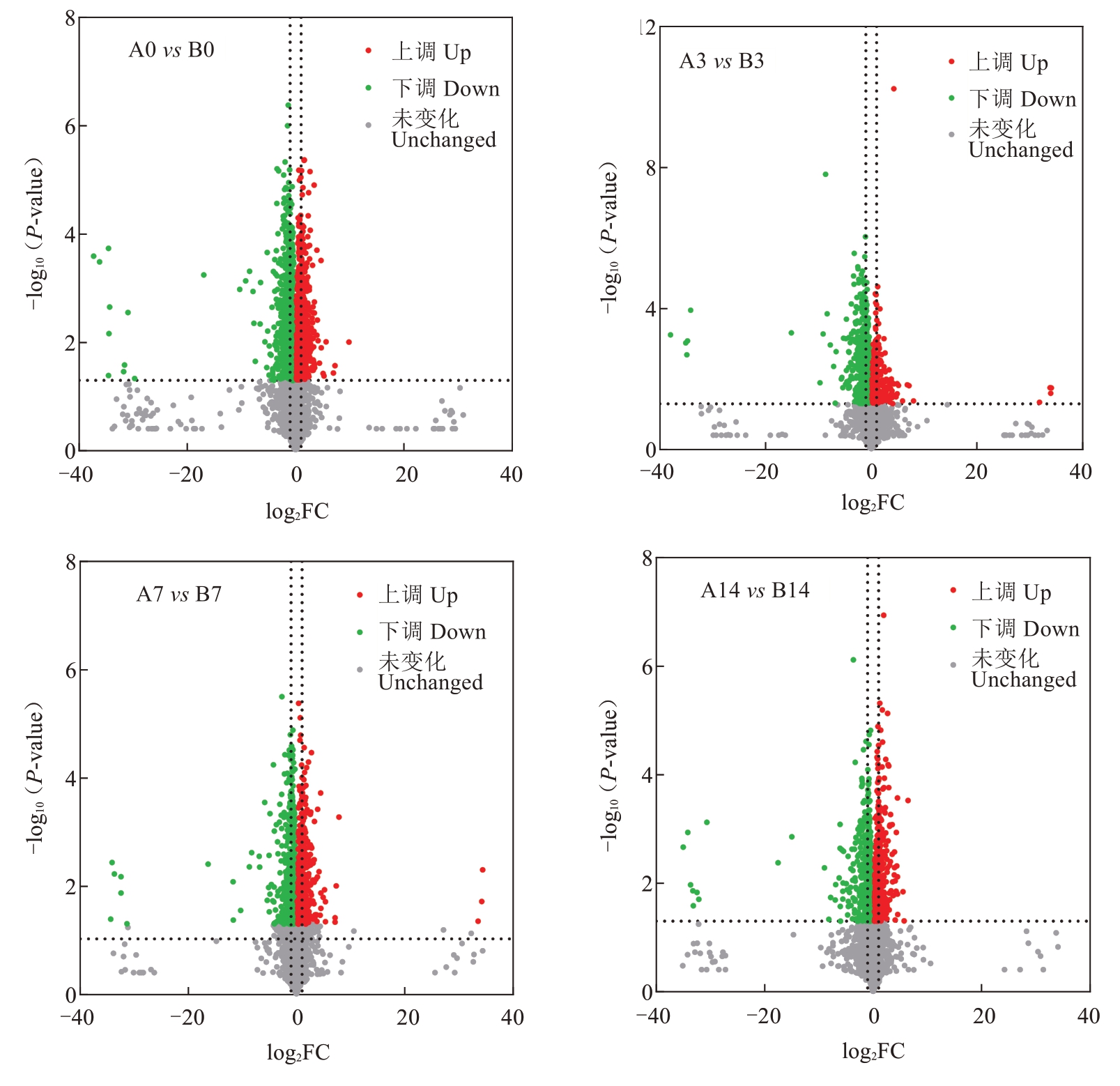
图3 抗感种质在不同溃疡病感染时间的差异代谢物火山图
Fig. 3 Volcano plots of differentially expressed metabolites in resistant and susceptible varieties at different times
2.4 不同接种时间抗感种质间共有差异代谢物
在接种溃疡病前后的4个时期,抗感种质有193种共有差异代谢物(图4),进一步对上述差异代谢物进行分类分析,结果显示这些差异代谢物主要包含苯和取代衍生物、香豆素及其衍生物、异戊烯醇脂类、羧酸及其衍生物等。
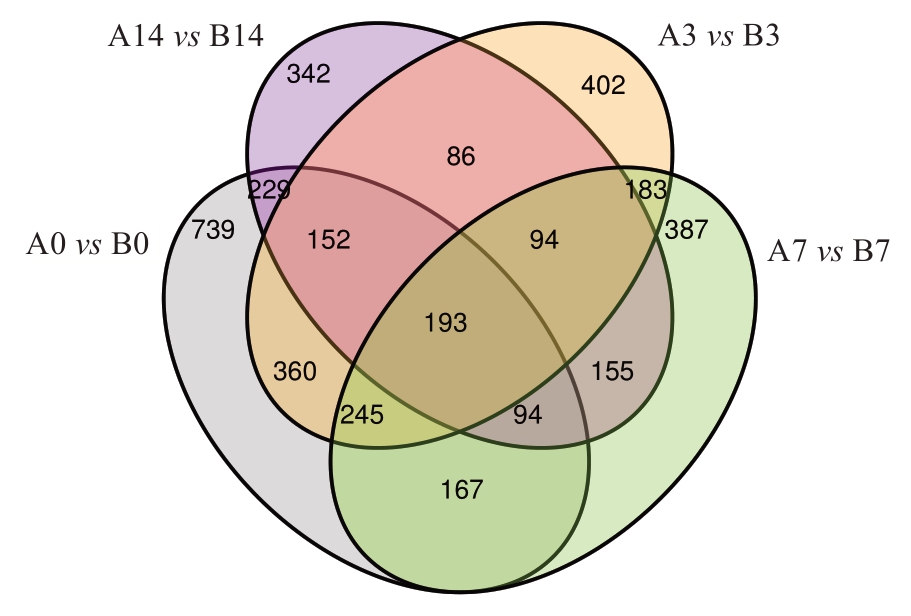
图4 抗感种质中差异代谢物数目
Fig. 4 The number of differential metabolites among resistant and susceptible germplasms
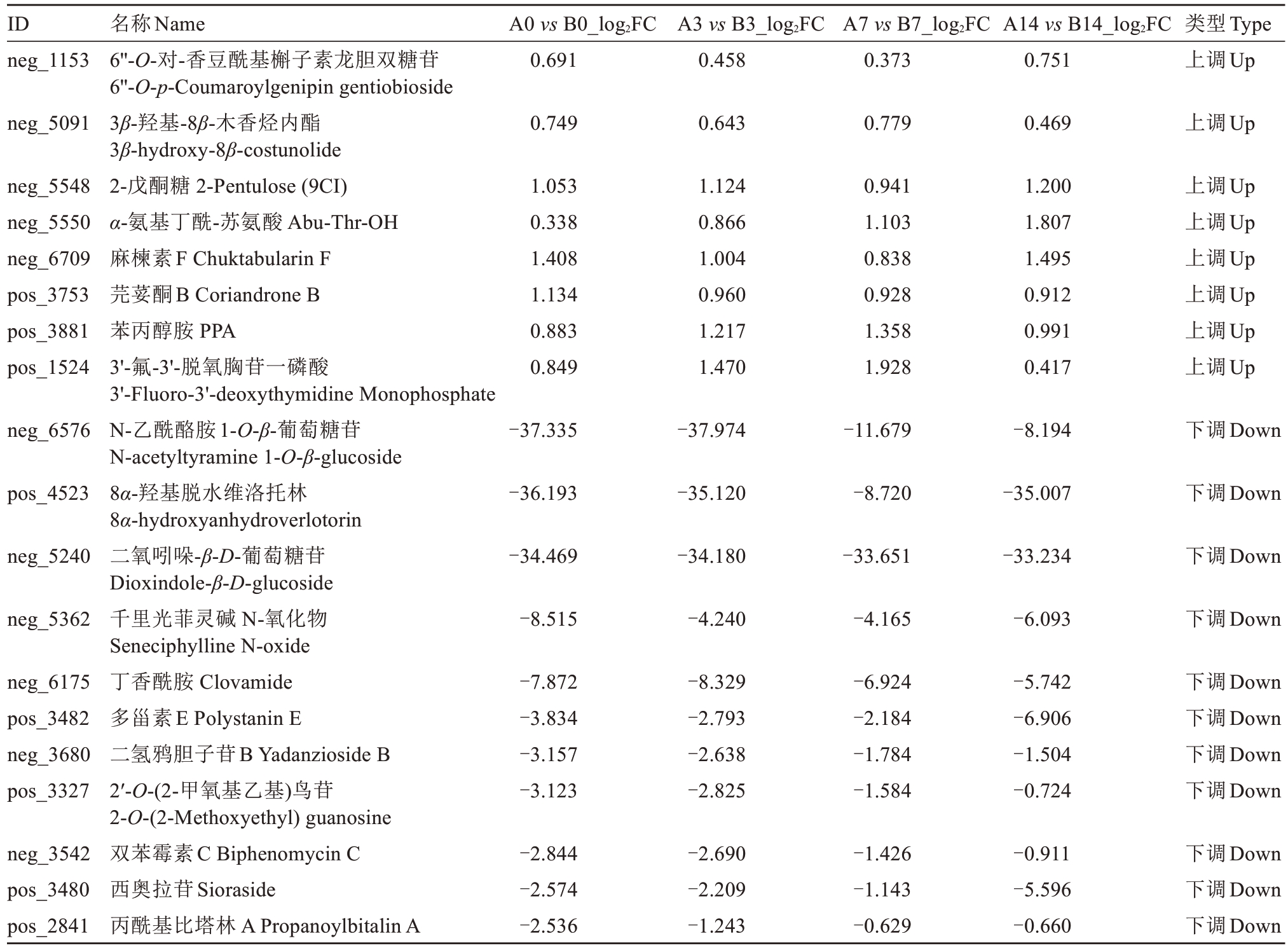
将各时期抗感种质间数据进行比对,发现17 种代谢物在抗病种质中的含量低于感病种质,表现为代谢物含量上调(部分数据如表3 所示),包括2-戊酮糖[2-pentulose (9CI)]、苯丙醇胺(PPA)、芫荽酮B(coriandrone B)、α-氨基丁酰-苏氨酸(Abu-Thr-OH)等。
表3 不同侵染时期猕猴桃抗感种质间部分差异代谢物种类
Table 3 Partial differential metabolite types in kiwifruit resistant/susceptible germplasms across infection periods
ID neg_1153 A0 vs B0_log2FC 0.691 A3 vs B3_log2FC 0.458 A7 vs B7_log2FC 0.373 A14 vs B14_log2FC 0.751类型Type上调Up neg_5091 0.749 0.643 0.779 0.469上调Up neg_5548 neg_5550 neg_6709 pos_3753 pos_3881 pos_1524 1.053 0.338 1.408 1.134 0.883 0.849 1.124 0.866 1.004 0.960 1.217 1.470 0.941 1.103 0.838 0.928 1.358 1.928 1.200 1.807 1.495 0.912 0.991 0.417上调Up上调Up上调Up上调Up上调Up上调Up neg_6576-37.335-37.974-11.679-8.194下调Down pos_4523-36.193-35.120-8.720-35.007下调Down neg_5240-34.469-34.180-33.651-33.234下调Down neg_5362-8.515-4.240-4.165-6.093下调Down neg_6175 pos_3482 neg_3680 pos_3327-7.872-3.834-3.157-3.123-8.329-2.793-2.638-2.825-6.924-2.184-1.784-1.584-5.742-6.906-1.504-0.724下调Down下调Down下调Down下调Down neg_3542 pos_3480 pos_2841名称Name 6''-O-对-香豆酰基槲子素龙胆双糖苷6''-O-p-Coumaroylgenipin gentiobioside 3β-羟基-8β-木香烃内酯3β-hydroxy-8β-costunolide 2-戊酮糖 2-Pentulose (9CI)α-氨基丁酰-苏氨酸 Abu-Thr-OH麻楝素F Chuktabularin F芫荽酮B Coriandrone B苯丙醇胺 PPA 3'-氟-3'-脱氧胸苷一磷酸3'-Fluoro-3'-deoxythymidine Monophosphate N-乙酰酪胺1-O-β-葡萄糖苷N-acetyltyramine 1-O-β-glucoside 8α-羟基脱水维洛托林8α-hydroxyanhydroverlotorin二氧吲哚-β-D-葡萄糖苷Dioxindole-β-D-glucoside千里光菲灵碱 N-氧化物Seneciphylline N-oxide丁香酰胺 Clovamide多甾素E Polystanin E二氢鸦胆子苷B Yadanzioside B 2′-O-(2-甲氧基乙基)鸟苷2-O-(2-Methoxyethyl) guanosine双苯霉素C Biphenomycin C西奥拉苷Sioraside丙酰基比塔林 A Propanoylbitalin A-2.844-2.574-2.536-2.690-2.209-1.243-1.426-1.143-0.629-0.911-5.596-0.660下调Down下调Down下调Down
在接种不同时期,87 种共有差异代谢物在抗病种质中的含量均高于感病种质,表现为下调(部分数据如表3 所示)。包括N-乙酰酪胺1-O-β-葡萄糖苷(N-acetyltyramine 1-O-beta-glucoside)、二氧吲哚-β-D-葡萄糖苷(dioxindole-beta-D-glucoside)、多甾素E(polystanin E)、乙酰水杨酸(aspirin)、乙酰胺素(acetylexidonin)、皂苷内酯C(saponaceolide C)、二氢鸦胆子苷B(yadanzioside B)、缬草三酯(valtratum)等。
综上所述,猕猴桃抗感种质在病菌侵染不同时期共有差异代谢物种类主要为苯和取代衍生物、香豆素及其衍生物、异戊烯醇脂类化合物、羧酸及其衍生物等。87 种共有差异代谢物在抗病种质中的含量始终高于感病种质,推测这些差异代谢物在猕猴桃防御溃疡病菌中发挥重要作用。
2.5 抗感种质间差异代谢物KEGG通路
差异代谢物KEGG 通路分析表明(图5),抗感种质间差异代谢物富集于苯丙烷类生物合成(phenylpropanoid biosynthesis)、卟啉代谢(porphyrin metabolism)、植物次生代谢产物生物合成(biosynthesis of various plant secondary metabolites)、ABC 转运蛋白(ABC transporters)、泛醌及其他萜类醌生物合成(ubiquinone and other terpenoid-quinone biosynthesis)、苯丙氨酸代谢(phenylalanine metabolism)、核黄素代谢(riboflavin metabolism)、半乳糖代谢(galactose metabolism)、酪氨酸代谢(tyrosime metabolism)、花青素生物合成(anthocyanin biosynthesis)等代谢通路,其中在苯丙烷类生物合成通路显著富集。进一步分析发现193 个共有差异代谢物显著富集于苯丙氨酸代谢(phenylalanine metabolism)、丁酸代谢(butanoate metabolism)、卟啉代谢(porphyrin metabolism)、苯丙烷类生物合成(phenylpropanoid biosynthesis)通路。
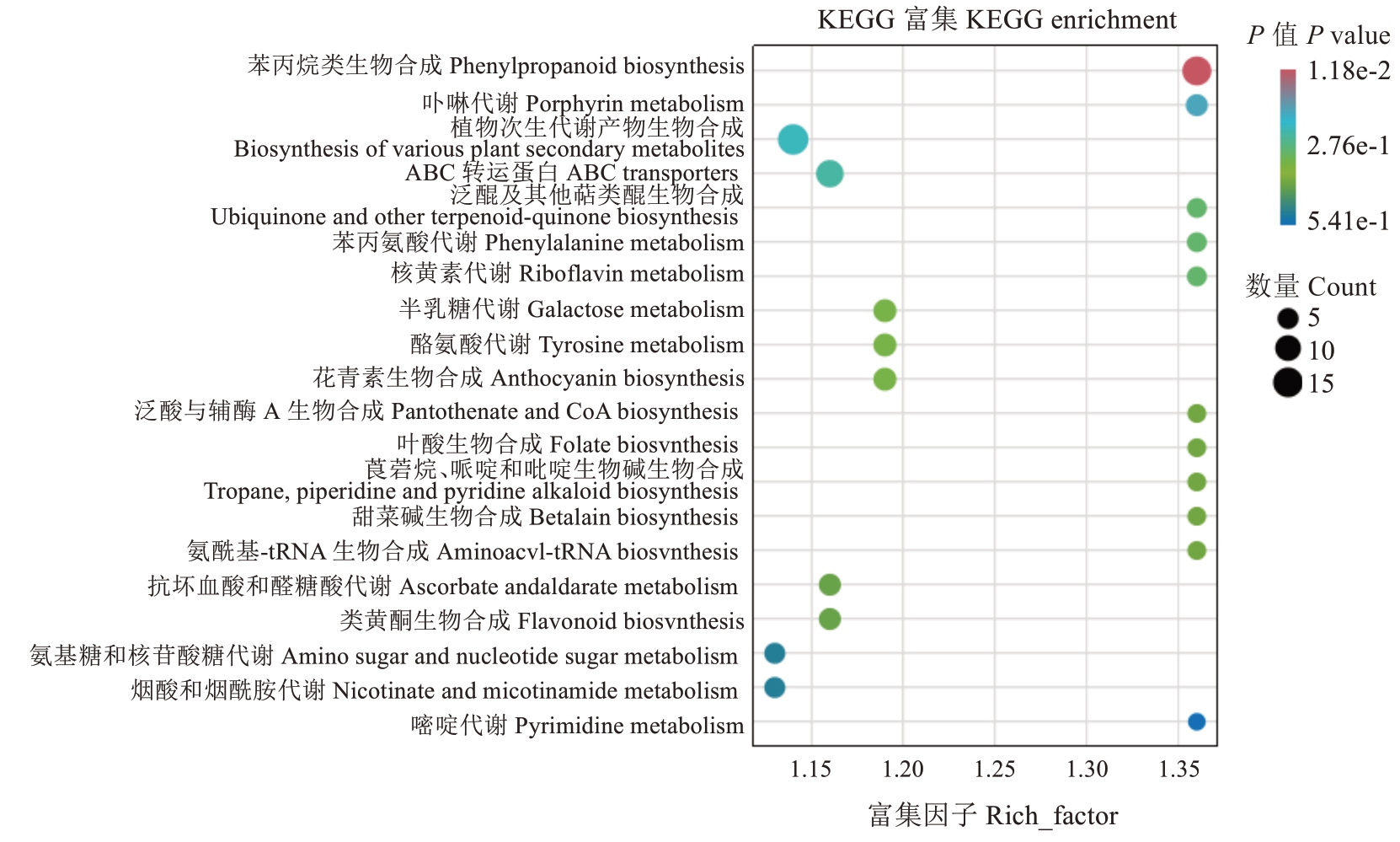
图5 抗感种质中差异代谢物KEGG 富集通路
Fig. 5 KEGG enrichment analysis of differential metabolites among resistant and susceptible germplasms
2.6 抗感品种间4种关键差异代谢物
研究发现,87 种共有差异代谢物中大多数是不同类型代谢物的衍生物,其中一些代谢物难以在市场上获得。为鉴定具有应用潜力的抗病防御相关代谢物,笔者基于代谢差异数据,筛选了4种极可能对溃疡病菌具有抑制作用且市售的典型化合物,对其含量变化及潜在功能进行了详细分析。
阿司匹林(aspirin)的主要成分是乙酰水杨酸(acetylsalicylic acid,ASA),是水杨酸(salicylic acid,SA)的衍生物。水杨酸是植物抗病信号通路的核心分子,尤其在生物营养型病原体(如真菌、细菌)的抗性机制中起关键作用。乙酰水杨酸可能通过影响植物体内水杨酸等激素的信号转导途径,进而调节植物的免疫反应。如图6 所示,接种前后抗病种质中阿司匹林含量始终高于感病种质,且随着侵染时间延长,抗病种质中阿司匹林含量逐渐升高。在第3天时,抗病种质中阿司匹林含量是感病种质的2.27倍;在第7天时,抗病种质中阿司匹林含量是感病种质的2.09 倍;在第14 天时,抗感种质间阿司匹林含量差异达到最大,差异倍数为2.65。与接种前相比,接种第14 天时,抗病种质与感病种质中阿司匹林含量分别提高了2.72倍和1.82倍。
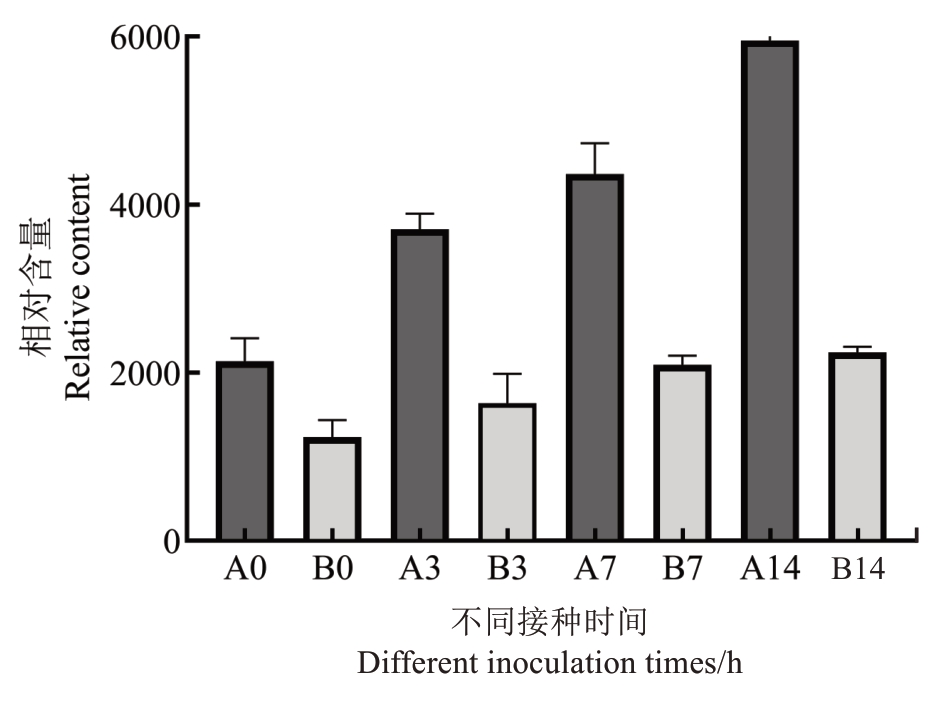
图6 不同抗性材料感染病原菌前后阿司匹林含量的变化
Fig. 6 Changes of aspirin content in different resistance materials before and after pathogen infection
甘草酸(liquoric acid)能诱导抗氧化酶产生,维持细胞内自由基氧化剂和抗氧化平衡环境,从而减轻植物在受到外界胁迫时产生的氧化损伤。如图7所示,接种溃疡病菌前,猕猴桃抗感种质中甘草酸含量较低,但随着侵染时间延长,甘草酸含量逐渐升高,且抗病种质中甘草酸含量增加趋势大于感病种质。在第3 天时,抗病种质中甘草酸含量是感病种质的1.56 倍;在第7 天时,抗感种质间甘草酸含量差异达到最大,抗病种质含量是感病种质的3.18倍;在第14 天时,抗病种质中甘草酸含量是感病种质的2.4 倍。与接种前相比,接种第14 天时,抗病种质与感病种质中甘草酸含量分别提高了55.20倍和26.80倍。
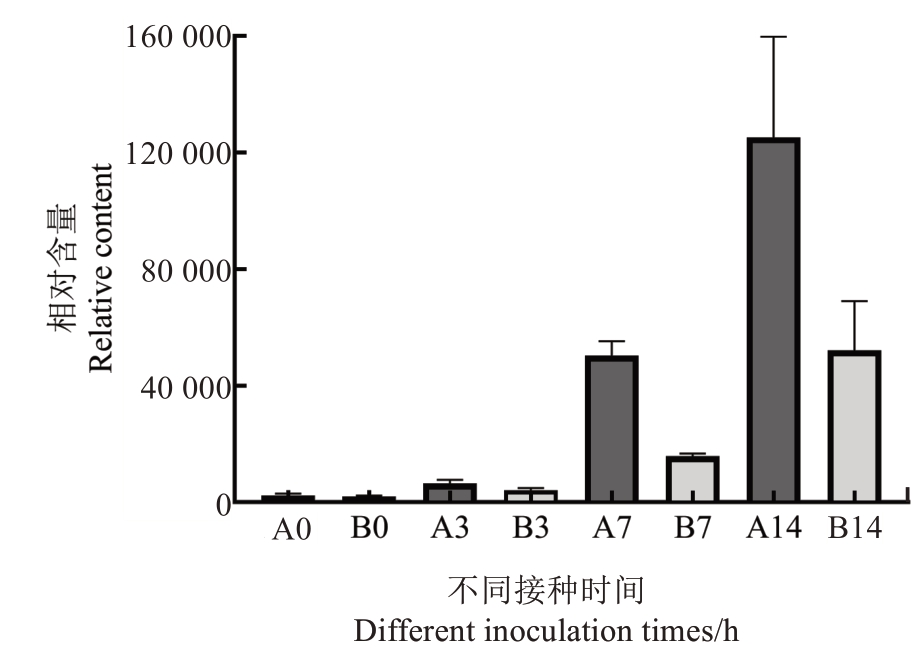
图7 不同抗性材料感染病原菌前后甘草酸含量的变化
Fig. 7 Changes of liquoric acid content in different resistance materials before and after pathogen infection
抗感种质间pestalactam B 的含量变化如图8 所示,抗病种质中pestalactam B 含量始终高于感病种质。接种前,抗病种质中pestalactam B 含量是感病种质的1.56 倍;在接种第3 天时,抗病种质中pestalactam B 是感病种质的2.65 倍,抗感种质间含量差异达到最大;在第7 天时,抗病种质中pestalactam B含量是感病种质的2.01 倍;在第14 天时,抗病种质中pestalactam B含量是感病种质的1.82倍。针对抗病种质,接种第3 天时pestalactam B 含量最高,是接种前的1.83 倍;而针对感病种质,pestalactam B 含量逐渐升高,在接种第14 天时达到最高,是接种前的1.23倍。
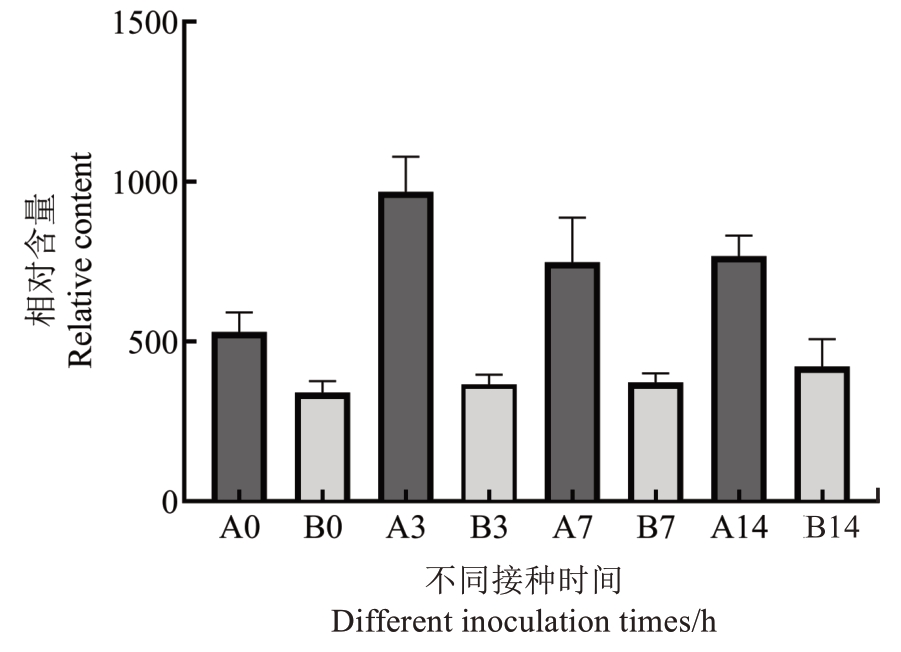
图8 不同抗性材料感染病原菌前后pestalactam B含量的变化
Fig. 8 Changes of pestalactam B content in different resistance materials before and after pathogen infection
缬草素(valtratum)在抗感种质间的含量变化如图9 所示,抗病种质中的缬草素含量始终高于感病种质。接种前,抗病种质中缬草素含量是感病种质的2.11 倍;在接种第3 天时,抗病种质中缬草素含量是感病种质的2.95 倍,抗感种质间含量差异达到最大;在第7 天时,抗病种质中缬草素含量是感病种质的1.86 倍;在第14 天时,抗病种质中缬草素含量是感病种质的2.25 倍。抗病种质中缬草素含量在第3天时最高,是接种前的1.67倍;感病种质中缬草素含量在第14天时达到最高,是接种前的1.31倍。
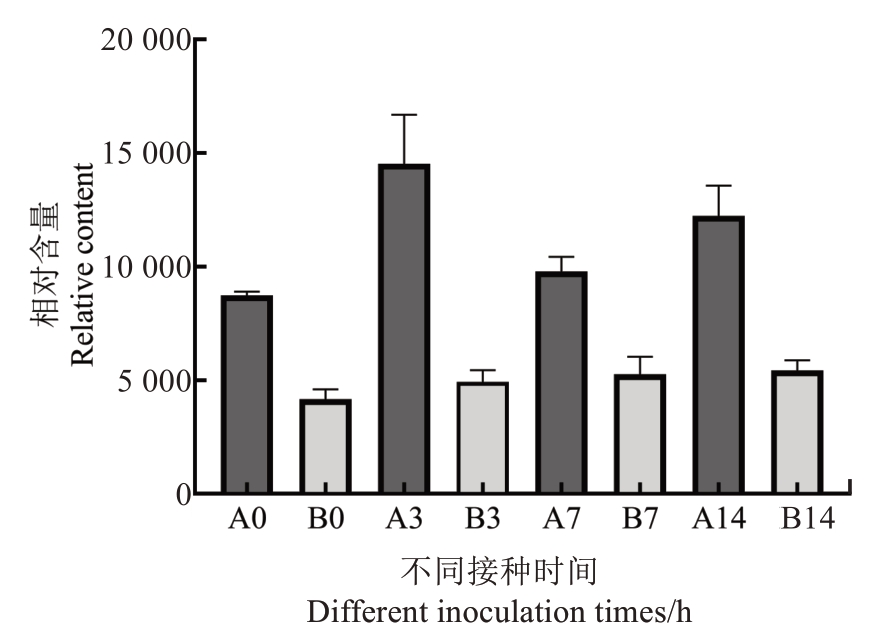
图9 不同抗性材料感染病原菌前后缬草素含量的变化
Fig. 9 Changes of valtratum content in different resistance materials before and after pathogen infection
3 讨 论
植物在长期进化过程中,为应对复杂的生物与非生物胁迫环境,形成了多层次的适应机制,如植物形态结构和生理变化、免疫系统的进化及具有缓压作用的次生代谢产物合成[22]。植物次生代谢产物因具有显著的化学结构多样性和广泛的生物活性特征,在抗逆过程中发挥着关键作用。当受到外界胁迫刺激时,植物以初级代谢产物为前体激活多元化的生物合成途径,特异性地诱导次生代谢产物的动态合成,形成针对不同胁迫类型的精准防御响应[23]。通过代谢组学分析,可快速阐明植物应对病原菌侵染阶段体内代谢物水平的变化情况[24]。本研究表明,猕猴桃感染溃疡病菌后抗感种质间差异代谢物种类主要为苯和取代衍生物、香豆素及其衍生物、异戊烯醇脂类化合物、羧酸及其衍生物等,与前期的多项研究结果一致。多项文献已证实香豆素类化合物具有高效抑菌作用,在离体条件下对多种病原菌具有抑菌活性[25-27]。本研究证实3 种香豆素衍生物(4-甲基伞形酮-β-D-葡糖苷酸、刺五加苷B1、6-甲基香豆素)含量在猕猴桃抗感种质间差异显著。其中,在张方贺等[28]研究中,6-甲基香豆素被证实对葡萄白腐病菌、柑橘炭疽病菌、棉花枯萎病菌、苹果腐烂病菌均存在一定的抑制作用。其他香豆素类衍生物,如蛇床子素也被证实对辣椒疫霉病菌、番茄灰霉病菌、小麦赤霉病菌等真菌具有显著的抑制作用,外施1%蛇床子素水乳剂对瓜类、草莓、花卉白粉病的防效在95%以上[29]。此外,植物受病原菌侵染后会产生香豆素类化合物,如大豆锈菌侵染的拟南芥可通过激活苯丙烷类代谢途径相关基因的表达,诱导产生东莨菪内酯,提高对病原菌的抗性;同时外源施用东莨菪内酯能够抑制大豆锈菌生长,降低大豆锈病的发生率[30]。在枸杞的叶和芽中秦皮素和东莨菪内酯含量与根腐病抗性呈正相关,果实中伞形花内酯、佛手柑内酯和茴芹内酯含量与抗根腐病能力呈正相关[31]。
除香豆素及其衍生物外,异戊烯醇脂类化合物在抗感猕猴桃种质响应溃疡病菌侵染过程中差异积累。异戊烯醇脂类物质是以异戊烯醇序列作为母核的化合物,是异戊二烯单位的缩合体,主要包括萜类及其衍生物[32]。研究表明从毛莲蒿(Artemisia vestita)中分离出的4 种倍半萜类化合物artemivestinolide,对多种病原菌如稻瘟病菌(Pyricularia oryzae)、尖孢镰刀菌(Fusarium oxysporum)、灰霉菌(Botrytis cinerea)等具有良好的抑菌效果[33]。柠檬烯能抑制核盘菌、辣椒疫霉菌、灰霉菌的活性,同时通过提高烟草中SA 和H2O2含量及上调防御相关的病程相关蛋白(NPR1、PR1 和PR5)表达量,从而诱导烟草对花叶病毒产生显著抗性[34]。此外,异戊二烯能够通过调控活性氧(ROS)平衡和MAPK 级联反应增强JA 信号,促进防御代谢物的合成,调节植物抗氧化系统和细胞膜稳定性,以增强拟南芥对丁香假单胞菌的抗性[35]。
KEGG 富集分析结果显示,抗感种质间的差异代谢物富集于植物次生代谢产物合成通路,表明在病原菌侵染下植物体内的次生代谢物活动显著增强。异戊烯基转移酶(prenyltransferase)等一些调节异戊烯醇脂类化合物生物合成途径的关键酶活性增强,促使植物快速合成具有防御功能的次生代谢产物,增强自身的防御能力。与KEGG 富集分析结果一致,本研究筛选出的潜在抗性相关代谢物甘草酸(三萜类)和缬草素(二萜类),是植物体内重要的次生代谢物质,能直接或间接增强植物的防御功能。其中,甘草酸含量在病菌侵染后第7~14 天急剧升高,表明其与抗病代谢紧密相关,值得后期重点关注。此外,87 种代谢物在抗病种质中的含量始终高于感病种质,很可能与猕猴桃响应溃疡病菌侵染相关,后续可经体外抑菌试验等验证后,进一步研发新型生防药剂,应用于猕猴桃溃疡病的防治。
笔者在抗感种质间的差异代谢物分类中鉴定到33 种黄酮类(flavonoids)、21 种酚类(phenols)、14 种香豆素及其衍生物(coumarins and derivatives)和11种肉桂酸及其衍生物(cinnamic acids and derivative)等物质。KEGG 分析结果同样显示,苯丙烷类生物合成通路和苯丙氨酸代谢通路在抗感种质间显著富集。苯丙烷类生物合成是植物防御病原菌的核心代谢途径,在植物的生长发育过程及应答逆境胁迫中发挥重要作用[36]。苯丙烷代谢途径始于莽草酸途径产生的苯丙氨酸,在苯丙氨酸解氨酶的催化作用下生成肉桂酸(PAL),经过肉桂酸-4-羟基化酶(C4H)和4-香豆酰辅酶A(4CL)关键酶的作用,合成香豆酰CoA[37],进一步通过不同途径转化为不同的苯丙烷类代谢产物。苯丙烷类物质以羟基芳香环为共同特征,包括总黄酮、黄酮醇、香豆素、木质素、花青素以及单宁等苯类化合物[38],与植物抗病性密切相关。Zhang等[39]研究发现,绿原酸通过诱导间座壳属真菌菌丝线粒体中ROS 的积累,导致病菌线粒体功能受损,并触发真菌细胞凋亡,从而减少猕猴桃采后腐烂。Jiao 等[40]发现绿原酸能通过激活水杨酸信号通路诱导桃果实对青霉菌产生抗性,降低青霉病发病率和病斑直径。Xu 等[41]研究表明,对羟基苯甲酸和4-香豆酸2∶1 混合液对核桃炭疽病具有显著的抑制作用。同时,对羟基苯甲酸可诱导番茄和黄瓜植株对丁香假单胞菌产生抗性[42]以及抑制猕猴桃中黄曲霉的生长[43]。本研究发现苯丙烷类生物合成通路在抗感种质间显著富集,表明在病原菌侵染过程中猕猴桃体内的苯丙烷类代谢通路增强。因此,苯丙烷类生物合成通路以及苯丙烷代谢通路可能是猕猴桃响应溃疡病菌侵染的关键代谢途径,后续可进行进一步的分析验证。
4 结 论
笔者利用非靶向代谢组技术分析了猕猴桃抗病种质E2545 和感病种质E674 在溃疡病菌侵染后不同时期的代谢物差异。结果表明,抗感猕猴桃种质间差异代谢物种类主要为苯和取代衍生物、香豆素及其衍生物、异戊烯醇脂类、羧酸及其衍生物等;87种共有差异代谢物在抗病材料中的含量始终高于感病材料,表明这些物质可能在猕猴桃防御溃疡病菌中发挥重要作用;筛选出阿司匹林、甘草酸、pestalactam B、缬草素4种可能具有应用潜力的防御相关代谢物,后续可结合抑菌试验进一步验证其防效,研发新型生防药剂应用于猕猴桃溃疡病的防治;苯丙烷类生物合成通路以及苯丙烷代谢通路可能是猕猴桃响应溃疡病菌侵染的关键代谢途径,具体抗性机制还需要进一步深入研究。
[1] 李想,石广丽,耿佳麒,郭建辉,刘雨萌,孙丹,王振兴,张苏苏,唐倩,艾军. 温室栽培对软枣猕猴桃光合特性及果实品质的影响[J]. 果树学报,2024,41(1):89-100.LI Xiang,SHI Guangli,GENG Jiaqi,GUO Jianhui,LIU Yumeng,SUN Dan,WANG Zhenxing,ZHANG Susu,TANG Qian,AI Jun. Effects of greenhouse cultivation on the photosynthetic characteristics and fruit quality of Actinidia arguta[J].Journal of Fruit Science,2024,41(1):89-100.
[2] 莫沙,石深深,田洁,朱佳慧,王仁才,罗飞雄. 对萼猕猴桃多样性分析及其性别鉴定[J]. 果树学报,2024,41(11):2182-2194.MO Sha,SHI Shenshen,TIAN Jie,ZHU Jiahui,WANG Rencai,LUO Feixiong. Study on diversity and sex determination of Actinidia valvata[J]. Journal of Fruit Science,2024,41(11):2182-2194.
[3] 李大卫,黄文俊,钟彩虹. 中国猕猴桃产业现状及“十五五” 发展建议[J]. 果树学报,2024,41(11):2149-2159.LI Dawei,HUANG Wenjun,ZHONG Caihong. Current status of China’s kiwifruit industry and development recommendations for the “15th Five-Year Plan”[J]. Journal of Fruit Science,2024,41(11):2149-2159.
[4] 联合国粮农组织数据库[OL]. https://www.fao.org/statistics/en/.Database of the food and agriculture organization of the United Nations[OL]. https://www.fao.org/statistics/en/.
[5] LI Y,ZHU Q M,ZHI T H,FAN R,XIE T,ZHAO Z B,LONG Y H,LI Z. Genetic causes of non-pathogenic Pseudomonas syringae pv. actinidiae isolates in kiwifruit orchards[J]. Frontiers in Microbiology,2021,12:650099.
[6] 张敏,唐冬梅,赵志博,仲伟敏. 贵州产区黄肉猕猴桃品种及优系溃疡病抗性评价[J]. 分子植物育种,2021,19(23):7892-7899.ZHANG Min,TANG Dongmei,ZHAO Zhibo,ZHONG Weimin. Evaluation of canker resistance on yellow-fleshed kiwifruit cultivars and superior lines in Guizhou[J]. Molecular Plant Breeding,2021,19(23):7892-7899.
[7] TANG H R,WANG Y L. Metabonomics:A revolution in progress[J]. Progress in Biochemistry and Biophysics,2006,33(5):401-417.
[8] 陶美奇,潘永飞,山溪,戴忠良,张振超. 基于非靶向代谢组学对青花菜花球表面蜡粉代谢物的差异分析[J]. 中国蔬菜,2024(5):51-58.TAO Meiqi,PAN Yongfei,SHAN Xi,DAI Zhongliang,ZHANG Zhenchao. Differential analysis of metabolites in wax powder on surface of broccoli florets based on non-targeted metabolomics[J]. China Vegetables,2024(5):51-58.
[9] 王溢,黄润生,程俊森,李永泉,张庆威,张晖. 基于UPLC-MS/MS 的油茶种仁成分差异分析及其油脂抗氧化活性研究[J].中国食品学报,2023,23(8):329-341.WANG Yi,HUANG Runsheng,CHENG Junsen,LI Yongquan,ZHANG Qingwei,ZHANG Hui. Differential composition analysis of seed kernels between two Camellia species by UPLC-MS/MS and the antioxidant activity research of seed kernels oil[J].Journal of Chinese Institute of Food Science and Technology,2023,23(8):329-341.
[10] LIU F J,JIANG Y,LI P,LIU Y D,YAO Z P,XIN G Z,LI H J.Untargeted metabolomics coupled with chemometric analysis reveals species-specific steroidal alkaloids for the authentication of medicinal Fritillariae Bulbus and relevant products[J]. Journal of Chromatography A,2020,1612:460630.
[11] 牛晓雪,包艳存,雷霆,李付军,李霞,牟萌,路远,李保华. 基于非靶向代谢组学的芦笋代谢物差异分析[J]. 中国蔬菜,2025(2):71-81.NIU Xiaoxue,BAO Yancun,LEI Ting,LI Fujun,LI Xia,MU Meng,LU Yuan,LI Baohua. Analysis of different metabolites in Asparagus by non-targeted metabolomics[J]. China Vegetables,2025(2):71-81.
[12] LV J H,DENG M H,LI Z S,ZHU H S,WANG Z R,YUE Y L,YANG Z G,XU J Q,JIANG S R,ZHAO W,LI J,ZHAO K. Integrative analysis of the transcriptome and metabolome reveals the response mechanism to tomato spotted wilt virus[J]. Horticultural Plant Journal,2023,9(5):958-970.
[13] LI J W,HUANG T M,LU J B,XU X H,ZHANG W P. Metabonomic profiling of clubroot-susceptible and clubroot-resistant radish and the assessment of disease-resistant metabolites[J].Frontiers in Plant Science,2022,13:1037633.
[14] XIAO X O,LIN W Q,FENG E Y,OU X C. Transcriptome and metabolome response of eggplant against Ralstonia solanacearum infection[J]. PeerJ,2023,11:e14658.
[15] DUAN B,REYMICK O O,LIU Z G,ZHOU Y,WANG X,FENG Z,TAO N G. Citral enhances disease resistance in postharvest citrus fruit through inducing jasmonic acid pathway and accumulating phenylpropanoid compounds[J]. Postharvest Biology and Technology,2024,207:112633.
[16] LIU S J,XU Y T,YANG K,HUANG Y,LU Z H,CHEN S L,GAO X,XIAO G A,CHEN P,ZENG X L,WANG L,ZHENG W K,LIU Z S,LIAO G L,HE F,LIU J J,WAN P F,DING F,YE J L,JIAO W B,CHAI L J,PAN Z Y,ZHANG F,LIN Z C,ZAN Y J,GUO W W,LARKIN R M,XIE Z Z,WANG X,DENG X X,XU Q. Origin and de novo domestication of sweet orange[J]. Nature Genetics,2025,57(3):754-762.
[17] 贺迪,钟彩虹,朱佳慧,潘慧,李文艺,杨洁,黄跃,刘普,李黎.山梨与中华猕猴桃种间杂交群体的抗病性评价及抗病机制的研究[J]. 果树学报,2024,41(11):2235-2249.HE Di,ZHONG Caihong,ZHU Jiahui,PAN Hui,LI Wenyi,YANG Jie,HUANG Yue,LIU Pu,LI Li. Evaluation of disease resistance and research of resistance mechanism of kiwifruit hybrid population derived from Actinidia rufa and Actinidia chinensis var. chinensis[J]. Journal of Fruit Science,2024,41(11):2235-2249.
[18] ZHAO Z B,GAO X N,HUANG Q L,HUANG L L,QIN H Q,KANG Z S. Identification and characterization of the causal agent of bacterial canker of kiwifruit in the Shaanxi province of China[J]. Journal of Plant Pathology,2013,95(1):155-162.
[19] 朱佳慧,李黎,贺迪,潘慧,李文艺,张琦,王仁才,钟彩虹. 猕猴桃主栽品种溃疡病抗性评价及生理指标分析[J]. 果树学报,2024,41(11):2312-2322.ZHU Jiahui,LI Li,HE Di,PAN Hui,LI Wenyi,ZHANG Qi,WANG Rencai,ZHONG Caihong. Evaluation on bacterial canker disease and analysis of physiological indexes in main kiwifruit cultivars[J]. Journal of Fruit Science,2024,41(11):2312-2322.
[20] 秦红艳. 软枣猕猴桃对细菌性溃疡病(Psa)侵染的生理响应及多组学分析[D]. 北京:中国农业科学院,2022.QIN Hongyan. Physiological response and multi-omics analysis of Actinidia arguta to bacterial canker (Psa) infection[D]. Beijing:Chinese Academy of Agricultural Sciences,2022.
[21] WANG J L,ZHANG T,SHEN X T,LIU J,ZHAO D L,SUN Y W,WANG L,LIU Y J,GONG X Y,LIU Y X,ZHU Z J,XUE F Z. Serum metabolomics for early diagnosis of esophageal squamous cell carcinoma by UHPLC-QTOF/MS[J]. Metabolomics,2016,12(7):116.
[22] SENTHIL- KUMAR M,MYSORE K S. Nonhost resistance against bacterial pathogens:Retrospectives and prospects[J]. Annual Review of Phytopathology,2013,51:407-427.
[23] 杨亮. 羟基香豆素类化合物对青枯雷尔氏菌致病特性的调控作用研究[D]. 重庆:西南大学,2020.YANG Liang. The effect of hydroxycoumarins on regulating virulence characteristics of Ralstonia solanacearum[D]. Chongqing:Southwest University,2020.
[24] SCHMIDT R,DURLING M B,DE JAGER V,MENEZES R C,NORDKVIST E,SVATOŠ A,DUBEY M,LAUTERBACH L,DICKSCHAT J S,KARLSSON M,GARBEVA P. Deciphering the genome and secondary metabolome of the plant pathogen Fusarium culmorum[J]. FEMS Microbiology Ecology,2018,94(6):4990469.
[25] 麻子君,吴雅倩,金鑫,丁伟,李石力. 东莨菪内酯与瑞香素诱导柑橘抗溃疡病的效果评价[J]. 植物医学,2025,4(1):20-27.MA Zijun,WU Yaqian,JIN Xin,DING Wei,LI Shili. Evaluation of scopoletin and daphnetin for induction of citrus resistance to canker disease[J]. Plant Health and Medicine,2025,4(1):20-27.
[26] 徐文雅,朱玉燕,徐启航,李生娥,沈淑铃,姚兰英,郑小林. 伞形花内酯处理对采后徐香猕猴桃果实灰霉病抗性的影响[J].核农学报,2021,35(4):846-853.XU Wenya,ZHU Yuyan,XU Qihang,LI Sheng’e,SHEN Shuling,YAO Lanying,ZHENG Xiaolin. Effect of umbelliferone treatment on disease resistance to Botrytis cinerea in kiwifruit cv. Xuxiang during storage[J]. Journal of Nuclear Agricultural Sciences,2021,35(4):846-853.
[27] 王栋,张方贺,孙健,郝双红. 8 种4-甲基香豆素衍生物的合成及其农药活性[J]. 中国农学通报,2013,29(15):199-203.WANG Dong,ZHANG Fanghe,SUN Jian,HAO Shuanghong.Synthesis and pesticidal activity of 8 derivatives of 4-methylcoumarin[J]. Chinese Agricultural Science Bulletin,2013,29(15):199-203.
[28] 张方贺,魏艳,王栋,宋卫,王现刚,郝双红. 8 种甲基香豆素衍生物的抑菌及除草活性[J]. 农药,2011,50(6):455-457.ZHANG Fanghe,WEI Yan,WANG Dong,SONG Wei,WANG Xiangang,HAO Shuanghong. Inhibitory and herbicidal activities of eight methyl coumarin derivatives[J]. Agrochemicals,2011,50(6):455-457.
[29] 杨亮,姚晓远,丁伟. 香豆素类化合物的抑菌活性研究[J]. 天然产物研究与开发,2018,30(2):332-338.YANG Liang,YAO Xiaoyuan,DING Wei. The advances on antibacterial activity of coumarins[J]. Natural Product Research and Development,2018,30(2):332-338.
[30] BEYER S F,BEESLEY A,ROHMANN P F W,SCHULTHEISS H,CONRATH U,LANGENBACH C J G. The Arabidopsis non-host defense-associated coumarin scopoletin protects soybean from Asian soybean rust[J]. The Plant Journal,2019,99(3):397-413.
[31] 孙红亮,孙莘一,辛彩云,谢咸升,赵芳,王睿,张红娟,刘杰辉,李蓉. 枸杞中8 种香豆素类成分含量测定及与抗根腐病关系分析[J/OL]. 分子植物育种,2024:1-24. (2024-01-04). https://link.cnki.net/urlid/46.1068.S.20240103.1515.016.SUN Hongliang,SUN Xinyi,XIN Caiyun,XIE Xiansheng,ZHAO Fang,WANG Rui,ZHANG Hongjuan,LIU Jiehui,LI Rong. Determination of 8 coumarin components in Lycium barbarum and analysis of their relationship with resistance to root rot[J/OL]. Molecular Plant Breeding,2024:1-24. (2024-01-04).https://link.cnki.net/urlid/46.1068.S.20240103.1515.016.
[32] 万娅,孟栋,李金玲,李春,王颖. 细胞区室化调控萜类化合物微生物合成[J]. 中国生物工程杂志,2023,43(9):93-104.WAN Ya,MENG Dong,LI Jinling,LI Chun,WANG Ying. Research progress of subcellular compartmentalization regulation of microbial synthesis of terpenes[J]. China Biotechnology,2023,43(9):93-104.
[33] DING Y H,WANG H T,SHI S,MENG Y,FENG J C,WU H B. Sesquiterpenoids from Artemisia vestita and their antifeedant and antifungal activities[J]. Molecules,2019,24(20):3671.
[34] LUO W,WANG K Y,LUO J Y,LIU Y C,TONG J W,QI M T,JIANG Y,WANG Y,MA Z Q,FENG J T,LEI B,YAN H. Limonene anti-TMV activity and its mode of action[J]. Pesticide Biochemistry and Physiology,2023,194:105512.
[35] FRANK L,WENIG M,GHIRARDO A,VAN DER KROL A,VLOT A C,SCHNITZLER J P,ROSENKRANZ M. Isoprene and β-caryophyllene confer plant resistance via different plant internal signalling pathways[J]. Plant,Cell & Environment,2021,44(4):1151-1164.
[36] XU Q,YIN X R,ZENG J K,GE H,SONG M,XU C J,LI X,FERGUSON I B,CHEN K S. Activator- and repressor-type MYB transcription factors are involved in chilling injury induced flesh lignification in loquat via their interactions with the phenylpropanoid pathway[J]. Journal of Experimental Botany,2014,65(15):4349-4359.
[37] 穆红梅,杜秀菊,张秀省,张敏,曹兴. 植物MYB 转录因子调控苯丙烷类生物合成研究[J]. 北方园艺,2015(24):171-174.MU Hongmei,DU Xiuju,ZHANG Xiusheng,ZHANG Min,CAO Xing. Study on plants MYB transcription factors regulate biological synthesis of phenylpropanoid metabolism[J]. Northern Horticulture,2015(24):171-174.
[38] 王玉,杨雪,杨蕊菁,王玉霞,杨飞霞,夏鹏飞,赵磊. 调控苯丙烷类生物合成的MYB 类转录因子研究进展[J]. 安徽农业大学学报,2019,46(5):859-864.WANG Yu,YANG Xue,YANG Ruijing,WANG Yuxia,YANG Feixia,XIA Pengfei,ZHAO Lei. Advances in research of MYB transcription factors in regulating phenylpropane biosynthesis[J].Journal of Anhui Agricultural University,2019,46(5):859-864.
[39] ZHANG D F,BI W L,KAI K,YE Y W,LIU J. Effect of chlorogenic acid on controlling kiwifruit postharvest decay caused by Diaporthe sp.[J]. LWT-Food Science and Technology,2020,132:109805.
[40] JIAO W X,LI X X,WANG X M,CAO J K,JIANG W B. Chlorogenic acid induces resistance against Penicillium expansum in peach fruit by activating the salicylic acid signaling pathway[J].Food Chemistry,2018,260:274-282.
[41] XU H F,WANG G F,ZHANG J,ZHANG M J,FU M R,XIANG K,ZHANG M Y,CHEN X. Identification of phenolic compounds and active antifungal ingredients of walnut in response to anthracnose (Colletotrichum gloeosporioides)[J]. Postharvest Biology and Technology,2022,192:112019.
[42] GOODWIN P H,TRUEMAN C,LOEWEN S A,TAZHOOR R.Variation in the responsiveness of induced resistance against Pseudomonas syringae pv. tomato by Solanum lycopersicum treated with para-aminobenzoic acid[J]. Physiological and Molecular Plant Pathology,2018,104:31-39.
[43] HUO Z Y,SHI X C,WANG Y X,JIANG Y H,ZHU G Y,HERRERA-BALANDRANO D D,WANG S Y,LABORDA P. Antifungal and elicitor activities of p-hydroxybenzoic acid for the control of aflatoxigenic Aspergillus flavus in kiwifruit[J]. Food Research International,2023,173:113331.